安徽省池州市第一中学2019-2020学年高一下学期期中教学质量检测化学试题
安徽
高一
期中
2020-06-11
419次
整体难度:
适中
考查范围:
化学反应原理、物质结构与性质、认识化学科学、常见无机物及其应用、化学实验基础
安徽省池州市第一中学2019-2020学年高一下学期期中教学质量检测化学试题
安徽
高一
期中
2020-06-11
419次
整体难度:
适中
考查范围:
化学反应原理、物质结构与性质、认识化学科学、常见无机物及其应用、化学实验基础
一、单选题 添加题型下试题
1. 最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的示意图如下:
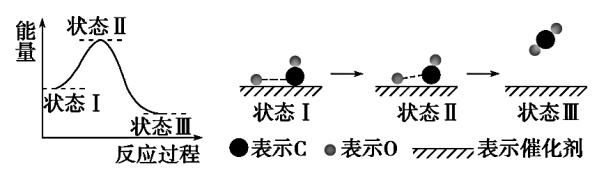
下列说法中正确的是

下列说法中正确的是
| A.CO和O生成CO2是吸热反应 |
| B.在该过程中,CO断键形成C和O |
| C.CO和O生成了具有极性共价键的CO2 |
| D.状态Ⅰ →状态Ⅲ表示CO与O2反应的过程 |
您最近一年使用:0次
2019-01-30更新
|
8855次组卷
|
196卷引用:2015年全国普通高等学校招生统一考试化学(北京卷)
2015年全国普通高等学校招生统一考试化学(北京卷)2014-2015学年四川省成都市树德中学高一下学期期末考试化学试卷河北省衡水中学2015-2016学年高二上一调考试化学试卷2016届河南省扶沟县高级中学高三上学期开学考试化学试卷2015-2016学年河北省衡水中学高二上学期调考化学试卷2015-2016学年福建省福州格致中学高二上学期半期考试化学试卷2015-2016学年山东枣庄三中高二10月学情调查化学卷2016届宁夏六盘山高级中学高三上学期期中考试化学试卷2015-2016学年河北省衡水二中高二上期中测试化学试卷2016届甘肃省嘉峪关一中高三上第三次模拟考试化学试卷2015-2016学年浙江省桐乡市高级中学高二上期中(普通班)化学试卷2016届上海市十一校高三上学期12月联考化学试卷2015-2016学年湖南省株洲二中高二上学期期末化学试卷2015-2016学年湖南省常德一中高二上学期期末理化学试卷2016届江苏省清江中学高三下冲刺模拟二化学试卷2015-2016学年四川省资阳市高一下学期期末化学试卷2016-2017学年河北冀州市中学高二上开学调研化学卷2016-2017学年湖南省长沙一中高二上第一次月考化学卷2016-2017学年辽宁沈阳东北育才学校高二阶段考一化学卷2017届山东师范大学附属中学高三上第二次模拟考试化学试卷2016-2017学年湖南省株洲二中高二上月考三化学卷2016-2017学年云南省云天化中学高二上学期期末考试化学(理)试卷江苏省泰州中学2016-2017学年高一5月月度检测化学试题山西省太原市第五中学2016-2017学年高一5月月考化学试题2【全国百强校】山西省太原市第五中学2016-2017学年高一5月月考化学试题湖北省部分重点中学2018届高三起点考试化学试题北京市清华大学附属中学2016-2017学年高一下学期期中考试化学试题河南省林州市第一中学2017-2018学年高二上学期开学考试化学试题黑龙江省哈尔滨市第六中学2018届高三9月阶段检测化学试题山西省忻州市第一中学2017-2018学年高二上学期摸底考试化学试题山西省山西大学附属中学2017-2018学年高二上学期9月月考化学试题山东省潍坊市2017-2018学年高二上学期期中考试化学试题山东省青岛市城阳区2018届高三上学期期中学分认定考试化学试题甘肃省武威第十八中学2018届高三上学期第三次月考化学试题(已下线)2017-2018学年上学期期末复习备考之精准复习模拟题高二化学选修4(C卷)北京市西城区重点中学2018届高三上学期期末复习检验化学试题浙江省杭十四中2018年高三化学选考3月考试试题卷(1)(已下线)【中等生百日捷进提升系列-技能方法】专题13 化学反应与能量类选择题解题方法和策略湖北省长望浏宁四县2018届高三3月联合调研考试理综化学试题湖北省襄阳市第四中学2017-2018学年高一3月月考化学试题(已下线)《周末培优君》2017-2018学年高一下学期化学-第05周 化学能与热能(已下线)2018年高考题及模拟题汇编 专题07 化学反应中的能量变化(已下线)第07天 吸热反应与放热反应的比较——《每日一题·2018快乐暑假》高二化学北京市第一七一中学2018-2019学年高二上学期期中考试化学试题高二人教版选修4 第一章 第一节 化学反应与能量的变化(已下线)2019高考备考二轮复习精品资料-专题8 化学反应中与能量变化(教学案)河南省中牟县第一高级中学2018-2019学年高一下学期第一次统一考试化学试题(已下线)2019年3月11日 《每日一题》 必修2 化学键与化学反应中能量变化的关系【全国百强校】广西自治区桂林市第十八中学2018-2019学年高二下学期开学考试化学试题河南省周口市扶沟县高级中学2018-2019学年高一下学期第一次月考化学试题【全国百强校】甘肃省兰州市第一中学2018-2019学年高一下学期期中考试化学试题河北安平中学2018-2019学年高一下学期期中考试化学(实验班)试题河南省周口扶沟县高级中学2018-2019学年高一下学期第二次月考化学试题河北安平中学2018-2019学年高二下学期期末考试化学试题云南省普洱市澜沧县民族中学2018-2019学年高二下学期期末考试化学试题北京四中2018-2019学年高一下学期期末考试化学试题安徽省合肥第十一中学2019-2020学年高二上学期入学考试化学试题贵州省遵义航天高级中学2019-2020学年高二上学期期中考试化学(理)试题黑龙江省绥化市青冈县第一中学2019-2020学年高二上学期(A)班月考化学试题贵州省遵义市南白中学2019-2020学年高二上学期期中考试化学试题2019—2020学年高二上学期化学期末复习—选择题专题训练一云南师范大学附属中学2019-2020学年高二上学期期中考试化学试题江西省新余市分宜中学2019-2020学年高二上学期第二次段考化学试题2020届高三化学二轮冲刺新题专练——能量变化的图像分析2020届高三化学选修4二轮专题练——中和热及其测定【选择精编25题】2020届高三化学知识点强化训练—化学反应中能量变化云南省曲靖市宣威市第九中学2019-2020学年高二上学期第二次段考化学试题上海市六校联考2016届高考模拟试卷(3月份)化学试题上海市六校2016届高三3月综合素养调考化学试题河北省邯郸市第一中学2019—2020学年高一4月月考化学试题山东省潍坊市2019-2020学年高一下学期4月阶段考试化学试题(已下线)专题九 化学能与热能(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训湖北省武汉市第三十九中学2019-2020学年高一下学期线上期中考试化学试题北京市101中学2019-2020学年高三化学统考三上海市宝山区2020届高三第二次模拟化学试题河北省石家庄市第二中学2020届高中毕业班四月份教学质量监测卷理科综合化学部分吉林省辽源市辽县第一高级中学2019-2020高一下学期期中考试化学试题山东省济宁市汶上圣泽中学2019-2020学年高一下学期第二次月考化学试题(已下线)专题6.1 化学能与热能(讲)——2020年高考化学一轮复习讲练测安徽省池州市第一中学2019-2020学年高一下学期期中教学质量检测化学试题江西省赣州市南康中学2019-2020学年高一下学期第二次大考化学试题北京市海淀区北京理工大学附中2019-2020学年高一下学期期末练习化学试题黑龙江省大庆市肇州县第二中学2019-2020学年高一下学期期末考试化学试题山东省济宁市2020届高三一模化学试卷湖南省长沙市雅礼中学2020届高三上学期第3次月考化学试题(已下线)1.1.1 反应热 焓变(练习)——2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)山东省滕州市第一中学2020-2021学年高二9月开学收心考试化学试题河南省开封市2019-2020学年高二下学期期末调研考试化学试题山东省菏泽市单县第五中学2020-2021学年高二上学期开学考试化学试题(已下线)第一章 化学反应的热效应(能力提升)-2020-2021学年高二化学单元测试定心卷(人教版2019选择性必修一)北京市第101中学2020届高三4月月考化学试题鲁科版(2019)高一必修第二册 第2章 化学键 反应规律 第二节 化学反应与能量转化 高考帮高一必修第二册(人教2019版)第六章 化学反应与能量 素养检测(已下线)【南昌新东方】3. 进贤一中 田荣达陕西省西安市第八十九中学2018-2019学年高二上学期期中考试化学试题湖南省岳阳市平江县第一中学2020-2021学年高二上学期10月联考化学试题(已下线)第19讲 化学能与热能 (精讲)——2021年高考化学一轮复习讲练测鲁科版(2019)高二选择性必修第一册第1章 化学反应与能量变化 过素养 学科素养拓展训练人教版(2019)高二化学选择性必修1第一章 化学反应的热效应 过素养 学科素养拓展训练广东省揭阳市第三中学2020-2021学年高二上学期期中考化学试题湖南省湘阴县知源学校2020-2021学年高二上学期9月月考化学试题河南省郑州市郑州中学2020-2021学年高二上学期期中考试化学试题浙江省宁波市北仑中学2020-2021学年高一上学期期中考试化学(1班)试题海南省北京师范大学万宁附属中学2019-2020学年高一下学期期中考试化学试题河南省驻马店市2020-2021学年高二上学期期终考试化学试题天津市南开区2021届高三上学期期末考试化学试题山东省聊城市茌平区第二中学2020-2021学年高二上学期第二次月考化学试题(人教版2019)必修第二册 第六章 化学反应与能量 第一节 化学反应与能量变化四川省雅安中学2020-2021学年高一下学期开学考试化学试题湖南师范大学附属中学、长沙市第一中学2019-2020学年高一下学期期中联考化学试题湖南省长沙市南雅中学2019-2020学年高一下学期期中考试化学试题山东省济宁市鱼台县第一中学2020-2021学年高一下学期第一次月考化学试题江西省抚州市南城一中2020-2021学年高一下学期4月月考化学试题江西省上高二中2020-2021学年高一下学期第四次月考试题(4月)化学试题安徽省淮北市第一中学2020-2021学年高一下学期第二次月考化学试题山东省齐河县第一中学2020-2021学年高一下学期第一次月考化学试题浙江之江教育评价2020-2021学年高一下学期期中联考化学试题江苏省苏州市吴中区2020-2021学年高二下学期期中调研测试化学试题浙江省北斗联盟2020-2021学年高一下学期期中联考化学试题北京师范大学附属中学2020-2021学年高一下学期期中考试化学(选考班)试题(已下线)【浙江新东方】高中化学20210513-045【2021】【高一下】广东省珠海市第二中学2020-2021学年高一下学期期中考试化学试题吉林省长春外国语学校2020-2021学年高一下学期期中考试化学(理科)试题河北省石家庄市第二十三中学2020-2021学年高一第二学期5月月考化学试题河北省临漳县第一中学2020-2021学年高一下学期3月份月考化学试题黑龙江省哈尔滨宾县第一中学2020-2021学年高一下学期第一次月考化学试题云南省易门一中2020-2021学年高二6月月考化学试题吉林省白城一中、大安一中、通榆一中、洮南一中、镇赉一中2020-2021学年高一下学期期末考试化学试题江西省宜春市第九中学2020-2021学年高一下学期第二次月考化学试题选择性必修1(SJ)专题1专题综合检测重庆市清华中学2020-2021学年高一下学期第一次月考化学试题(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(浙江专用)北京市延庆区2020-2021学年高一下学期期中考试化学试题云南省曲靖市罗平县第二中学2020-2021学年高一下学期6月月考化学试题湖南省长沙市周南中学2021-2022学年高二上学期入学考试化学试题江苏省外国语学校2020-2021学年高二下学期期中调研测试化学试卷贵州省毕节市金沙县第一中学2021-2022学年高二上学期第一次月考化学试题江苏省华东师范大学盐城实验中学2021-2022学年高二上学期第一次月考化学试题 江苏省扬州中学2021-2022学年高二上学期10月阶段检测化学试题北京市昌平区新学道临川学校2021-2022学年高二上学期第一次月考化学试题青海省西宁市北外附属新华联国际学校2021-2022学年高二上学期第一次月考化学(理)试题黑龙江省哈尔滨市依兰县高级中学2021-2022学年高二上学期第一次月考化学试题山西省太原市第五中学2016-2017学年高一5月月考化学试题1广西罗城仫佬族自治县高级中学2021-2022学年高二上学期开学检测化学试题山东省2021-2022学年高二12月“山东学情”联考(人教版)化学试题宁夏六盘山高级中学2021-2022学年高二上学期期中考试化学试题河南省重点高中2021-2022学年高二上学期阶段性调研联考二化学试题河南省中原名校联盟2021-2022学年高二上学期第三次适应性联考化学试题广东省梅州市丰顺县和五华县2022届高三1月质检(一模)化学试题北京市平谷区2021-2022学年高二上学期期末化学试题(已下线)第10讲 化学反应与热能(word讲义)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)天津市红桥区2020-2021学年高三上学期期末考试化学试题(已下线)【期中复习】必刷题-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)内蒙古赤峰二中2021-2022学年高一下学期第一次月考化学试题湖北省沙市中学2021-2022学年高一下学期期中考试化学试题广东省大联考2021-2022学年高一下学期期中检测化学试题北京市汇文中学2021-2022学年高一下学期期中考试化学试题河北省沧州市沧县中学2021-2022学年高一下学期4月月考化学试题甘肃省永昌县第一高级中学2021-2022学年高一下学期期中选择性考试化学试题辽宁省沈阳市第八十三中学2021-2022学年高一下学期6月复学考试化学试题(已下线)考点17 化学反应的热效应-备战2023年高考化学一轮复习考点帮(全国通用)北京师范大学附属中学2021-2022学年高一下学期期中考试化学试题江苏省溧阳市2021-2022学年高一下学期期末教学质量调研化学试题四川省遂宁中学校2020-2021学年高二下学期第一次月考化学试题江苏省盐城市田家炳中学2021-2022学年高二上学期期中考试化学(选修)试题湖南省长沙市宁乡市2021-2022学年高一下学期期末考试化学试题河南省开封市五县2021-2022学年高二上学期期末考试化学试题湖南省永州市祁阳县2021-2022学年高三下学期一模联考化学试题贵州省黔东南州2020-2021学年高一下学期期末考试化学试题西藏拉萨市第二高级中学2021-2022学年高二上学期期中考试化学试题江苏省盐城市东台创新高级中学2021-2022学年高二4月份月检测化学试题黑龙江省大庆市东风中学2022-2023学年高二10月月考化学试题湖南省株洲市五雅中学2022-2023学年高二上学期11月期中考试化学试题河南省兰考县第二高级中学2021-2022学年高二上学期期中考试化学试题陕西省西安市鄠邑区第二中学2021-2022学年高二上学期第一次月考化学试题安徽省怀宁县第二中学2021-2022学年高三上学期期末考试化学试题江苏省盐城市东台创新高级中学2021-2022学年高一下学期2月份月检测化学试题广东省广州市第一中学2022-2023学年高二上学期期末考试化学试题(已下线)题型97 结合能量变化图像或反应历程图像考查能量变化江西省上饶市2019-2020学年高一下学期期末教学质量测试化学试题黑龙江省齐齐哈尔市第八中学校2022-2023学年高一下学期3月月考化学试题陕西省西安市大联考2022-2023学年高一下学期4月期中考试化学试题广东省广州市白云中学2022-2023学年高一下学期期中考试化学试题云南省昆明市第一中学2022-2023学年高一下学期期中考试化学试题河南省郑州市第一中学2022-2023学年高一下学期期中考试化学试题湖南省长沙市宁乡一中2022-2023学年高一下学期期中测试化学试题浙江省温州环大罗山联盟期中2022-2023学年高一下学期4月期中考试化学试题福建省福州市第七中学2022-2023学年高一下学期期末考试化学试题黑龙江省鹤岗市第一中学2022-2023学年高一下学期期末考试化学试题云南省西双版纳傣族自治州第一中学2022-2023学年高二下学期期末考试化学试题辽宁省鞍山市2023-2024学年高三上学期第一次质量监测化学试题上海交通大学附属中学2023-2024学年高二上学期开学摸底考试化学试题云南省保山市腾冲市2022-2023学年高二上学期期中教育教学质量监测化学试卷黑龙江省哈尔滨师范大学附属中学2023-2024学年高三上学期11月期中化学试题河南省濮阳市南乐县第一高级中学2023-2024学年高一下学期模拟预测化学试题
单选题
|
容易(0.94)
名校
2. 下列说法正确的是
| A.HCl的电子式为H:Cl |
| B.Na2O2只含有离子键 |
| C.质量数为12的C原子符号为12C |
D.用电子式表示KBr的形成过程: |
您最近一年使用:0次
2018-11-13更新
|
1202次组卷
|
11卷引用:【区级联考】北京市海淀区2019届高三第一学期期中考试化学试题
【区级联考】北京市海淀区2019届高三第一学期期中考试化学试题【区级联考】北京市海淀区2019届高三上学期期中考试化学试题河北省隆化县存瑞中学2020届高三上学期第一次质检化学试题河南省郑州市郑州外国语学校2019-2020学年高一下学期第一次调研化学试题重庆市华蓥中学校2019-2020学年高一下学期5月月考化学试题安徽省池州市第一中学2019-2020学年高一下学期期中教学质量检测化学试题甘肃省靖远县第四中学2019-2020学年高一下学期期中考试化学(实验班)试题陕西省榆林市绥德县绥德中学2019-2020学年高一下学期第二次阶段检测化学试题陕西省西北农林科技大学附属中学2021-2022学年高一下学期期中考试化学试题(已下线)4.3化学键-同步学习必备知识北京市东城区东直门中学2021-2022学年高三上学期期中考试化学试题
单选题
|
适中(0.65)
名校
3. 下列说法正确的是
| A.化学反应中的能量变化都表现为热量的变化 |
| B.吸热反应在不加热的条件一定不能发生 |
| C.需要加热才能发生的反应一定是吸热反应,放热反应在常温下一定很容易发生 |
| D.反应是吸热还是放热必须看旧键断裂时吸收的能量和新键生成时释放的能量的大小 |
【知识点】 化学反应中能量变化的原因
您最近一年使用:0次
2016-12-09更新
|
249次组卷
|
5卷引用:2009—2010学年河北冀州中学高一下学期期中考试化学卷
(已下线)2009—2010学年河北冀州中学高一下学期期中考试化学卷(已下线)2010—2011学年江苏省黄桥中学高一第二学期期末复习化学试题22014-2015学年北京市房山区周口店中学高一下期中考试化学试卷安徽省池州市第一中学2019-2020学年高一下学期期中教学质量检测化学试题陕西省西北农林科技大学附属中学2021-2022学年高一下学期期中考试化学试题
单选题
|
容易(0.94)
名校
解题方法
4. 金属及其化合物的转化关系是化学学习的重要内容之一。下列各组物质的转化不能全部通过一步反应直接完成的是
| A.Al→Al2O3→Al(OH)3→AlCl3 | B.Na→NaOH→Na2CO3→NaCl |
| C.Mg→MgCl2→Mg(OH)2→MgSO4 | D.Fe→FeCl2→Fe(OH)2→Fe(OH)3 |
您最近一年使用:0次
2022-11-17更新
|
2460次组卷
|
86卷引用:2014届山东省烟台市高三上学期期末统考化学试卷
(已下线)2014届山东省烟台市高三上学期期末统考化学试卷(已下线)2013-2014学年江西省鹰潭市高一上学期期末考试化学试卷(已下线)2014届广东省韶关市高三4月高考二模理综化学试卷(已下线)2015届宁夏银川市唐徕回民中学高三上学期期中考试化学试卷2014-2015天津市和平区高一上学期期末考试化学试卷2015-2016学年山西省太原五中高一上12月月考化学试卷2015-2016学年河北省永年二中高一上学期12月月考化学试卷2017届广东省深圳市三校高三上学期第一次联考化学卷2016-2017学年江西省南昌市第十中学高一上学期期末考试化学试卷云南省南涧县民族中学2017-2018学年高二12月月考化学试题四川省成都市第七中学2017-2018学年度上学期高一1月阶段性测试化学试题山东省桓台县2017-2018学年高一上学期期末考试化学试题山东省桓台第二中学2017-2018学年高一上学期期末考试化学试题辽宁省抚顺中学2017-2018学年高一上学期期末考试化学试题江西省临川实验学校2017-2018学年高一上学期期末质量检测化学试题黑龙江省牡丹江中学2017-2018学年高一上学期期末考试化学试题福建省莆田第一中学2017-2018学年高一上学期期末考试化学试题(已下线)【艺体生文化课百题突围系列-基础练测】专题2.10 金属及其化合物成都外国语学校2017-2018学年高一下学期期中考试化学试题河北省衡水市安平中学2019届高三上学期第二次月考化学试题【全国百强校】甘肃省天水市第一中学2019届高三上学期一轮复习第二次质量检测化学试题内蒙古第一机械制造(集团)有限公司第一中学2018-2019学年高一上学期12月月考化学试题河北省承德市第一中学2018-2019学年高一上学期第三次月考化学试题贵州省息烽县一中2018-2019学年高一上学期11月考试化学试题【全国百强校】四川省成都市成都外国语学校2018-2019学年高一上学期12月月考化学试题河南省鹤壁市淇县第一中学2018-2019学年高一上学期第三次月考化学试题江西省赣州教育发展联盟2018-2019学年高一上学期12月联考化学试题河南省驻马店市上蔡县第二高级中学2018-2019学年高一上学期期中考试化学试题【校级联考】安徽省六安市毛坦厂中学、金安高级中学2018-2019学年高一上学期期末联考化学试题【校级联考】江西省南昌市八一中学、洪都中学2018-2019学年高一上学期期末考试化学试题内蒙古开来中学2018-2019学年高二下学期期末考试化学试题新疆疏勒县八一中学2018-2019学年高一上学期期末考试化学试题湖南省长郡中学2018-2019学年高二下学期期末考试化学试题吉林省油田第十一中学2020届高三上学期第一次阶段考试化学试题山西省朔州市怀仁一中2018-2019学年高一上学期第五次月考化学试题陕西省西安中学2019-2020学年高一12月月考化学试题广西北海市北海中学2019-2020学年高二上学期期中考试化学试题黑龙江省哈尔滨市第六中学2019-2020学年高一上学期期末考试化学试题人教版高中化学必修一第三章《金属及其化合物》测试卷12019-2020学年高一上学期期末复习《新题速递·化学》12月(考点21-22)(已下线)【南昌新东方】2019 南昌五中 高一下 第一次月考辽宁省大连市普兰店区第一中学2019-2020学年高一上学期期末考试化学试题安徽省池州市第一中学2019-2020学年高一下学期期中教学质量检测化学试题辽宁省本溪满族自治县高级中学2019-2020学年高二下学期期末考试化学试题人教版(2019)高一必修第一册第三章 铁 金属材料 素养拓展区山西省晋中市平遥第四中学2020-2021学年高一上学期10月月考化学试题湖南省邵东县第一中学2021届高三上学期第二次月考化学试题江西省余干县新时代学校2020-2021学年高一上学期阶段测试(二)化学试题黑龙江伊春林业管理局第二中学2021届高三上学期期中考试化学试题江西省上饶市铅山县第一中学2020-2021学年上学期高一联考(自招班)化学试题新疆哈密市第八中学2020届高三上学期期中考试化学试题四川省成都外国语学校2020-2021学年高一下学期开学考试化学试题云南省元江县一中2020-2021学年高一上学期期中考试化学试题福建省泉州第五中学2020-2021学年高一下学期期中考试化学试题2016-2017学年湖北省武汉市第二中学高一上学期期末考试化学试卷河北师范大学田家炳中学2020-2021学年高一上学期第3次月考化学试题湖南省长沙市雅礼中学2021 -2022学年上学期高一12月月考化学试题黑龙江省双鸭山市第一中学2021-2022学年高一上学期期末考试化学试题(已下线)第09练 铁及其化合物-2022年【寒假分层作业】高一化学(人教版2019)山西省大同市2021-2022学年高一上学期期末调研化学试题江西省吉安市2021-2022学年高一上学期期末考试化学试题广东省广州市三校2021-202学年高一上学期期末联考化学试题天津市红桥区2021-2022学年高一上学期期末考试化学试题福建省武平县第一中学2021-2022学年高三上学期11月教学质量检测化学试题江西省吉安市遂川中学2021-2022学年高一上学期第一次月考化学(A卷)试题广东省汕头市潮南区2021-2022学年高一上学期期末考试化学试题甘肃省天水市第一中学2021-2022学年高二上学期学业测试一模化学试题内蒙古霍林郭勒市第一中学2021-2022学年高二上学期12月月考化学试题山西省金科大联考2022-2023学年高三上学期11月质量检测化学试题福建省厦门市大同中学2022-2023学年高一上学期第二次月考化学试卷广东省江门市第一中学2022-2023学年高一上学期期末考试化学试题甘肃省张掖市高台县第一中学2022-2023学年高一下学期开学检测化学试题陕西省西安市第六中学2022-2023学年高一上学期期末考试化学试题黑龙江省富锦市第一中学2022-2023学年高一下学期第一次考试化学试题四川省广安市第二中学校2022-2023学年高一下学期第一次月考化学试题(已下线)专题突破卷03?金属及其化合物?-2024年高考化学一轮复习考点通关卷(新教材新高考)(已下线)考点巩固卷03 金属及其化合物(4大考点48题)-2024年高考化学一轮复习考点通关卷(新高考通用)江西省宜春市宜丰中学2022-2023学年高一上学期期末考试化学试题河南省新乡市原阳县第一高级中学2023-2024学年高一上学期1月月考化学试题江西省南昌市第二中学2023-2024学年高一上学期12月月考考试化学试题河南省南阳市社旗县第一高级中学2023-2024学年高三上学期1月月考化学试题安徽省六安市金寨县青山中学2023-2024学年高一下学期第一次月考化学试题陕西省安康市2023-2024学年高一上学期12月联考化学试题江西省宜春市万载县万载二中 2023?2024 学年高一上学期期末模拟考试化学试卷河南省平顶山市第二中学2023-2024学年高一上学期期末化学试题四川省德阳市外国语学校2023-2024学年高一上学期期末模拟考试化学试题
单选题
|
适中(0.65)
名校
解题方法
5. 用3g块状大理石与30mL3mol·L-1盐酸反应制取CO2气体,若要增大反应速率,可采取的措施是
①再加入30mL1mol·L-1盐酸
②改用30mL6mol·L-1盐酸
③改用3g粉末状大理石
④适当升高温度
①再加入30mL1mol·L-1盐酸
②改用30mL6mol·L-1盐酸
③改用3g粉末状大理石
④适当升高温度
| A.①②④ | B.②③④ | C.①③④ | D.①②③ |
您最近一年使用:0次
2020-08-04更新
|
148次组卷
|
29卷引用:2010年新疆哈巴河县高级中学高二上学期第一次月考化学试题
(已下线)2010年新疆哈巴河县高级中学高二上学期第一次月考化学试题(已下线)2011-2012学年云南省蒙自县文澜高级中学高二上学期期中考试化学试卷2015-2016学年四川省雅安中学高二上期中考试化学试卷2015-2016学年山东省淄博市淄川一中高二上第一次阶段测化学试卷2015-2016学年河北省保定一中高二上学期第一次段考化学试卷2015-2016学年广西南宁市八中高二下学期期中段考化学试卷2015-2016学年浙江金华、温州、台州三市部分学校高一下期中化学卷2015-2016学年甘肃省武威二中高一下期末化学试卷2016-2017学年河南省师大附中高二上期中化学试卷2016-2017学年河南省郏县一高、叶县二高等五校高二上期中化学卷2016-2017学年云南省曲靖一中高二上期中化学试卷陕西省咸阳市西藏民族学院附中2016-2017学年高二12月月考化学卷福建省福州市八县(市)协作校2017-2018学年高二上学期期中联考化学(理)试题福建省清流一中2017-2018学年高二上学期第二阶段(期中)考试化学(理)试题安徽省定远重点中学2017-2018学年高一下学期第一次月考化学试题河北省安平中学2017-2018学年高一下学期期末考试化学试题1内蒙古自治区巴彦淖尔市临河三中2018-2019学年高二上学期期中考试化学试题【校级联考】黑龙江省龙东南七校2018-2019学年高二上学期期末联考化学试题福建省泉州第十六中学2019-2020学年高二上学期期中考试化学(选考班)试题西藏自治区林芝一中2019-2020学年高二上学期期末考试化学试题湖南省常德市石门县第二中学2019-2020学年高二上学期第二次月考化学试题黑龙江省牡丹江市穆棱市第一中学2019-2020学年高二上学期期末考试化学试题安徽省池州市第一中学2019-2020学年高一下学期期中教学质量检测化学试题上海市嘉定区封浜高级中学2019-2020学年高一下学期化学试题山东省菏泽市2019-2020学年高一下学期期中考试 化学试题(B)黑龙江省伊春市伊美区第二中学2019-2020学年高二上学期开学考试化学试题湖南省娄底市第一中学2020-2021学年高二上学期9月月考化学试题华中师范大学海南附属中学2019-2020学年高二上学期第三次月考化学试题吉林省松原市长岭县第三中学2021-2022学年高二上学期第三次考试化学试题
单选题
|
适中(0.65)
真题
名校
6. 主族元素W、X、Y、Z的原子序数依次增加,且均不大于20。W、X、Z最外层电子数之和为10;W与Y同族;W与Z形成的化合物可与浓硫酸反应,其生成物可腐蚀玻璃。下列说法正确的是
| A.常温常压下X的单质为气态 |
| B.Z的氢化物为离子化合物 |
| C.Y和Z形成的化合物的水溶液呈碱性 |
| D.W与Y具有相同的最高化合价 |
【知识点】 元素周期律、元素周期表的推断
您最近一年使用:0次
2018-06-09更新
|
16237次组卷
|
63卷引用:2018年全国普通高等学校招生统一考试化学(新课标I卷)
2018年全国普通高等学校招生统一考试化学(新课标I卷)安徽师范大学附属中学2017-2018学年高一下学期期末考试化学试题河北省安平中学2017-2018学年高一下学期期末考试化学试题2(已下线)2018年高考题及模拟题汇编 专题06 物质结构 元素周期律(已下线)高考母题题源04 元素周期表及周期律河南省天一大联考2017-2018学年高一下学期阶段性测试(四)化学试题【全国百强校】天津市第一中学2019届高三上学期第一次月考化学试题贵州省习水县一中2019届高三上学期12月份考试理科综合化学试题【全国百强校】河南省实验中学2019届高三上学期质量预测模拟(三)化学试题(已下线)2019高考备考二轮复习精品资料-专题7 物质结构与元素周期律(教学案)(已下线)考点07 元素周期律和元素周期表——备战2019年浙江新高考化学考点(已下线)2019年高考总复习巅峰冲刺-专题04 物质结构 元素周期律应试策略【全国百强校】安徽省黄山市屯溪第一中学2018-2019学年高一下学期期中考试化学试题【全国百强校】山西省平遥中学校2018-2019学年高二下学期期中考试化学试题黑龙江省大庆实验中学2018-2019学年高一下学期6月月考化学试题云南省广南县第三中学2020届高三上学期开学考试化学试题云南省文山州广南县第二中学2020届高三上学期9月份考试化学试题云南省西畴县第二中学2020届高三上学期开学考试化学试题云南省玉溪元江民中2020届高三开学考试化学试题云南省大理白族自治州漾濞二中2019—2020学年9月份高三化学考试试题云南省玉溪市江川二中2019-2020学年高三上学期期中考试化学试题吉林省德惠市实验中学、前郭五中等九校2020届高三上学期期中考试化学试题河北省衡水市深州市长江中学2020届高三上学期12月月考化学试题甘肃省武威第一中学2020届高三12月月考化学试题云南省广南县二中2019-2020学年高三上学期期末考试化学试题贵州省荔波高级中学2019-2020学年高三上学期期末考试理综化学试题第1章原子结构与元素周期律 挑战区 模拟高考专题1微观结构与物质的多样性 模拟高考第一章物质结构元素周期律 模拟高考广西壮族自治区崇左市宁明中学2019-2020学年高一上学期期末考试化学试题第1章 原子结构——C挑战区 模拟高考(鲁科版选修3)(已下线)专题八 物质结构与元素周期律(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训宁夏回族自治区银川一中2019-2020学年高二下学期期中考试化学试题内蒙古鄂尔多斯市2020届高考模拟试卷理科综合化学试题(已下线)专题5.2 元素周期律和元素周期表(讲)——2020年高考化学一轮复习讲练测(已下线)专题5.3 化学键(讲)——2020年高考化学一轮复习讲练测(已下线)专题5.2 元素周期律和元素周期表(练)——2020年高考化学一轮复习讲练测(已下线)专题5.3 化学键(练)——2020年高考化学一轮复习讲练测安徽省池州市第一中学2019-2020学年高一下学期期中教学质量检测化学试题云南省昆明市官渡区第一中学2020届高三上学期期中考试理综化学试题苏教版(2020)高一必修第一册专题5 总结检测人教版(2019)高一必修第一册 第四章素养检测(已下线)【全国百强校】黑龙江省大庆实验中学2018-2019学年高一6月月考试化学试题(已下线)第18讲 元素周期律和元素周期表(精讲)——2021年高考化学一轮复习讲练测(已下线)第17讲 原子结构 化学键(精讲)——2021年高考化学一轮复习讲练测(已下线)练习13 元素周期律-2020-2021学年【补习教材·寒假作业】高一化学(人教版)贵州省毕节市金沙县第一中学2020-2021学年高一下学期第一次月考化学试题江西省宜春市第九中学2020-2021学年高一下学期第一次月考化学试题河南省开封市铁路中学2020-2021学年高二下学期期中考试化学试题(已下线)考点07 元素周期律和元素周期表-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点07 元素周期律和元素周期表-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第13讲 原子结构 化学键(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第14讲 元素周期律和元素周期表(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)天津市蓟州区燕山中学2021-2022学年高三上学期第一次月考化学试题河南省南阳市第一中学2019届高三第二十次考试理综化学试题云南省玉溪市三中2021-2022学年高一下学期3月份入学考试 化学试题(已下线)专题06物质结构元素周期律-五年(2018~2022)高考真题汇编(全国卷)(已下线)考点07 元素周期律和元素周期表-备战2023年高考化学一轮复习考点帮(全国通用)黑龙江省密山市第四中学2021-2022学年高三上学期第二次月考化学试题云南省富宁县第一中学2021-2022学年高一下学期开学考试化学试题(已下线)专题07 元素周期律与元素周期表(测)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)第一部分 二轮专题突破 专题9 “位—构—性”综合推断黑龙江省牡丹江市第二高级中学2022-2023学年高二下学期4月月考化学试题
单选题
|
适中(0.65)
名校
解题方法
7. Mg-AgCl电池是一种能被海水激活的一次性贮备电池,电池反应方程式为2AgCl+Mg=Mg2++2Ag+2Cl-。有关该电池的说法正确的是
| A.Mg为电池的正极 |
| B.负极反应式为AgCl+e-=Ag+Cl- |
| C.可用于海上应急照明供电 |
| D.电池工作时,电解质溶液质量不断减轻 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
8. W、X、Y、Z属于短周期元素,其性质或原子结构特点如下表,下列说法不正确的是
| W | 能形成两种常见的氧化物,其中一种可作为呼吸面具中的供氧剂 |
| X | 其单质为双原子分子,且呈黄绿色 |
| Y | 与X同周期,且离子半径为本周期最小 |
| Z | Z的一种核素在考古时常用来鉴定一些文物的年代 |
| A.X分别与W和Y形成的化合物中含有相同的化学键 |
| B.W、X、Y的最高价氧化物的水化物之间可以两两反应 |
| C.X与Z形成的最简单的化合物中X、Z均满足8电子稳定结构 |
| D.1 mol W与氧气完全反应转移的电子数为NA |
您最近一年使用:0次
2018-05-18更新
|
236次组卷
|
3卷引用:2018届高三第三次全国大联考(新课标Ⅱ卷)
(已下线)2018届高三第三次全国大联考(新课标Ⅱ卷)【全国百强校】黑龙江省大庆实验中学2019届高三上学期11月月考(期中)理科综合化学试题安徽省池州市第一中学2019-2020学年高一下学期期中教学质量检测化学试题
单选题
|
较易(0.85)
名校
解题方法
9. 下列物质反应后一定有+3价铁生成的是
①Fe与过量的S反应
②Fe与过量稀硫酸反应后,再向其中加KNO3
③Fe(NO3)2溶液中加少量盐酸
④Fe和Fe2O3的混合物溶于盐酸中
①Fe与过量的S反应
②Fe与过量稀硫酸反应后,再向其中加KNO3
③Fe(NO3)2溶液中加少量盐酸
④Fe和Fe2O3的混合物溶于盐酸中
| A.①② | B.②③ | C.①②③ | D.①②③④ |
您最近一年使用:0次
单选题
|
适中(0.65)
10. 下述实验中均有红棕色气体产生,对比分析所得结论不正确的是
 | 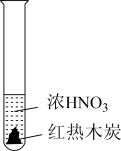 | 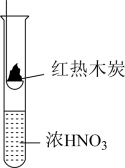 |
| ① | ② | ③ |
| A.由①中的红棕色气体,推断产生的气体一定是混合气体 |
| B.由②中的红棕色气体不能表明木炭与浓硝酸发生了反应 |
| C.由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物 |
| D.③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应 |
【知识点】 硝酸的不稳定性解读 化学实验方案的设计与评价 物质性质的探究解读
您最近一年使用:0次
2022-06-29更新
|
3739次组卷
|
81卷引用:河南省洛阳市第一高级中学2016-2017学年高一6月月考化学试题
河南省洛阳市第一高级中学2016-2017学年高一6月月考化学试题2017年全国普通高等学校招生统一考试理综化学(北京卷精编版)河北省衡水中学2018届高三上学期一调考试化学试题山东省淄博第一中学2018届高三上学期开学考试化学试题四川省德阳市三校2018届高三联合测试化学试题(已下线)黄金30题系列 高一化学 小题好拿分【提升版】北京市清华大学附属中学2018届高三10月月考化学试题广西陆川县中学2018届高三12月月考化学试题北京市一零一中学2018届高三10月月考化学试题宁夏银川一中2017-2018学年高一上学期期末考试化学试题云南省峨山彝族自治县第一中学2018届高三上学期期末考试仿真化学试题黑龙江省伊春中学2017-2018学年高一化学上学期期末考试题河南省三门峡市2017-2018学年高一上学期期末考试化学试题广西陆川县中学2018届高三3月月考化学试题云南省玉溪第一中学2017-2018学年高一下学期4月月考化学试题云南省玉溪市玉溪一中2017-2018学年高一下学期4月月考化学试题(已下线)解密06 非金属及其化合物(教师版)——备战2018年高考化学之高频考点解密(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第4讲 氮及其化合物【教学案】云南省玉溪市峨山一中2019届高三9月月考化学试题江苏省常州市第一中学2019届高三第一学期期初(8月)考试化学试题【全国百强校】陕西省西安市长安区第一中学2018-2019学年高一上学期期末考试化学试题【全国百强校】山西省山西大学附属中学2018-2019学年高一下学期2月模块诊断化学试题福建省泉州市泉港区第一中学2018-2019学年高一下学期期中考试化学试题百所名校联考-非金属及其化合物内蒙古包头稀土高新区二中2020届高三10月月考理综化学试题四川省绵阳市南山中学2020届高三10月月考化学试题(已下线)2019年12月11日 《每日一题》化学人教版(必修1)——硝酸的强氧化性2020届高三化学二轮冲刺新题专练——硝酸的性质及应用(提升练)贵州省黔南布依族苗族自治州龙里中学2019-2020学年高三上学期期末考试理综化学试题贵州省长顺县二中2019-2020学年高三上学期期末考试理综化学试题贵州省施秉县一中2019-2020学年高三上学期期末考试化学试题(已下线)专题3.5 氮及其化合物 -巅峰冲刺山东省2020年高考化学一轮考点扫描《2020年新高考政策解读与配套资源》福建省福州市第一中学2020年高一在线自测自评质检化学试题贵州省贵阳市第一中学2020届高三教学质量监测理科综合化学试题安徽省池州市第一中学2019-2020学年高一下学期期中教学质量检测化学试题云南省昆明市寻甸县民族中学2019-2020学年高一下学期第一次月考化学试题湖南省长沙市雅礼中学2020届高三5月高考化学模拟试卷安徽省六安市舒城中学2019-2020学年高一下学期第一次月考化学试题(已下线)专题05 元素及其化合物-2020年高考真题和模拟题化学分项汇编(已下线)第12讲 氮及其化合物-2021年高考化学一轮复习名师精讲练2019年上海市高中生化学竞赛初赛试题(“华理一化工杯”)初赛试题鲁科版(2019)高一必修第一册第三章C 高考挑战区 过高考 3年真题强化闯关高一必修第一册(鲁科2019)第3章 第3节 氮的循环 高考帮(已下线)小题必刷20 氮及其化合物——2021年高考化学一轮复习小题必刷(通用版)湖南省长沙市雅礼中学2021届高三上学期第一次月考化学试题北京一零一中2021届高三上学期第三次统练化学试题(已下线)【浙江新东方】48安徽省滁州市定远县重点中学2021届高三上学期11月质量检测化学试题(已下线)【浙江新东方】【2020】【高二上】【期中】【HD-LP406】【化学】陕西省西安市长安区第一中学2019-2020学年高一上学期期末考试化学试题专题7 第一~二单元 综合拔高练-高中化学必修第二册苏教版2019(人教版2019)必修第二册 第五章 化工生产中的重要非金属元素 第二节 氮及其化合物(已下线)【浙江新东方】高中化学20210304-015黑龙江省哈尔滨市阿城区龙涤中学2020-2021学年高一4月月考化学试题黑龙江省哈尔滨市第一六二中学校2020-2021学年高一下学期4月月考化学试题浙江省诸暨市2021届高三5月适应性考试化学试题福建省泉州科技中学2020-2021学年高一下学期期中考试化学试题(苏教版2019)必修第二册专题7 氮与社会可持续发展 C 高考挑战区安徽省芜湖市2020-2021学年高一下学期期末质量检测联考化学试题(已下线)课时23 氮及其化合物-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第12讲 氮及其化合物(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)河南部分学校2022届新高三8月份摸底联考化学试题北京市中国农业大学附属中学2020-2021学年高一上学期期末学业水平调研化学试题(已下线)专题07 常见非金属及其化合物-备战2022年高考化学学霸纠错(全国通用)课后-5.2.3 硝酸 酸雨及防治-人教2019必修第二册云南省瑞丽市第一民族中学2021-2022学年高三下学期3月月考化学试题辽宁省沈阳市第二十中学2019-2020学年高一下学期第一次月考化学试题江西省吉安市2021-2022学年高二下学期期末检测化学试题(已下线)考点11 氮及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第14讲 氮及其化合物(讲)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第13练 氮及其化合物-2023年高考化学一轮复习小题多维练(全国通用)广东省揭阳华侨高级中学2021-2022学年高一下学期第一次阶段化学试题北京市首师附密云中学2021-2022学年高一下学期等级考化学试题山东省菏泽市单县第二中学2021-2022学年高一上学期(实验班)12月段考化学试题第四章 非金属及其化合物 第23讲 硝酸 含氮化合物的转化关系巩固训练12(已下线)题型61 硝酸、硝酸盐的性质安徽省合肥市第一中学2022-2023学年高一下学期第4次月考化学试题(已下线)考点11 氮及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
单选题
|
较难(0.4)
名校
解题方法
11. 下列说法中正确的是
①离子化合物中一定有离子键,可能有共价键
②离子化合物都属于强电解质
③非金属单质中不含离子键,一定只含有共价键
④稳定性:H2O>H2S,沸点:H2O<H2S
⑤NaCl 和 HCl 溶于水破坏相同的作用力
⑥非极性键可能存在于非金属单质中,也可能存在于离子化合物或共价化合物中
①离子化合物中一定有离子键,可能有共价键
②离子化合物都属于强电解质
③非金属单质中不含离子键,一定只含有共价键
④稳定性:H2O>H2S,沸点:H2O<H2S
⑤NaCl 和 HCl 溶于水破坏相同的作用力
⑥非极性键可能存在于非金属单质中,也可能存在于离子化合物或共价化合物中
| A.①②⑥ | B.①③④⑥ | C.③④⑤⑥ | D.①④⑤ |
您最近一年使用:0次
2017-05-17更新
|
2425次组卷
|
4卷引用:四川省彭州市五校2016-2017学年高一下学期期中联考化学试题
单选题
|
较难(0.4)
名校
12. 在一绝热(不与外界发生热交换)的恒容容器中,发生反应:2A(g)+B(s) C(g)+D(g),下列描述中能表明反应已达到平衡状态的有( )个
C(g)+D(g),下列描述中能表明反应已达到平衡状态的有( )个
①容器内温度不变 ②混合气体的密度不变 ③混合气体的压强不变
④混合气体的平均相对分子质量不变 ⑤C(g)的物质的量浓度不变
⑥容器内A、C、D三种气体的浓度之比为2:1:1 ⑦某时刻v(A)=2v(C)且不等于零
⑧单位时间内生成n mol D,同时生成2n mol A
 C(g)+D(g),下列描述中能表明反应已达到平衡状态的有( )个
C(g)+D(g),下列描述中能表明反应已达到平衡状态的有( )个①容器内温度不变 ②混合气体的密度不变 ③混合气体的压强不变
④混合气体的平均相对分子质量不变 ⑤C(g)的物质的量浓度不变
⑥容器内A、C、D三种气体的浓度之比为2:1:1 ⑦某时刻v(A)=2v(C)且不等于零
⑧单位时间内生成n mol D,同时生成2n mol A
| A.4 | B.5 | C.6 | D.7 |
【知识点】 化学平衡状态的判断方法解读
您最近一年使用:0次
2018-05-01更新
|
7446次组卷
|
24卷引用:【全国校级联考】湖北省部分重点中学2017-2018学年高一下学期期中考试化学试题
【全国校级联考】湖北省部分重点中学2017-2018学年高一下学期期中考试化学试题湖南省醴陵市第一中学2017-2018学年高一下学期期末考试化学试题四川省成都市外国语学校2019届高三上学期开学考试化学试题【校级联考】湖北省孝感市六校2018-2019学年高二上学期12月月考化学试题安徽省阜阳市第三中学2018-2019学年高一下学期第二次调研考试化学试题江西省上饶中学2019-2020学年高二上学期第一次月考(理科培优班)化学试题人教版高中化学必修2第二章《化学反应与能量》测试卷3【全国百强校】安徽省六安市第一中学2020届高三下学期自测(二)化学试题(已下线)专题06 化学反应的速率和限度(核心素养卷)-【新教材精创】2019-2020学年高一化学新教材知识讲学(必修第二册)安徽省池州市第一中学2019-2020学年高一下学期期中教学质量检测化学试题甘肃省兰州市第一中学2019-2020学年高一下学期期中考试化学试题内蒙古赤峰二中2019-2020学年高一下学期第二次月考(6月)化学试题河南省南阳市第一中学2019-2020学年高一下学期期末考前模拟化学试题辽宁省锦州市义县高级中学2020-2021学年高一下学期3月考试化学试题湖北省襄阳五中2020-2021学年高二上学期入学考试化学试题辽宁省六校2020-2021学年高一下学期期中联考化学试题云南省通海县一中2020-2021学年高一下学期期中考试化学试题黑龙江省绥化市明水县第一中学2020-2021学年高一下学期第二次月考化学试题宁夏六盘山高级中学2021-2022学年高二上学期期中考试化学试题广东省大联考2021-2022学年高一下学期期中检测化学试题云南省昆明市第三中学2021-2022学年高一下学期期中考试化学试题黑龙江省哈尔滨市第三中学校2022-2023学年高二上学期开学验收考试化学试题山西省太原市山西现代双语学校2021-2022学年高一下学期5月月考化学试题河南省南阳市镇平县第一高级中学2022-2023学年高二下学期5月月考化学试题
单选题
|
较易(0.85)
名校
13. 科学家发现了铝的“超级原子”结构 和
和 。已知这类“超级原子”最外层电子数之和为40时处于相对稳定状态。下列说法正确的是
。已知这类“超级原子”最外层电子数之和为40时处于相对稳定状态。下列说法正确的是
 和
和 。已知这类“超级原子”最外层电子数之和为40时处于相对稳定状态。下列说法正确的是
。已知这类“超级原子”最外层电子数之和为40时处于相对稳定状态。下列说法正确的是A. 和 和 互为同位素 互为同位素 |
B. “超级原子”中 “超级原子”中 原子间通过离子键结合 原子间通过离子键结合 |
C. 和 和 都具有较强的还原性,容易失去电子生成阳离子 都具有较强的还原性,容易失去电子生成阳离子 |
D. 最外层电子数之和为42,与第ⅡA族元素原子的化学性质相似 最外层电子数之和为42,与第ⅡA族元素原子的化学性质相似 |
您最近一年使用:0次
2023-02-13更新
|
227次组卷
|
7卷引用:安徽省无为县2018届高三上学期第一次月考化学试题
单选题
|
适中(0.65)
名校
14. 下列叙述正确的是
| A.两种粒子,若核外电子排布完全相同,则其化学性质一定相同 |
| B.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布 |
| C.两原子,如果核外电子排布相同,则一定属于同种元素 |
| D.阴离子的核外电子排布一定与比它原子序数小的稀有气体元素原子的核外电子排布相同 |
您最近一年使用:0次
2021-08-18更新
|
159次组卷
|
34卷引用:2010-2011学年山西省吕梁市高二下学期期中考试化学试卷
(已下线)2010-2011学年山西省吕梁市高二下学期期中考试化学试卷(已下线)2011-2012学年江苏省泰州中学高二上学期期中考试化学(选修)试卷(已下线)2011-2012学年陕西省师大附中高二下学期期中考试化学试卷(已下线)2014届湖北省武穴中学高三上学期12月月考化学试卷(已下线)2013-2014山西省太原五中高二下学期期中化学(理)试卷2014-2015辽宁实验中学分校高一下学期4月月考化学试卷2015-2016学年湖南省浏阳一中高一下第一次阶段测化学卷2015-2016学年山西省晋城市高平市特立高中高二下期中文科化学试卷2016-2017学年陕西省西安市长安区第一中学高一(平行班)下学期第一次教学检测化学试卷2016-2017学年山东省曲阜师范大学附属中学高一下学期第一次月考化学试卷2016-2017学年陕西省西安市第一中学高一下学期第一次月考化学试卷江西省南昌市八一中学、洪都中学、麻丘中学、十七中、桑海中学2016-2017学年高一下学期期中考试化学试题安徽省铜陵市第一中学2016-2017学年高一下学期期中考试化学试题河北省蠡县中学2016-2017学年高二6月月考化学试题河北省廊坊市第一中学2016-2017学年高二下学期6月月考化学试题黑龙江省牡丹江市第一高级中学2018届高三10月月考化学试题宁夏青铜峡市高级中学2017-2018学年高二上学期期末考试化学试题河南省周口中英文学校2017-2018学年高一下期第一次月考化学试题【全国百强校】黑龙江省哈尔滨市第六中学2019届高三上学期10月月考化学试题广东省湛江市第一中学2017-2018学年高一下学期第一次大考化学试题黑龙江省牡丹江市第一高级中学2020届高三上学期开学检测化学试题上海市上外附中2017-2018学年高二上学期期中考化学试卷云南省普洱市江城县第一中学2019—2020学年高一上学期期末考试化学试题浙江省金华市曙光学校2019-2020学年高一下学期第一次月考化学试题安徽省池州市第一中学2019-2020学年高一下学期期中教学质量检测化学试题河南省新乡市辉县市第二高级中学2019-2020学年高一下学期第一次月考化学试题(B部)(已下线)2.3.2 原子核外电子排布练习(2)——《高中新教材同步备课》(苏教版 必修第一册)(已下线)鲁科版高中化学必修2第一章《原子结构与元素周期律》章节测试卷江西省上饶市横峰中学2020-2021学年高一下学期第一次月考(统招班)化学试题(已下线)课时25 原子结构-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第13讲 原子结构 化学键(练) — 2022年高考化学一轮复习讲练测(新教材新高考)江苏省淮安市涟水县第一中学2021-2022学年高二下学期第二次阶段检测化学试题(已下线)第五章 物质结构与性质元素周期律 第26练 原子结构 核外电子排布原理福建省建瓯市芝华中学2023-2024学年高一下学期第一次阶段考试化学试题
单选题
|
适中(0.65)
名校
15. W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,且四种元素的最外层电子数之和为24。下列说法错误的是
| W | X | |
| Y | Z |
| A.单核阴离子的还原性Y强于X |
| B.W的简单气态氢化物与其最高价含氧酸反应生成离子化合物 |
| C.X、Y、Z最简单氢化物中稳定性最弱的是Y |
| D.在元素周期表中118号元素与Z位于同一主族 |
您最近一年使用:0次
2021-09-29更新
|
863次组卷
|
17卷引用:【全国市级联考】山东省潍坊市2018届高三第三次高考模拟考试理综化学试题
【全国市级联考】山东省潍坊市2018届高三第三次高考模拟考试理综化学试题(已下线)2018年高考题及模拟题汇编 专题06 物质结构 元素周期律四川省泸县第二中学2019届高三下学期三诊模拟理科综合化学试题2020届人教版高三化学二轮复习选择题专攻练——物质结构 元素周期律四川省宜宾市南溪一中2018-2019学年高一下学期期中化学试题安徽省池州市第一中学2019-2020学年高一下学期期中教学质量检测化学试题(已下线)【全国百强校】贵州省思南中学2018-2019学年2018-2019学年高一下学期期中考试化学试题(已下线)专题讲座(五) “位-构-性”综合推断题的解题方法(精讲)——2021年高考化学一轮复习讲练测江西省抚州市部分中学联合体2020-2021学年高一下学期第一次月考化学试题山东省实验中学2020~2021学年高一下学期期中考试化学试题四川省南充市2020-2021学年高一下学期期末联考化学试题(已下线)专题讲座(三)“位-构-性”综合推断题的解题方法(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)四川省成都市大弯中学校2022届高三9月月考化学试题四川省邻水实验学校2021-2022学年高一下学期第6月月考化学试题云南省楚雄天人中学2021-2022学年高一6月月考化学试题山东烟台2022-2023学年高一下学期3月月考化学试题山东省滨州市博兴第二中学2022-2023学年高一下学期第二次月考化学试题
单选题
|
适中(0.65)
名校
解题方法
16. 我国首艘使用了钛合金材料的国产航母已成功下水,钛(Ti)常温下与酸、碱均不反应,但高温下能被空气氧化,由钛铁矿(主要成分是FeO和TiO2)提取金属钛的主要工艺流程如图。下列说法错误的是
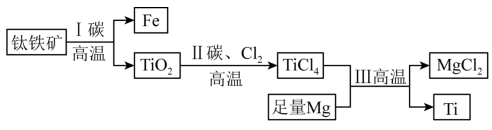

| A.步骤Ⅰ中碳作还原剂 |
| B.步骤Ⅱ中未发生氧化还原反应 |
| C.步骤Ⅲ中需在氩气环境中进行,防止金属被空气氧化 |
| D.可用稀硫酸除去金属钛中的少量镁 |
您最近一年使用:0次
2020-06-10更新
|
1178次组卷
|
11卷引用:四川省成都市2017-2018学年高一上期期末调研考试化学试题
四川省成都市2017-2018学年高一上期期末调研考试化学试题2018-2019学年高一化学《金属及其化合物》单元训练题湖南省邵东县第一中学2019-2020学年高一上学期第三次月考化学试题安徽省池州市第一中学2019-2020学年高一下学期期中教学质量检测化学试题(已下线)第三单元 金属及其化合物测试题-2021年高考化学一轮复习名师精讲练苏教版(2020)高一必修第一册 综合训练重庆市第一中学2019-2020学年高一上学期10月月考化学试题鲁科版(2019)高一必修第一册 综合训练(一)(已下线)小题必刷13 镁及其化合物——2021年高考化学一轮复习小题必刷(通用版)吉林省白城市洮南市第一中学2020-2021学年高一上学期第一次月考化学试题(已下线)易错21 化学工艺流程类选择题-备战2021年高考化学一轮复习易错题
单选题
|
适中(0.65)
名校
解题方法
17. 世界某著名学术刊物介绍了一种新型中温全瓷铁-空气电池,其结构如图所示。下列有关该电池放电时的说法正确的是


| A.a极发生氧化反应 |
| B.正极的电极反应式为FeOx+2xe-=Fe+xO2- |
| C.若有22.4L(标准状况)空气参与反应,则电路中有4mol电子转移 |
| D.铁表面发生的反应为xH2O(g)+Fe=FeOx+xH2 |
【知识点】 电化学计算 原电池电极反应式书写解读
您最近一年使用:0次
2021-03-12更新
|
980次组卷
|
19卷引用:考点09 原电池及化学电源——《备战2020年高考精选考点专项突破题集》
(已下线)考点09 原电池及化学电源——《备战2020年高考精选考点专项突破题集》2020届高三化学知识点强化训练----化学能与电能2020届高三化学化学二轮复习——高考常考题型:新型电池【夯基提能】【精编30题】安徽省阜阳市2019-2020学年高一下学期开学考化学试题安徽省池州市第一中学2019-2020学年高一下学期期中教学质量检测化学试题黑龙江大庆实验中学2019-2020学年高一下学期6月月考(期中)化学试题广东省广雅、执信、六中、深外四校2020届高三上学期8月开学联考理综化学试题甘肃省兰州市第一中学2019-2020学年高一下学期期末考试化学试题湖南省长沙市第一中学2021届高三上学期第二次月考化学试题(已下线)专题讲座(六)新型电源及电极反应式的书写(精练)-2021年高考化学一轮复习讲练测(已下线)【浙江新东方】高中化学20210304-004辽宁省实验中学东戴河分校两校2020-2021学年高一4月联考化学试题江西省兴国县第三中学2020-2021学年高一下学期第三次月考化学(兴特班)试题选择性必修1(SJ)专题1第二单元课时2 化学电源(已下线)单科化学-2021年秋季高三开学摸底考试卷01(课标全国专用)(已下线)专题06 电化学原理应用—2022年高考化学二轮复习讲练测(全国版)-讲义广西柳城县中学2021-2022学年高三上学期10月月考化学试卷(已下线)题型16 金属-空气电池的应用(已下线)热点题型训练 新型化学电源及其应用
单选题
|
适中(0.65)
名校
解题方法
18. 下列叙述正确的是
| A.SiO2既能和NaOH溶液反应,又能和HF反应,所以SiO2属于两性氧化物 |
B.因为Na2CO3+SiO2 Na2SiO3+CO2↑,所以H2SiO3的酸性比H2CO3强 Na2SiO3+CO2↑,所以H2SiO3的酸性比H2CO3强 |
| C.CO2和SiO2都能与C反应 |
| D.CO2和SiO2都是酸性氧化物,所以两者物理性质相似 |
您最近一年使用:0次
2020-06-10更新
|
154次组卷
|
2卷引用:安徽省池州市第一中学2019-2020学年高一下学期期中教学质量检测化学试题
二、计算题 添加题型下试题
计算题
|
适中(0.65)
名校
解题方法
19. 把0.6molW气体和0.5molX气体混合于2L密闭容器中,使它们发生如下反应:4W(g)+3X(g) 2Y(g)+nZ(g)。2min末已生成0.2molY,若测知以Z的浓度变化表示的反应速率为0.0025mol/(L·s),试计算
2Y(g)+nZ(g)。2min末已生成0.2molY,若测知以Z的浓度变化表示的反应速率为0.0025mol/(L·s),试计算
(1)前2min内用W的浓度变化表示的平均反应速率为______ 。
(2)2min末时X的浓度为__________ 。
(3)化学反应方程式中n=________ 。
(4)2min末,恢复到反应前温度,体系内压强是反应前压强的___ 倍。
 2Y(g)+nZ(g)。2min末已生成0.2molY,若测知以Z的浓度变化表示的反应速率为0.0025mol/(L·s),试计算
2Y(g)+nZ(g)。2min末已生成0.2molY,若测知以Z的浓度变化表示的反应速率为0.0025mol/(L·s),试计算(1)前2min内用W的浓度变化表示的平均反应速率为
(2)2min末时X的浓度为
(3)化学反应方程式中n=
(4)2min末,恢复到反应前温度,体系内压强是反应前压强的
您最近一年使用:0次
2018-05-01更新
|
761次组卷
|
4卷引用:【全国校级联考】湖北省部分重点中学2017-2018学年高一下学期期中考试化学试题
三、填空题 添加题型下试题
填空题
|
适中(0.65)
名校
解题方法
20. 正确认识和使用电池有利于我们每一个人的日常生活。电化学处理SO2是目前研究的热点,利用双氧水氧化吸收SO2是目前研究的热点。
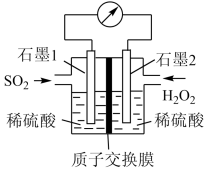
(1)反应的总化学方程式为___ ,正极的电极反应式为___ 。
(2)H+的迁移方向为由___ 到___ (填“左”或“右”)。
(3)若11.2L(标准状况)SO2参与反应,则迁移H+的物质的量为___ 。
(4)下列化学电池不易造成环境污染的是___ (填字母)。
A.氢氧燃料电池 B.锌锰电池 C.镍镉电池 D.铅蓄电池
(5)某同学关于原电池的笔记中,不合理的有___ (填序号)。
①原电池两电极活泼性一定不同
②原电池负极材料参与反应,正极材料都不参与反应
③Fe-NaOH溶液-Si原电池,Fe是负极

(1)反应的总化学方程式为
(2)H+的迁移方向为由
(3)若11.2L(标准状况)SO2参与反应,则迁移H+的物质的量为
(4)下列化学电池不易造成环境污染的是
A.氢氧燃料电池 B.锌锰电池 C.镍镉电池 D.铅蓄电池
(5)某同学关于原电池的笔记中,不合理的有
①原电池两电极活泼性一定不同
②原电池负极材料参与反应,正极材料都不参与反应
③Fe-NaOH溶液-Si原电池,Fe是负极
您最近一年使用:0次
四、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
名校
解题方法
21. 硫代硫酸钠(Na2S2O3)是一种重要的化工产品。某研究小组制备硫代硫酸钠晶体(Na2S2O3·5H2O)的实验装置如图所示(省略夹持装置):
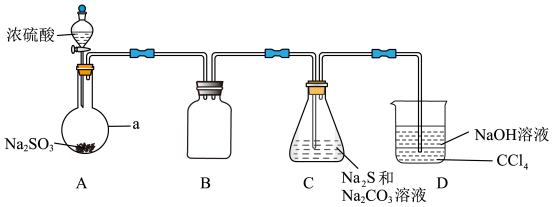
【查阅资料】
Ⅰ.Na2S2O3·5H2O是无色晶体,易溶于水,其稀溶液与BaCl2溶液混合无沉淀生成;
Ⅱ.向Na2CO3和Na2S混合液中通入SO2可制得Na2S2O3。
根据题意,填写下列空白。
(1)仪器a的名称是___ ;B的作用是___ 。
(2)C中反应氧化剂与还原剂的物质的量之比为___ 。
(3)该实验制取的产品中常含有少量Na2SO3和Na2SO4杂质。为了检验产品中是否含有这两种杂质,某小组设计了以下实验方案(所需试剂从稀硝酸、稀硫酸、稀盐酸、蒸馏水中选择),请将方案补充完整。
取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,过滤、洗涤后,向沉淀中滴加足量的___ (填试剂名称),若___ (填实验现象),则可以确定产品中含有Na2SO3和Na2SO4。
(4)称取样品137.5g配成500mL溶液。取50mL溶液,向其中加入足量稀硫酸,充分反应(S2O +2H+=S↓+SO2↑+H2O),静置、过滤、洗涤、干燥、称量得沉淀1.6g。
+2H+=S↓+SO2↑+H2O),静置、过滤、洗涤、干燥、称量得沉淀1.6g。
准确配制500mL溶液所需仪器有:天平、药匙、烧杯、玻璃棒、___ 、___ 。经计算,样品中硫代硫酸晶体的百分含量为___ 。(保留三位有效数字)

【查阅资料】
Ⅰ.Na2S2O3·5H2O是无色晶体,易溶于水,其稀溶液与BaCl2溶液混合无沉淀生成;
Ⅱ.向Na2CO3和Na2S混合液中通入SO2可制得Na2S2O3。
根据题意,填写下列空白。
(1)仪器a的名称是
(2)C中反应氧化剂与还原剂的物质的量之比为
(3)该实验制取的产品中常含有少量Na2SO3和Na2SO4杂质。为了检验产品中是否含有这两种杂质,某小组设计了以下实验方案(所需试剂从稀硝酸、稀硫酸、稀盐酸、蒸馏水中选择),请将方案补充完整。
取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,过滤、洗涤后,向沉淀中滴加足量的
(4)称取样品137.5g配成500mL溶液。取50mL溶液,向其中加入足量稀硫酸,充分反应(S2O
 +2H+=S↓+SO2↑+H2O),静置、过滤、洗涤、干燥、称量得沉淀1.6g。
+2H+=S↓+SO2↑+H2O),静置、过滤、洗涤、干燥、称量得沉淀1.6g。准确配制500mL溶液所需仪器有:天平、药匙、烧杯、玻璃棒、
您最近一年使用:0次
解答题-无机推断题
|
适中(0.65)
名校
解题方法
22. 短周期五种元素A、B、C、D、E的原子序数依次增大。A、B、C的单质在常温下都呈气态,C原子最外层电子数是电子层数的3倍,C和E位于同主族。1molDAx与足量的A2C反应生成44.8L(标准状况)G气体。A、B的单质依次为G、T,在密闭容器中充入一定量的G、T,一定条件下发生反应G+T W(未配平),测得各物质的浓度如表所示。
W(未配平),测得各物质的浓度如表所示。
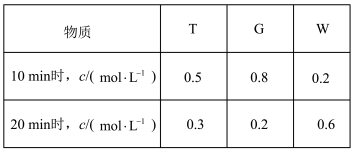
回答下列问题:
(1)A、B、C能组成既含离子键又含共价键的化合物,则该化合物的化学式为___ 。
(2)B、C、D、E的简单离子中,离子半径大小排序为___ 。(用具体的离子表示)
(3)J、L是由A、B、C、E四种元素组成的两种化合物,J、L溶液混合可产生有刺激性气味的气体,写出这两种溶液发生反应的离子方程式:___ ;J、L中能使酸性高锰酸钾溶液褪色的是___ (填化学式)。
(4)B2A4—C2碱性燃料电池放电效率高。该电池放电时,负极反应式为___ ;正极附近溶液的pH___ (填“增大”“减小”或“不变”)。
(5)由上述五种元素中的四种组成的单质、化合物在一定条件下的转化关系(部分条件和产物已省略)如图所示:

①Y是___ (填化学式);W的电子式为___ 。
②B的最高价氧化物对应的水化物为Q,X与足量的Q溶液反应的化学方程式为___ 。
③1molW与足量乙完全反应生成K和甲,转移的电子数约为___ 。
 W(未配平),测得各物质的浓度如表所示。
W(未配平),测得各物质的浓度如表所示。
回答下列问题:
(1)A、B、C能组成既含离子键又含共价键的化合物,则该化合物的化学式为
(2)B、C、D、E的简单离子中,离子半径大小排序为
(3)J、L是由A、B、C、E四种元素组成的两种化合物,J、L溶液混合可产生有刺激性气味的气体,写出这两种溶液发生反应的离子方程式:
(4)B2A4—C2碱性燃料电池放电效率高。该电池放电时,负极反应式为
(5)由上述五种元素中的四种组成的单质、化合物在一定条件下的转化关系(部分条件和产物已省略)如图所示:

①Y是
②B的最高价氧化物对应的水化物为Q,X与足量的Q溶液反应的化学方程式为
③1molW与足量乙完全反应生成K和甲,转移的电子数约为
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:化学反应原理、物质结构与性质、认识化学科学、常见无机物及其应用、化学实验基础
试卷题型(共 22题)
题型
数量
单选题
18
计算题
1
填空题
1
解答题
2
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 吸热反应和放热反应 共价键概念及判断 | |
| 2 | 0.94 | 共价化合物的结构及形成过程 电子式的书写与判断 离子键概念及判断 | |
| 3 | 0.65 | 化学反应中能量变化的原因 | |
| 4 | 0.94 | 物质的转化 碳酸钠与碳酸氢钠的相互转化 铝三角转化 与“铁三角”有关的推断 | |
| 5 | 0.65 | 影响化学反应速率的因素 浓度对化学反应速率的影响 温度对化学反应速率的影响 | |
| 6 | 0.65 | 元素周期律、元素周期表的推断 | |
| 7 | 0.65 | 原电池原理理解 原电池正负极判断 原电池电极反应式书写 原电池原理的综合应用 | |
| 8 | 0.65 | 根据物质性质进行元素种类推断 “位构性”关系理解及应用 | |
| 9 | 0.85 | 铁与非金属单质反应 铁与非氧化性酸的反应 铁与铁离子反应 Fe2+的还原性 | |
| 10 | 0.65 | 硝酸的不稳定性 化学实验方案的设计与评价 物质性质的探究 | |
| 11 | 0.4 | 共价键与离子键的比较 化学键与物质类别关系的判断 共价键对分子构型、性质的影响 氢键对物质性质的影响 | |
| 12 | 0.4 | 化学平衡状态的判断方法 | |
| 13 | 0.85 | 元素周期律的应用 元素、核素、同位素 化学键与物质类别关系的判断 | |
| 14 | 0.65 | 原子中相关数值及其之间的相互关系 元素、核素、同位素 基态核外电子排布规律 | |
| 15 | 0.65 | 元素周期律、元素周期表的推断 元素非金属性强弱的比较方法 | |
| 16 | 0.65 | 氧化还原反应基本概念 镁原子的结构与化学性质 几种铁的氧化物的化学性质 物质制备的探究 | |
| 17 | 0.65 | 电化学计算 原电池电极反应式书写 | |
| 18 | 0.65 | 二氧化硅的化学性质 二氧化硅与二氧化碳结构与性质的比较 | |
| 二、计算题 | |||
| 19 | 0.65 | 化学反应速率计算 化学反应速率与化学计量数之间的关系 | |
| 三、填空题 | |||
| 20 | 0.65 | 原电池正负极判断 原电池电极反应式书写 电极材料的特殊性质对原电池正负极判断的影响 原电池有关计算 | |
| 四、解答题 | |||
| 21 | 0.65 | 二氧化硫的制备 硫酸根离子的检验 物质含量的测定 物质制备的探究 | 实验探究题 |
| 22 | 0.65 | 原电池电极反应式书写 元素周期律、元素周期表的推断 结合物质计算的元素周期律、元素周期表相关推断 | 无机推断题 |



