河南省鹤壁市淇县第一中学2018-2019学年高一上学期第三次月考化学试题
河南
高一
阶段练习
2018-12-31
454次
整体难度:
适中
考查范围:
化学实验基础、认识化学科学、化学与STSE、常见无机物及其应用
一、单选题 添加题型下试题
| A.标准状况下,22.4 L氦气中含有的电子数为2NA |
| B.7.8 g Na2O2与足量水反应转移电子数为0.2NA |
| C.100 g 98%的浓硫酸中,氧原子总数为4NA |
| D.0.2NA的Al与足量的NaOH溶液反应产生H2的体积为6.72 L |
 有BaCl2和KCl的混合溶液分成5等份,取一份加入含
有BaCl2和KCl的混合溶液分成5等份,取一份加入含
 硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含
硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含
 硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子浓度为
硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子浓度为A.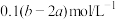 | B. |
C.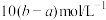 | D.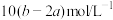 |
【知识点】 物质的量浓度计算-与溶质成分有关的计算解读
| A.“血液透析”和“静电除尘”利用了胶体的不同性质 |
| B.把石灰浆喷涂在树干上可消灭树皮上的过冬虫卵 |
| C.酸性重铬酸钾用于检查酒驾是利用其强还原性 |
| D.在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化 |
【知识点】 化学科学对人类文明发展的意义解读
| A.钠和水反应Na+H2O=Na++OH-+H2↑ |
| B.碳酸钙与稀盐酸反应:2H++CO32- = CO2↑+H2O |
| C.NaHCO3溶液与少量Ca(OH) 2溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O |
| D.碳酸氢钠溶液中加入醋酸:HCO3-+ CH3COOH = CH3COO- + H2O + CO2↑ |
| A.Na+、H+、SO42-、HCO3- | B.Cu2+、K+、SO42-、NO3- |
| C.Fe3+、K+、I-、Cl- | D.Fe3+、K+、SO42-、SCN- |
【知识点】 离子共存 限定条件下的离子共存解读 铁盐
| A.Na+、Mg2+、SO42-、Cl﹣ | B.K+、Na+、Cl﹣、SiO32- |
| C.K+、NH4+、Cl﹣、SO42- | D.Na+、K+、HCO3-、Cl﹣ |
【知识点】 限定条件下的离子共存解读
| A.Ca2+、K+、OH−、Cl−、NO3− | B.Fe2+、H+、Br−、NO3−、Cl− |
| C.Na+、K+、SO42−、NO3−、Cl− | D.Al3+、Na+、Cl−、SO42−、NO3− |
【知识点】 限定条件下的离子共存解读
①2BrO3-+Cl2→Br2+2 C1O3- ②C1O3-+5Cl-+6H+→3Cl2+3H2O
③2FeCl3+2KI→2FeCl2+2KCl+I2 ④2FeCl2+Cl2→2FeCl3
下列叙述正确的是
| A.氧化能力: C1O3->BrO3->Cl2>Fe3+>I2 |
| B.还原能力Fe2+>I->Cl- |
| C.反应C1O3-+Br- →-Cl-+BrO3-能顺利进行 |
| D.氧化能力:BrO3- >ClO3->Cl2>Fe3+>I2 |
| A.切开的金属Na暴露在空气中,光亮表面逐渐变暗:2Na+O2═Na2O2 |
| B.钠与盐酸反应的离子方程式:2Na+2H+═2Na++H2↑ |
| C.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 |
| D.Na的金属活动性比Mg强,故可用Na与MgCl2溶液反应制Mg |
| A.HCl | B.H2SO4 | C.H2O | D.饱和NaOH溶液 |
【知识点】 化学方程式计算中物质的量的运用解读 钠与水反应原理解读
①Ca(OH)2 ②盐酸③CaCl2 ④NaOH ⑤加热
| A.②③ | B.①④ | C.①③ | D.②⑤ |
①先加氯水,后加KSCN溶液后显红色 ②先加KSCN溶液,不显红色,再加氯水后显红色 ③滴加NaOH溶液,先产生白色沉淀,迅速变为灰绿色,最后呈红褐色 ④只滴加KSCN溶液
| A.①② | B.②③ | C.③④ | D.①④ |
【知识点】 Fe2+的鉴别及其应用解读 常见阳离子的检验解读
| A.2.48g | B.2.58g | C.4.16g | D.4.41g |
| A.NaHSO4和Ba(OH)2 |
| B.AlCl3和NaOH |
| C.NaAlO2和H2SO4 |
| D.Na2CO3和H2SO4 |
| A.1:1:1 | B.1:1:2 |
| C.1:2:1 | D.4:3:2 |
【知识点】 化学方程式计算中物质的量的运用解读 钠 氧化钠 过氧化钠
| A.1:2:3:2 | B.6:3:2:3 | C.1:1:1:1 | D.2:1:1:1 |
【知识点】 铁
| A.Al→Al2O3→Al(OH)3→AlCl3 | B.Na→NaOH→Na2CO3→NaCl |
| C.Mg→MgCl2→Mg(OH)2→MgSO4 | D.Fe→FeCl2→Fe(OH)2→Fe(OH)3 |
二、填空题 添加题型下试题
A. Cl2 B. S2— C. H+ D. Na E. FeCl2
(2)在4HCl(浓)+MnO2
 MnCl2+Cl2↑+2H2O反应中
MnCl2+Cl2↑+2H2O反应中①氧化剂是
②
(1)写出用小苏打治疗胃酸过多的离子方程式:
(2)如果病人同时患胃溃疡,为了防止引起胃壁穿孔,不能服用小苏打,其原因是:
此时最好服用胃舒平,胃舒平的主要成分是Al(OH)3,也能用于治疗胃酸过多。反应的离子方程式为:
三、计算题 添加题型下试题

试计算:
(1)合金中Al的质量
(2)NaOH溶液的物质的量浓度
【知识点】 氢氧化铝与强碱反应解读 探究物质组成或测量物质的含量解读
试卷分析
试卷题型(共 23题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
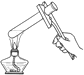
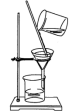
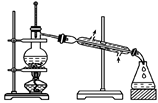
| 1 | 0.65 | 物质分离、提纯的常见物理方法 蒸馏与分馏 萃取和分液 过滤 | |
| 2 | 0.65 | 阿伏加德罗常数的求算 结合气体物质与NA相关推算 结合氧化还原反应知识与NA相关推算 | |
| 3 | 0.65 | 物质的量浓度计算-与溶质成分有关的计算 | |
| 4 | 0.85 | 化学科学对人类文明发展的意义 | |
| 5 | 0.65 | 离子反应的发生条件 离子方程式的书写 离子方程式的正误判断 | |
| 6 | 0.65 | 离子共存 限定条件下的离子共存 铁盐 | |
| 7 | 0.85 | 限定条件下的离子共存 | |
| 8 | 0.65 | 限定条件下的离子共存 | |
| 9 | 0.65 | 氧化还原反应的几组概念 氧化还原反应定义、本质及特征 氧化性、还原性强弱的比较 氧化还原反应的规律 | |
| 10 | 0.85 | 镁的结构与化学性质 铝与强碱溶液反应 物质分离、提纯综合应用 | |
| 11 | 0.65 | 钠 钠的化学性质 | |
| 12 | 0.85 | 化学方程式计算中物质的量的运用 钠与水反应原理 | |
| 13 | 0.85 | 碳酸钠与碳酸氢钠鉴别的实验 物质的检验 物质检验和鉴别的基本方法选择及应用 物质检验和鉴别的实验方案设计 | |
| 14 | 0.65 | Fe2+的鉴别及其应用 常见阳离子的检验 | |
| 15 | 0.65 | 碳酸钠、碳酸氢钠混合物的有关求算 探究物质组成或测量物质的含量 | |
| 16 | 0.4 | 碳酸钠与盐酸的反应 铝盐与强碱溶液反应 偏铝酸钠与盐酸的反应 | |
| 17 | 0.65 | 化学方程式计算中物质的量的运用 钠 氧化钠 过氧化钠 | |
| 18 | 0.65 | 铁 | |
| 19 | 0.85 | 钠与氧气等非金属的反应 镁 铝 铁 | |
| 20 | 0.94 | 物质的转化 碳酸钠与碳酸氢钠的相互转化 铝三角转化 与“铁三角”有关的推断 | |
| 二、填空题 | |||
| 21 | 0.85 | 氧化还原反应的应用 氧化还原反应的规律 | |
| 22 | 0.65 | 碳酸氢钠与酸反应 氢氧化铝与强酸反应 药物的合理使用 | |
| 三、计算题 | |||
| 23 | 0.65 | 氢氧化铝与强碱反应 探究物质组成或测量物质的含量 | |