河南省驻马店市上蔡县第二高级中学2018-2019学年高一上学期期中考试化学试题
河南
高一
期中
2019-01-10
393次
整体难度:
适中
考查范围:
化学实验基础、认识化学科学、常见无机物及其应用、化学反应原理
一、单选题 添加题型下试题
| A.不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 |
| B.燃着的酒精灯不慎翻倒,灯内酒精流出并着火,可用湿抹布覆盖 |
| C.不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硫酸 |
| D.配制硫酸溶液时,可先在烧杯中加入一定体积的水,再在搅拌条件下慢慢加入浓硫酸 |
| A.焰色试验是化学变化 | B.用稀盐酸清洗做焰色试验的铂丝 |
| C.焰色试验均应透过蓝色钴玻璃观察 | D.利用焰色试验可区分NaCl与Na2CO3固体 |
| A.+2 | B.0 | C.+4 | D.+6 |
【知识点】 氧化还原反应有关计算
| A.23 g Na与足量H2O反应完全后可生成NA个H2分子 |
| B.1 mol Na2O2和足量CO2反应转移2NA个电子 |
| C.27g铝与足量氢氧化钠溶液反应失去3NA个电子 |
| D.3 mol单质Fe与足量盐酸反应,失去9NA个电子 |
【知识点】 阿伏加德罗常数的求算解读
| A.Al→Al2O3→Al(OH)3→AlCl3 | B.Na→NaOH→Na2CO3→NaCl |
| C.Mg→MgCl2→Mg(OH)2→MgSO4 | D.Fe→FeCl2→Fe(OH)2→Fe(OH)3 |
| A.氢氧化钡溶液和稀硫酸反应Ba2++OH—+H++SO42—=BaSO4↓+H2O |
| B.钠与水反应Na+2H2O=Na++2OH—+H2↑ |
| C.金属铝溶于氢氧化钠溶液Al+2OH-=AlO2-+H2↑ |
| D.碳酸氢钠与醋酸反应HCO3—+CH3COOH=CH3COO—+CO2↑+H2O |
【知识点】 离子反应的发生及书写 离子方程式的书写解读 离子方程式的正误判断解读
①MgSO4溶液 ②NaCl溶液 ③Na2SO4溶液 ④Ca(HCO3)2溶液⑤Al2(SO4)3溶液 ⑥CuSO4溶液
| A.①②④⑤ | B.③④⑤⑥ | C.①④⑤⑥ | D.②④⑤⑥ |
| A.用量筒量取所需的浓硫酸时俯视读数 |
| B.定容后摇匀,发现液面最低点低于刻度线 |
| C.定容时,俯视刻度线 |
| D.用量筒量取浓硫酸倒入烧杯,用蒸馏水洗量筒2~3次,洗液倒入烧杯中 |
【知识点】 配制一定物质的量浓度的溶液实验的误差分析解读
 5NaBr+NaBrO3+3H2O的反应,下列说法中不正确的是
5NaBr+NaBrO3+3H2O的反应,下列说法中不正确的是| A.Br 2既是氧化剂,又是还原剂 |
| B.被氧化的溴原子与被还原的溴原子质量比是1:5 |
| C.NaBr是氧化产物,NaBrO3是还原产物 |
| D.转移1mol电子时,消耗NaOH 1.2mol |
【知识点】 氧化还原反应基本概念 氧化还原反应有关计算 氧化还原反应的规律解读
| A.2.0mol/L | B.1.5 mol/L | C.0.18 mol/L | D.0.64mol/L |
 Fe2O3+3Cu。铜在氯化铁溶液中发生反应:Cu+2FeCl3=2FeCl2+CuCl2,一定质量的铁与氧化铜的混合物,在高温条件下恰好完全反应.将反应后的固体粉末倒入盛有足量稀盐酸的烧杯中,振荡,充分反应后静置,然后从烧杯中取适量溶液(表示为“甲”)于试管中,并加入一定质量的锌粉,充分反应后过滤,得到滤液乙和固体丙。下列判断正确的是
Fe2O3+3Cu。铜在氯化铁溶液中发生反应:Cu+2FeCl3=2FeCl2+CuCl2,一定质量的铁与氧化铜的混合物,在高温条件下恰好完全反应.将反应后的固体粉末倒入盛有足量稀盐酸的烧杯中,振荡,充分反应后静置,然后从烧杯中取适量溶液(表示为“甲”)于试管中,并加入一定质量的锌粉,充分反应后过滤,得到滤液乙和固体丙。下列判断正确的是①甲中含有FeCl3;②甲中不含FeCl3;③若向固体丙加稀盐酸无明显现象,则滤液乙中一定含有ZnCl2、FeCl2,可能含有CuCl2;④若向固体丙加稀盐酸有气体产生,则滤液乙中可能含有ZnCl2、FeCl2,一定不含有CuCl2。
| A.①③ | B.②③ | C.①④ | D.②④ |
【知识点】 常见金属的活动性顺序及其应用解读 铁 铁盐 铜
| A.胶体一定是混合物 |
| B.胶体与溶液的本质区别是有丁达尔效应 |
| C.将饱和氯化铁溶液滴入稀氢氧化钠溶液中加热,可得氢氧化铁胶体 |
| D.胶体能通过半透膜 |
【知识点】 分散系
①氢氧化铝加热能分解为金属氧化物和水;氢氧化镁、氢氧化铁也能加热分解生成金属氧化物和水 ②Fe露置在潮湿空气中一段时间后就会锈迹斑斑;性质更活泼的Al不能稳定存在于空气中 ③碳酸钠、碳酸氢钠溶液均显碱性;钠盐溶液均能使酚酞变红 ④钠和硫反应生成Na2S;镁、铝、铁均能与硫直接化合生成相应的硫化物 ⑤化合物NaCl的焰色为黄色;Na2CO3的焰色也为黄色 ⑥钠与水反应生成NaOH和H2;所有金属与水反应都生成对应碱和H2
| A.①④⑤ | B.①③⑥ | C.②③⑥ | D.①②③ |
| A.Cl— | B.Fe3+ | C.OH— | D.Na+ |

| A.OA段发生反应的离子方程式为:H++OH-=H2O、CO32-+H+=HCO3- |
| B.A点溶液中的溶质为NaCl、NaHCO3 |
| C.当加入45 mL盐酸时,产生CO2的体积为336mL |
| D.混合物中NaOH的质量0.20 g |
二、填空题 添加题型下试题

(1)写出下列物质的名称:B
(2)写出E→F的离子方程式
F(固体)→E的化学方程式
(3)写出C与二氧化碳反应的化学方程式为:
【知识点】 无机综合推断
三、解答题 添加题型下试题
84消毒液:【有效成分】NaClO;【规格】1000ml;【质量分数】25%;【密度】1.19g/cm3。
(1)该“84消毒液”的物质的量浓度约为
(2)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制240mL含NaClO质量分数为25%的消毒液,需要称量NaClO固体的质量为
(3)下列操作会使所配浓度偏高、偏低或无影响。
A.定容时仰视容量瓶刻度线
(4)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84g·cm−3)的浓硫酸配制1000mL2.3mol·L−1的稀硫酸用于增强“84消毒液”的消毒能力。需用浓硫酸的体积为
四、填空题 添加题型下试题
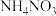

 ①
①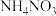

 ②
②

 ③
③

 ④
④请回答下列问题
(1)若反应②生成标准状况下的33.6LN2O,则转移电子数为
(2)反应③中物质X的化学式是
(3)反应④中氧化产物是
II.某同学写出以下三个化学方程式(未配平):
①NO+HNO2→N2O3+H2O ②NH3+NO→HNO2+H2O
③N2O4+H2O→HNO3+HNO2 其中你认为有可能实现的是
III.下列三个氧化还原反应中,氧化剂氧化性由强到弱的顺序是
①2FeCl3+2KI=2FeCl2+2KCl+I2
②2FeCl2+Cl2=2FeCl3
③2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
五、解答题 添加题型下试题

请回答下列有关问题:
(1)下列有关铝矾石以及用铝矾石炼铝的说法中,正确的是
A.铝矾石中含有两种类型氧化物
B.铝矾石与河沙含有完全相同的成分
C.铝矾石炼铝需要消耗电能
D.铝矾石炼铝的过程中涉及置换反应
(2)加入原料A时发生反应的离子方程式有
(3)滤液Ⅱ中所含溶质有
(4)若步骤③中用氨气代替CO2,步骤③生成沉淀的离子方程式为
六、计算题 添加题型下试题
(1)钠铝合金中两金属的物质的量
(2)所得溶液的物质的量浓度
【知识点】 物质的量有关计算 物质的量浓度的计算 化学方程式计算中物质的量的运用解读 钠
试卷分析
试卷题型(共 21题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 常用仪器及使用 化学实验基础操作 实验安全 | |
| 2 | 0.65 | 物理变化与化学变化 焰色试验 钠的物理性质 化学实验基础操作 | |
| 3 | 0.85 | 氧化还原反应有关计算 | |
| 4 | 0.85 | 阿伏加德罗常数的求算 | |
| 5 | 0.94 | 物质的转化 碳酸钠与碳酸氢钠的相互转化 铝三角转化 与“铁三角”有关的推断 | |
| 6 | 0.85 | 离子反应的发生及书写 离子方程式的书写 离子方程式的正误判断 | |
| 7 | 0.85 | 物质分离、提纯的常见物理方法 | |
| 8 | 0.85 | 钠与盐溶液的反应 | |
| 9 | 0.85 | 配制一定物质的量浓度的溶液实验的误差分析 | |
| 10 | 0.85 | 氧化还原反应基本概念 氧化还原反应有关计算 氧化还原反应的规律 | |
| 11 | 0.85 | 物质的量浓度的计算 氢氧化钠、碳酸钠混合溶液与盐酸反应相关考查 | |
| 12 | 0.65 | 常见金属的活动性顺序及其应用 铁 铁盐 铜 | |
| 13 | 0.64 | 分散系 | |
| 14 | 0.65 | 钠 镁 铝 铁 | |
| 15 | 0.85 | 离子共存 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 | |
| 16 | 0.85 | 物质的量有关计算 氢氧化钠、碳酸钠混合溶液与盐酸反应相关考查 | |
| 二、填空题 | |||
| 17 | 0.85 | 无机综合推断 | |
| 19 | 0.65 | 氧化还原反应基本概念 氧化性、还原性强弱的比较 氧化还原反应有关计算 氧化还原反应的规律 | |
| 三、解答题 | |||
| 18 | 0.85 | 物质的量浓度的计算 配制一定物质的量浓度的溶液的步骤、操作 配制一定物质的量浓度的溶液实验的误差分析 配制一定物质的量浓度的溶液实验的仪器 | 实验探究题 |
| 20 | 0.65 | 含氧化铝的混合物的提纯 偏铝酸钠与二氧化碳的反应 物质分离、提纯综合应用 常见无机物的制备 | 工业流程题 |
| 四、计算题 | |||
| 21 | 0.65 | 物质的量有关计算 物质的量浓度的计算 化学方程式计算中物质的量的运用 钠 | |



