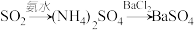重庆市永川景圣中学2020-2021学年高三上学期第二次月考化学试题
重庆
高三
阶段练习
2021-04-17
306次
整体难度:
容易
考查范围:
常见无机物及其应用、化学与STSE、认识化学科学、化学实验基础、有机化学基础、化学反应原理
重庆市永川景圣中学2020-2021学年高三上学期第二次月考化学试题
重庆
高三
阶段练习
2021-04-17
306次
整体难度:
容易
考查范围:
常见无机物及其应用、化学与STSE、认识化学科学、化学实验基础、有机化学基础、化学反应原理
一、单选题 添加题型下试题
单选题
|
适中(0.65)
真题
名校
1. 下列有关从海带中提取碘的实验原理和装置能达到实验目的的是
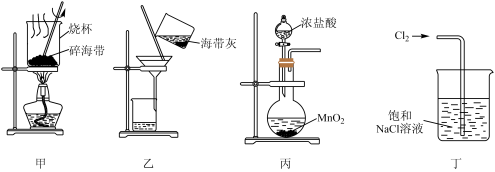

| A.用装置甲灼烧碎海带 |
| B.用装置乙过滤海带灰的浸泡液 |
| C.用装置丙制备用于氧化浸泡液中I−的Cl2 |
| D.用装置丁吸收氧化浸泡液中I−后的Cl2尾气 |
【知识点】 氯气的实验室制法解读 海带中碘的提取及检验解读
您最近一年使用:0次
2018-06-10更新
|
11754次组卷
|
84卷引用:2018年全国普通高等学校招生统一考试化学(江苏卷)
2018年全国普通高等学校招生统一考试化学(江苏卷)【全国百强校】山西省临汾第一中学2017-2018学年高二下学期期末考试化学试题黑龙江省青冈县一中2017-2018学年高一下学期期末考试化学试题江西省南昌三中2019届高二下期末考试 化学(已下线)2018年高考题及模拟题汇编 专题11 化学实验基础【全国百强校】黑龙江省哈尔滨市第三中学2017-2018学年高二下学期期末考试化学试题江苏省盐城市田家炳中学2019届高三上学期开学考试化学试题陕西省城固县第一中学2019届高三上学期第一次月考化学试题辽宁省沈阳市东北育才学校2019届高三上学期第一次模拟考试化学试题湖北省汉川市第二中学2017-2018学年高一下学期期末考试化学试题甘肃省师范大学附属中学2019届高三上学期第一次月考化学试题辽宁省葫芦岛协作校2019届高三上学期第一次月考化学试题甘肃省武威市第二中学2019届高三上学期第二次(10月)月考化学试题【全国百强校】山西省山西大学附属中学2018-2019学年高二上学期9月模块诊断化学试题云南省腾冲市第八中学2018-2019学年高二上学期期中考试化学试题【全国百强校】甘肃省平凉市静宁县第一中学2019届高三上学期第三次模拟考试化学试题江苏师范大学附属实验学校2019届高三上学期10月学情调研化学试题河南省郑州市实验中学2019届高三上学期期中考试化学试题【全国百强校】山东省山东师范大学附属中学2019届高三上学期第五次模拟考试化学试题山西省长治二中2018-2019学年高一下学期第一次月考化学试题【市级联考】陕西省榆林市2019届高三下学期高考模拟第三次测试理科综合化学试题吉林省长春汽车经济开发区第三中学2018-2019学年高一下学期4月月考化学试题(已下线)2019年5月20日 《每日一题》 必修2 海带提碘步步为赢 高一化学暑假作业:作业十六 开发利用金属矿物和海水资源【全国百强校】吉林省延边第二中学2018-2019学年高二下学期第二次月考化学试题黑龙江省大庆市第四中学2018-2019学年高一下学期第三次月考化学试题四川省武胜县烈面中学校2018届高三9月入学考试化学试题湖北省利川市第三中学2019届高三一模化学试题江西省宜春市万载中学2019-2020学年高二上学期期中考试化学试题(衔接班)(已下线)专题10.2 物质的分离、提纯、检验与鉴别(练)-《2020年高考一轮复习讲练测》(已下线)专题10.2 物质的分离、提纯、检验与鉴别(讲)-《2020年高考一轮复习讲练测》河南省南阳市2020届高三上学期期中质量评估化学试题(已下线)考点20 化学基础实验——《备战2020年高考精选考点专项突破题集》福建省莆田第二十五中学2020届高三上学期期末考试化学试题2020届人教版高中化学高三专题基础复习专题1《从实验学化学》测试卷上海市宝山区2020届高三上学期第一次模拟考试(等级考)化学试题广东省2020年普通高中学业水平考试化学合格性考试模拟试题(五)新疆阿克苏市阿瓦提四中2020届高三上学期第二次月考化学试题(已下线)专题3.6 金属材料和无机非金属材料 海水的开发利用 -巅峰冲刺山东省2020年高考化学一轮考点扫描《2020年新高考政策解读与配套资源》江苏省南通市启东市吕四中学2020届高三第一次质量检测化学试题四川省广安市邻水县四川省邻水中学2019-2020学年高一下学期期中考试化学试题(已下线)第02讲 物质的分离和提纯(精讲)——2021年高考化学一轮复习讲练测四川省成都市龙泉中学2021届高三上学期开学考试化学试题(已下线)第6单元 常见的非金属元素(B卷 滚动提升检测)-2021年高考化学一轮复习单元滚动双测卷(已下线)小题必刷18 氯及其化合物——2021年高考化学一轮复习小题必刷(通用版)鲁科版(2019)高一必修第二册 第1章 原子结构 元素周期律微项目 海带提碘与海水提溴高一必修第二册(人教2019版)第八章 化学与可持续发展 素养检测高一必修第一册(苏教2019版)专题3 C 高考挑战区 过模拟 2年模拟精编精练江苏省扬州市江都区大桥高级中学2021届高三上学期期初调研化学试题高一必修第一册(苏教2019)专题3 第三单元 海洋化学资源的综合利用3江苏省邗江中学2020-2021学年高一上学期期中考试化学试题山东师范大学附属中学2021届高三上学期期中考试(11月)化学试题山西省实验中学2019届高三上学期第四次月考化学试题江苏省泰州中学2021届高三上学期第二次月考化学试题专题3 第三单元综合拔高练-高中化学苏教2019版必修第一册(人教版2019)必修第二册 第八章 化学与可持续发展 第一节 自然资源的开发利用云南省普洱市景东县第一中学2021届高三上学期期末考试化学试题(已下线)解密11 化学实验(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密11 化学实验(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)重庆市永川景圣中学2020-2021学年高三上学期第二次月考化学试题吉林省通化县综合高级中学2020-2021学年高一下学期期末考试化学试题内蒙古巴彦淖尔市乌拉特前旗第一中学2020-2021学年高二下学期期末考试化学试题(已下线)考点30 物质的分离、提纯和检验-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点30 物质的分离、提纯和检验-备战2022年高考化学一轮复习考点帮(浙江专用)内蒙古包头市2022届高三上学期起点调研考试化学试题(已下线)课时52 物质的分离、提纯和检验-2022年高考化学一轮复习小题多维练(全国通用)重庆市开州中学高 2021-2022学年高三上学期10月月考化学试题湖北省武汉市蔡甸区实验高级中学2020-2021学年高二上学期10月联合考试化学试题福建省厦门市湖滨中学2021-2022学年高三上学期期中考试化学试题山东省济南市莱芜第一中学2021-2022学年高三上学期期中考试化学试题福建省厦门市翔安第一中学2021-2022学年高一下学期第一次月考(3月)化学试题湖南省浏阳市第一中学2022届高三下学期期中考试化学试题云南省昭通市永善、绥江县2021-2022学年高一上学期期末考试化学试题山东省菏泽市单县第五中学2021-2022学年高一下学期第一次段考化学(A)试题新疆叶城县第八中学2021-2022学年高三上学期第二次月考化学试题贵州省贵阳市2022-2023学年高三上学期10月质量监测化学试题四川省广安市育才学校2022-2023学年高一上学期9月月考化学试题江苏省扬州中学2022-2023学年高一上学期期中检测化学试题湖南省长沙市同升湖实验学校2022-2023学年高三上学期第三次月考化学试题广东省揭阳市惠来县第一中学2022-2023学年高二上学期期中考试化学试题第四章 非金属及其化合物 第19讲 卤素的性质及提取(已下线)题型46 从海水中提取氯、溴、碘广东省广州市越秀区2023-2024学年高二上学期开学考试化学试题河南省焦作第一中学2023-2024学年高三上学期9月化学模拟测试
单选题
|
适中(0.65)
名校
2. 在给定条件下,下列选项所示的物质间转化均能实现的是
A. |
B. |
C.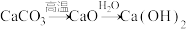 |
D.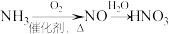 |
【知识点】 物质的转化 一氧化氮的化学性质解读 含硫化合物之间的转化解读
您最近一年使用:0次
2021-01-08更新
|
2157次组卷
|
36卷引用:山东省淄博市淄川中学2016-2017学年高二下学期学分认定(期末)考试化学试题
山东省淄博市淄川中学2016-2017学年高二下学期学分认定(期末)考试化学试题河北省涞水波峰中学2018届高三第一次调研考试化学试题(已下线)【中等生百日捷进提升系列-基础练测】专题2.11 非金属及其化合物吉林省长春汽车经济开发区第六中学2017-2018学年高一下学期4月月考化学试题北京市密云区2017-2018学年高三第二学期阶段性练习理综化学试题(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第4讲 氮及其化合物【教学案】(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第3讲 铁及其化合物【教学案】(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第2讲 氧及其化合物【教学案】(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第3讲 硫及其化合物【教学案】(已下线)2019高考热点题型和提分秘籍 第四章 常见的非金属及其化合物 第3讲 硫及其化合物 (教学案)(已下线)2019高考热点题型和提分秘籍 第四章 常见的非金属及其化合物 第4讲 氮及其化合物 (教学案)(已下线)2019高考备考二轮复习精品资料-专题5 金属及其化合物(教学案)【校级联考】辽宁省六校协作体2018-2019学年高一下学期期初考试化学试题百所名校联考-化学物质及其变化四川省内江市2018-2019学年高一下学期期末检测(理)化学试题海南省嘉积中学2020届高三上学期第二次月考化学试题辽宁省大连市第三中学2019-2020学年高三上学期第三次月考化学试题黑龙江省哈尔滨市第三十二中学2020届高三上学期期末考试化学试题人教版(2019)必修第二册第五章 模拟高考江西省安福中学2019-2020学年高一(普通班)下学期3月线上考试化学试题湖北省武汉市华中师范大学第一附属中学2020届高三2月份网络教学质量监测理综化学试题吉林省长春市东北师大附中2020届高中毕业班二月份网络教学质量监测卷理科综合化学部分江苏省连云港市赣榆区2020届高三高考仿真训练化学试题必修第二册RJ第5章挑战区 模拟高考(已下线)第三单元 物质的性质与转化(基础过关)-2020-2021学年高一化学必修第一册单元测试定心卷 (鲁科版2019)甘肃省武威市民勤县第一中学2019-2020学年高一下学期期中考试化学(文) 试题吉林省长春市第五中学2021届高三上学期期中考试化学试题内蒙古自治区乌兰察布市四子王旗第一中学2021届高三上学期期中考试化学试题专题7 第一~二单元 综合拔高练-高中化学必修第二册苏教版2019(已下线)【浙江新东方】高中化学20210304-019重庆市永川景圣中学2020-2021学年高三上学期第二次月考化学试题黑龙江省哈尔滨市阿城区龙涤中学2020-2021学年高一4月月考化学试题黑龙江省哈尔滨市第一六二中学校2020-2021学年高一下学期4月月考化学试题河南省宋基信阳实验中学2021-2022学年高一下学期第二次月考化学试题辽宁省北镇市满族高级中学2022-2023学年高三上学期第一次质量检测化学试题宁夏六盘山高级中学2022-2023学年高一下学期第一次月考化学(乙卷)试题
单选题
|
适中(0.65)
3. 根据SO2通入不同溶液中的实验现象,所得结论不正确的是
| 选项 | 实验 | 现象 | 结论 |
| A | 含HCl、BaCl2的FeCl3溶液 | 产生白色沉淀 | SO2有还原性 |
| B | H2S溶液 | 产生黄色沉淀 | SO2有氧化性 |
| C | 酸性KMnO4溶液 | 紫色溶液褪色 | SO2有漂白性 |
| D | Na2SiO3溶液 | 产生胶状沉淀 | 酸性:H2SO3>H2SiO3 |
| A.A | B.B | C.C | D.D |
【知识点】 二氧化硫的化学性质 物质性质实验方案的设计解读
您最近一年使用:0次
2023-06-07更新
|
1558次组卷
|
108卷引用:山东省淄博市淄川中学2016-2017学年高二下学期学分认定(期末)考试化学试题
山东省淄博市淄川中学2016-2017学年高二下学期学分认定(期末)考试化学试题河北省安平中学2016-2017学年高二下学期期末考试化学试题2017年全国普通高等学校招生统一考试理综化学(北京卷精编版)河北省涞水波峰中学2018届高三第一次调研考试化学试题江西省横峰中学、铅山一中、德兴一中2018届高三上学期第一次月考化学试题宁夏六盘山高级中学2018届高三上学期第一次月考化学试题山东省郓城实验中学2018届高三10月月考化学试题江西省铅山县第一中学2018届高三上学期第一次月考化学试题黑龙江省哈尔滨市第六中学2018届高三12月月考化学试题辽宁省大连渤海高级中学2018届高三上学期期末考试化学试题云南省玉溪第一中学2017-2018学年高一下学期4月月考化学试题云南省玉溪市玉溪一中2017-2018学年高一下学期4月月考化学试题内蒙古北方重工业集团有限公司第三中学2017-2018学年高一3月月考化学试题(已下线)《考前20天终极攻略》-5月21日 基础实验(已下线)《考前20天终极攻略》-5月26日 元素及其化合物(已下线)解密06 非金属及其化合物(教师版)——备战2018年高考化学之高频考点解密【全国市级联考】四川省广安市2017-2018学年高一下学期期末考试化学试题(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第2讲 氧及其化合物【教学案】(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第3讲 硫及其化合物【教学案】【全国百强校】北京市中央民族大学附属中学(朝阳分校)2019届高三上学期10月月考化学试题【全国百强校】宁夏回族自治区育才中学2019届高三上学期月考(二)化学试题云南省腾冲市第八中学2018-2019学年高二上学期期中考试化学试题【全国百强校】山东省济南市第一中学2019届高三上学期期中考试化学试题(已下线)2019高考热点题型和提分秘籍 第四章 常见的非金属及其化合物 第3讲 硫及其化合物 (教学案)【全国百强校】黑龙江省哈尔滨市第六中学2019届高三上学期12月月考化学试题(已下线)2019高考热点题型和提分秘籍 第四章 常见的非金属及其化合物 第1讲 碳、硅及无机非金属材料 (教学案)山东省德州市夏津县第一中学2019届高三上学期12月月考化学试题(已下线)2019高考备考二轮复习精品资料-专题6 非金属及其化合物(教学案)(已下线)2019高考备考二轮复习精品资料-专题6 非金属及其化合物(押题专练)(已下线)2019高考备考二轮复习精品资料-专题5 金属及其化合物(教学案)(已下线)2019年高考总复习巅峰冲刺-专题08 常见无机物及其应用应试策略河南省封丘县第一中学2018-2019学年高一下学期开学考试化学试题步步为赢 高二化学暑假作业:作业十三 化学实验综合内蒙古包头稀土高新区二中2020届高三10月月考理综化学试题四川省绵阳市南山中学2020届高三10月月考化学试题四川省成都石室中学2019-2020学年高二入学考试化学试题北京师范大学实验中学丰台学校2019-2020学年高三上学期期中考试化学试题2020届高三化学一轮复习 化学基础实验(选择题和大题训练)四川省成都市实验中学2020届高三上学期第十四次周考理科综合化学试题(已下线)专题01 硫及其化合物(核心素养卷)-【新教材精创】2019-2020学年高一化学新教材知识讲学(必修第二册)(已下线)专题六 元素化合物的性质、应用及转化(真题汇编)-2020年高考二轮模块化复习之《元素化合物》名师讲案与提分特训四川省成都市第七中学2020年高中毕业班教学质量监测卷理科综合化学试题广东省深圳中学2020年高中毕业班教学质量监测卷理科综合化学试题河北省衡水中学2020年高中毕业班教学质量监测卷理科综合化学试题辽宁省沈阳东北育才中学2020年高中毕业班教学质量监测卷理科综合化学试题山东省济宁市汶上圣泽中学2019-2020学年高一下学期第二次月考化学试题贵州省贵阳市第一中学2020届高三教学质量监测理科综合化学试题安徽省黄山市八校联盟2019-2020学年高一下学期期中联考化学试题(已下线)专题4.3 硫及其化合物(练)——2020年高考化学一轮复习讲练测(已下线)专题4.3 硫及其化合物(讲)——2020年高考化学一轮复习讲练测云南省昆明市寻甸县民族中学2019-2020学年高一下学期第一次月考化学试题河北省衡水市桃城区第十四中学2019-2020学年高一下学期第二次综合测试化学试题黑龙江省大庆市第十中学2019-2020学年高二下学期期末考试化学试题四川省泸县第二中学2019-2020学年高一下学期期末模拟考试化学试题苏教版(2020)高一必修第一册专题4 总结检测(已下线)第15讲 硫及其化合物(精讲)——2021年高考化学一轮复习讲练测安徽省阜阳市阜南实验中学2020届高三下学期4月月考化学试题山东省济南市章丘区第四中学2021届高三上学期第一次教学质量检测(8月)化学试题黑龙江省哈尔滨市第三中学校2020-2021学年高三上学期第一次验收考试化学试题湖北省宜昌市葛洲坝中学2021届高三9月月考化学试题陕西省西安中学2018-2019学年高一下学期期末考试化学题湖南省邵阳市邵东县创新实验学校2021届高三上学期第一次月考化学试题(已下线)专题讲座(四) 常见气体的实验室制备、净化和收集(精练)-2021年高考化学一轮复习讲练测福建省莆田第二十五中学2021届高三上学期期中考试化学试题江西省鹰潭市2019-2020年度高一下学期期末检测化学试题吉林省长春市第二十九中学2021届高三上学期期末考试化学试题专题4 第一单元综合拔高练-高中化学苏教2019版必修第一册辽宁沈阳市第二十八中学2020--2021学年高一上学期期末考试化学试题河北省深州市长江中学2020-2021学年高一下学期3月底月考化学试题新疆维吾尔自治区巴州二中2021届高三第六次月考化学试题重庆市永川景圣中学2020-2021学年高三上学期第二次月考化学试题广东实验中学2020-201学年高一下学期期中考试化学(合格考)试题云南省楚雄天人中学2020-2021学年高一下学期3月月考化学(A)试题(已下线)课时22 硫及其化合物-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第11讲 硫及其化合物(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第7周 晚练题-备战2022年高考化学周测与晚练(新高考专用)安徽省马鞍山市含山县第二中学2021-2022学年高三上学期第一次月考化学试题广西河池市高级中学2021-2022学年高三上学期第三次月考化学试题云南省丽江市第一高级中学2021-2022学年高二下学期4月月考化学试题(已下线)考点10 硫及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)北京市顺义牛栏山第一中学2021-2022学年高一下学期居家学习成果展示化学测试题北京师范大学附属中学2021-2022学年高一下学期期中考试化学试题(已下线)第11讲 硫及其化合物(讲)-2023年高考化学一轮复习讲练测(新教材新高考)甘肃省武威第十八中学2022-2023学年高三上学期第一次诊断化学试题黑龙江省哈尔滨市第三中学校2022-2023学年高三上学期第一次验收考试化学试题黑龙江省哈尔滨市第三中学校2022-2023学年高三上学期9月月考化学试题辽宁省本溪满族自治县高级中学2021-2022学年高一下学期开学考试化学试题黑龙江省哈尔滨市第十九中学2021-2022学年高三上学期第一次月考化学试题(已下线)化学(北京A卷)-学易金卷:2023年高考第一次模拟考试卷云南省红河县第一中学2020-2021学年高一下学期期末考试化学试题(已下线)题型48 SO2的制备与性质探究北京市顺义区第一中学2022-2023学年高一下学期3月月考化学试题宁夏银川市第二中学2022-2023学年高一下学期第一次月考化学试题山东省济宁市曲阜孔子高级中学2022-2023学年高一下学期4月月考化学试题黑龙江省齐齐哈尔市第八中学校2022-2023学年高一下学期3月月考化学试题广东省开平市忠源纪念中学2022-2023学年高一下学期4月期中考试化学试题广东省东莞市东华高级中学2022-2023学年高一下学期3月月考化学试题广东省深圳聚龙科学中学2022-2023学年高一下学期第一次段考(学业水平)化学试题广东省广州市广东实验中学2020-2021学年高一下学期期中考试(合格考)化学试题(已下线)第3讲 硫及其重要化合物北京市第二中学2022-2023学年高一下学期期末考试化学试题黑龙江省七台河市勃利县高级中学2022-2023学年高三上学期11月期中考试化学试题江苏省南菁高级中学2023-2024学年高一上学期9月阶段性检测化学(创优班)试题北京师范大学第二附属中学2023-2024学年高一下学期3月化学测试题陕西省咸阳市三原县北城中学2023-2024学年高一下学期第一次月考化学试题(已下线)专题01 硫、氮及其化合物-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(北京专用)
单选题
|
适中(0.65)
名校
4. 下图是制取和收集某气体的实验装置,该装置可用于


| A.用浓硫酸和氯化钠反应制取HCl |
| B.用浓氨水和生石灰反应制取NH3 |
| C.用双氧水与二氧化锰反应制取O2 |
| D.用饱和食盐水和电石反应制取C2H2 |
【知识点】 氨气的制备 乙炔的制备 常见气体的制备与收集解读
您最近一年使用:0次
2016-12-09更新
|
715次组卷
|
4卷引用:2013届上海市浦东新区高三下学期二模化学试卷
(已下线)2013届上海市浦东新区高三下学期二模化学试卷上海交通大学附属中学2016-2017学年高一上学期期中考试化学试题2(已下线)上海市浦东新区2013届高三4月高考预测(二模)化学试题重庆市永川景圣中学2020-2021学年高三上学期第二次月考化学试题
单选题
|
适中(0.65)
名校
您最近一年使用:0次
2021-04-14更新
|
155次组卷
|
2卷引用:重庆市永川景圣中学2020-2021学年高三上学期第二次月考化学试题
单选题
|
容易(0.94)
名校
6. 等物质的量的下列物质,分别与足量NaOH溶液反应,消耗NaOH的物质的量最多的是
| A.Al2O3 | B.KAl(SO4)2 |
| C.Al(OH)3 | D.Al |
您最近一年使用:0次
2017-11-27更新
|
1217次组卷
|
7卷引用:2015-2016学年山东省武城县第二中学高一下学期3月月考化学试卷
单选题
|
较易(0.85)
7. 下列有关焰色反应的实验操作及注意事项正确的是( )
| A.只有把盐配制成溶液才能进行焰色反应 |
| B.实验时用铂丝直接蘸取药品在酒精灯上灼烧 |
| C.可以用铁丝代替铂丝进行焰色反应 |
| D.实验后要用稀硫酸将铂丝洗净 |
您最近一年使用:0次
2020-01-29更新
|
206次组卷
|
4卷引用:苏教版高中化学必修1专题一《化学家眼中的物质世界》测试卷
单选题
|
较易(0.85)
名校
8. 下列关于钠的说法中不正确的是
| A.金属钠和氧气反应,条件不同,产物不同 |
| B.大量的钠着火时可以用沙子扑灭,少量的钠应保存在煤油中 |
| C.将一小块钠投入装有氯化镁溶液的试管里,钠熔成小球并在液面上游动 |
| D.将一小块钠投入装有硫酸铜溶液的试管里,试管底部有红色物质生成 |
您最近一年使用:0次
2018-10-23更新
|
1075次组卷
|
21卷引用:山东省德州市第一中学2018-2019学年高一第一学期模块检测化学试题
山东省德州市第一中学2018-2019学年高一第一学期模块检测化学试题福建省邵武七中2018-2019学年高一上学期期中考试化学试题第1章《走进化学科学》期中复习检测试卷海南省海南枫叶国际学校2019-2020学年高一上学期期中考试化学试题鲁教版高中必修1化学第一章《认识化学科学》测试卷2019-2020学年高一上学期期末复习《新题速递·化学》12月(考点06-11)福建省连城县第一中学2020-2021学年高一上学期月考(一)化学试题(已下线)第一章 认识化学科学(基础过关)-2020-2021学年高一化学上学期必修第一册《单元测试定心卷》 (鲁科版2019)辽宁省黑山县黑山中学2020-2021学年高一10月月考化学试题湖北生松滋市言程中学2020-2021学年高一上学期10月月考化学试题广东省东莞市光明中学2020-2021学年高一上学期期中考试化学试题山西省临汾市县底中学校2020-2021学年高一上学期开学考试化学试题重庆市永川景圣中学2020-2021学年高三上学期第二次月考化学试题吉林省吉林市永吉县第四中学2021-2022学年高一上学期期中考试化学试题广东省东莞市第四高级中学2021-2022学年高一上学期期中考试化学试题吉林省辉南县第一中学2021-2022学年高一上学期第二次月考化学试卷广东实验中学附属天河学校2021-2022学年高一上学期期中考试化学试题江西省抚州创新实验学校2021-2022学年高一上学期期末考试化学试题云南省蒙自市第一高级中学与会泽县茚旺高中致远中学2023-2024学年高一上学期10月月考化学试题内蒙古自治区赤峰四中2021-2022学年高一上学期期中考试化学试题河南省郑州市第四高级中学2023-2024学年高一上学期西藏班第二次调研考试 化学试题
单选题
|
较易(0.85)
解题方法
9. 下列说法不正确的是
| A.二氧化硫和二氧化氮是主要的大气污染物 |
| B.普通玻璃的主要成分是纯碱、石灰石和石英砂 |
| C.铝制餐具不宜用来蒸煮或长时间存放酸性、碱性或咸的食物 |
| D.煤的干馏、气化和液化是煤综合利用的主要途径,都属于化学变化 |
您最近一年使用:0次
单选题
|
适中(0.65)
10. 物质的性质往往决定了其用途,下列说法不正确的是
| A.硅是半导体材料,可用作光导纤维 |
B. 能与 能与 反应,可用作呼吸面具的供氧剂 反应,可用作呼吸面具的供氧剂 |
C.明矾能水解生成 胶体,可用作净水剂 胶体,可用作净水剂 |
D. 熔点高,可用于制作耐高温仪器 熔点高,可用于制作耐高温仪器 |
您最近一年使用:0次
2021-04-14更新
|
158次组卷
|
2卷引用:重庆市永川景圣中学2020-2021学年高三上学期第二次月考化学试题
单选题
|
容易(0.94)
真题
名校
您最近一年使用:0次
2020-07-11更新
|
5422次组卷
|
44卷引用:2020年天津卷化学高考试题
2020年天津卷化学高考试题(已下线)专题05 元素及其化合物-2020年高考真题和模拟题化学分项汇编(已下线)小题必刷01 物质的组成、分类和性质 ——2021年高考化学一轮复习小题必刷(通用版)辽宁师范大学附属中学2019-2020学年高二下学期期末考试化学试题黑龙江省哈尔滨市第九中学2021届高三上学期开学考试化学试题安徽省六安市城南中学2020-2021学年高二上学期开学考试化学试题山东省日照市五莲县2020-2021学年高一上学期期中考试化学试题吉林松原市油田第十一中学2021届高三第二次阶段考试化学试题重庆市第七中学2021届高三上学期第一次月考化学试题天津市第三中学2021届高三下学期2月月考化学试题云南省文山州砚山县第三高级中学2020-2021学年高一上学期期中考试化学试题吉林省长春市第二十中学2020-2021学年高一上学期第二次考试化学试题吉林省长春市第二十中学2020-2021学年高一上学期第三次考试化学试题上海市崇明区2021届高三下学期二模化学试题重庆市永川景圣中学2020-2021学年高三上学期第二次月考化学试题天津市实验中学滨海学校2021届高三上学期第一次月考化学试题黑龙江双鸭山市第一中学2020-2021学年高二下学期期末考试化学试题(已下线)课时14 钠及其化合物-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考向06 钠及其重要化合物-备战2022年高考化学一轮复习考点微专题(已下线)第10讲 氯及其化合物(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)考向11 氯及其化合物-备战2022年高考化学一轮复习考点微专题吉林市第五十五中学2021-2022学年高一上学期期中考试化学(理)试题江西省赣州市赣县第三中学2021-2022学年高一上学期期中适应考试化学试题河北省唐山市2021-2022学年高一上学期期末考试化学试题(已下线)2020年天津卷化学高考真题变式题1-12陕西省西北农林科技大学附属中学2021-2022学年高一上学期期末考试化学试题(已下线)卷04 元素及其化合物-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)陕西省丹凤中学2021-2022学年高一下学期5月月考化学试题天津市河东区普通高中2022年高二学业水平合格考试模拟化学试题(已下线)专题02 海水中的重要元素——钠和氯-2023年高考化学一轮复习小题多维练(全国通用)黑龙江省饶河县高级中学2021-2022学年高一上学期期中考试化学试题(已下线)第10讲 氯及其化合物(练)-2023年高考化学一轮复习讲练测(新教材新高考)天津市红桥区2020-2021学年高一下学期期末考试化学试题云南省德宏州2020-2021学年高一上学期期末统一监测化学试题新疆额敏县第二中学2021-2022学年高一上学期期中考试化学试题湖南省张家界市慈利县2020-2021学年高一上学期期中教学质量检测化学试题湖南省长沙市实验中学2022-2023学年高一上学期期中考试化学试题湖南省邵阳市武冈市2020-2021学年高一上学期期中考试化学试题黑龙江省齐齐哈尔市三立高级中学2022-2023学年高三上学期期中考试化学试题陕西省西安市鄠邑区第二中学2021-2022学年高三上学期第二次月考化学试题湖南省新邵县第二中学2020-2021学年高一上学期期中考试化学试题第三章 金属及其化合物 第12讲 Na2CO3、NaHCO3 碱金属安徽省马鞍山市第二十二中学2022-2023学年高二下学期开学考试化学试题辽宁省阜新市第二高级中学2023-2024学年高一上学期第二次月考化学试卷
12. 用CuS、Cu2S处理酸性废水中的Cr2O ,发生反应如下:
,发生反应如下:
反应Ⅰ:CuS+Cr2O +H+→Cu2++SO
+H+→Cu2++SO +Cr3++H2O(未配平)
+Cr3++H2O(未配平)
反应Ⅱ:Cu2S+Cr2O +H+→Cu2++SO
+H+→Cu2++SO +Cr3++H2O(未配平)
+Cr3++H2O(未配平)
下列有关说法正确的是( )
 ,发生反应如下:
,发生反应如下:反应Ⅰ:CuS+Cr2O
 +H+→Cu2++SO
+H+→Cu2++SO +Cr3++H2O(未配平)
+Cr3++H2O(未配平)反应Ⅱ:Cu2S+Cr2O
 +H+→Cu2++SO
+H+→Cu2++SO +Cr3++H2O(未配平)
+Cr3++H2O(未配平)下列有关说法正确的是( )
A.反应Ⅰ和Ⅱ中Cu2+、SO 都是氧化产物 都是氧化产物 |
| B.反应Ⅱ中还原剂、氧化剂的物质的量之比为2∶5 |
C.处理1molCr2O 时反应Ⅰ、Ⅱ中消耗H+的物质的量相等 时反应Ⅰ、Ⅱ中消耗H+的物质的量相等 |
D.反应Ⅰ、Ⅱ中每处理1molCr2O ,转移电子的数目相等 ,转移电子的数目相等 |
【知识点】 氧化还原反应有关计算 氧化还原反应方程式的配平解读
您最近一年使用:0次
2020-10-03更新
|
153次组卷
|
2卷引用:宁夏银川一中2021届高三上学期第二次月考理综化学试题
单选题
|
适中(0.65)
13. 若NA表示阿伏加 德罗常数,则下列说法正确的是( )
| A.64g铜与足量的S完全反应,转移的电子数为NA |
| B.标准状况下,22.4LNO与11.2LO2充分反应后得到的气体分子数为NA |
| C.pH=13的Ba(OH)2溶液中,含有OH-0.2NA个 |
| D.50mL18mol·L-1的浓硫酸与足量的铜加热充分反应后,得到的气体分子数为0.45NA |
您最近一年使用:0次
2020-10-03更新
|
235次组卷
|
4卷引用:宁夏银川一中2021届高三上学期第二次月考理综化学试题
单选题
|
适中(0.65)
名校
解题方法
14. 在FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断错误的是( )
| A.加入KSCN溶液一定不变红色 | B.溶液中一定含Cu2+ |
| C.溶液中一定含Fe2+ | D.剩余固体中一定含铜 |
您最近一年使用:0次
2020-10-25更新
|
843次组卷
|
22卷引用:2013-2014学年河北冀州中学高一上学期第四次月考化学试卷
(已下线)2013-2014学年河北冀州中学高一上学期第四次月考化学试卷2014-2015河北省故城县高级中学高一12月月考化学试卷2014-2015黑龙江省绥化市三校高一上学期期末联考化学试卷黑龙江省哈尔滨市第六中学2017-2018学年高一12月月考化学试题黑龙江省哈尔滨六中2017-2018学年高一12月月考化学试卷【全国百强校】山西省山西大学附属中学2018-2019学年高一上学期12月月考化学试题人教版(2019)高一必修第一册 第三章 第一节 铁及其化合物甘肃省武威第六中学2021届高三上学期第三次过关考试化学试题吉林省吉化第一高级中学校2020-2021学年高一上学期第一次月考化学试题重庆市永川景圣中学2020-2021学年高三上学期第二次月考化学试题浙江省诸暨市2016-2017学年高一上学期期末考试化学试题 河南省开封市五县2021-2022学年高一上学期12月月考联考化学试题(已下线)5.2.3 重要的金属化合物(第3课时)-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)陕西省西安市西航一中2021~2022学年高一上学期期末考试化学试题江苏省苏州市吴江汾湖高级中学2021-2022学年高一下学期期中考试化学试题(已下线)第三章 铁 金属材料(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)湖南省长沙市明德中学2022-2023学年高一上学期12月选科调研考试化学试题河北省石家庄外国语学校2022-2023学年高一上学期期中考试化学试题山东省枣庄市滕州市第五中学2022-2023学年高一上学期第二次线上考试化学试题福建省三明第一中学2023-2024学年高一上学期期中考试化学试题天津市第五十四中学2023-2024学年高一上学期第二次月考(12月考)化学试题湖南省永州市蓝山县第二中学2023-2024学年高一上学期第三次月考化学试卷
二、填空题 添加题型下试题
填空题
|
适中(0.65)
15. 根据要求回答下列问题:
(1)写出下列物质在水溶液中的电离方程式:
① :
:__________ ;
②
___________ ;
③写出①②水溶液混合后恰好沉淀完全的离子方程式______________ ;
(2)标准状况下,相同质量的 和
和 物质的量比为
物质的量比为_____ ,所含氧原子数比为______ ,密度比为______ 。
(3)某建筑材料主要成分为铝硅酸盐,化学式是 ;改写成氧化物形式为
;改写成氧化物形式为______ 。
(1)写出下列物质在水溶液中的电离方程式:
①
 :
:②

③写出①②水溶液混合后恰好沉淀完全的离子方程式
(2)标准状况下,相同质量的
 和
和 物质的量比为
物质的量比为(3)某建筑材料主要成分为铝硅酸盐,化学式是
 ;改写成氧化物形式为
;改写成氧化物形式为
您最近一年使用:0次
填空题
|
较易(0.85)
解题方法
16. 完成下列各题。
光导纤维的主要成分是________ (填“ ”或“Si”),实验室里常往
”或“Si”),实验室里常往 溶液中加入
溶液中加入_____ (填“氨水”或“NaOH溶液”)来制取 。实验室检测
。实验室检测 中含有
中含有 ,应选用的试剂是
,应选用的试剂是______ (填“ 溶液”或“NaOH溶液”),应选择的试纸是
溶液”或“NaOH溶液”),应选择的试纸是_______ (填“红色石蕊试纸”或“蓝色石蕊试纸”)。
光导纤维的主要成分是
 ”或“Si”),实验室里常往
”或“Si”),实验室里常往 溶液中加入
溶液中加入 。实验室检测
。实验室检测 中含有
中含有 ,应选用的试剂是
,应选用的试剂是 溶液”或“NaOH溶液”),应选择的试纸是
溶液”或“NaOH溶液”),应选择的试纸是
您最近一年使用:0次
三、计算题 添加题型下试题
计算题
|
适中(0.65)
名校
解题方法
17. 把由NaOH、 、
、 三种固体组成的混合物溶于足量的水中,有
三种固体组成的混合物溶于足量的水中,有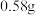 白色沉淀析出,向所得的浑浊液中逐滴加入
白色沉淀析出,向所得的浑浊液中逐滴加入 的盐酸,加入盐酸的体积和生成沉淀的质量如图所示。
的盐酸,加入盐酸的体积和生成沉淀的质量如图所示。

(1)混合物中NaOH的质量是________ g, 的质量是
的质量是________ g, 的质量是
的质量是________ g。
(2) 点加入盐酸的体积为
点加入盐酸的体积为________ mL。
 、
、 三种固体组成的混合物溶于足量的水中,有
三种固体组成的混合物溶于足量的水中,有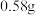 白色沉淀析出,向所得的浑浊液中逐滴加入
白色沉淀析出,向所得的浑浊液中逐滴加入 的盐酸,加入盐酸的体积和生成沉淀的质量如图所示。
的盐酸,加入盐酸的体积和生成沉淀的质量如图所示。 
(1)混合物中NaOH的质量是
 的质量是
的质量是 的质量是
的质量是(2)
 点加入盐酸的体积为
点加入盐酸的体积为
您最近一年使用:0次
2020-02-17更新
|
189次组卷
|
3卷引用:2018学年上海市控江中学高二第一学期第一次月考化学考试
四、解答题 添加题型下试题
解答题-工业流程题
|
适中(0.65)
名校
解题方法
18. 从含铜丰富的自然资源黄铜矿(CuFeS2)冶炼铜的工艺流程如下:
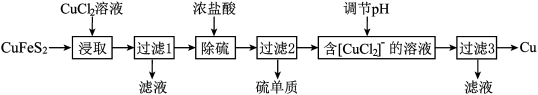
已知:CuFeS2+3CuCl2=4CuCl+FeCl2+2S
(1)浸取时,若改用FeCl3溶液,也能生成CuCl和S,该反应化学方程式为_____ .
(2)若过滤1所得滤液中只含FeCl2,则将其在空气中加热蒸干、灼烧后,所得固体的化学式为_____ .
(3)调节溶液的pH后,除生成Cu外,还能产生一种金属离子,此金属离子是_____ .(填离子符号)
(4)过滤3所得滤液中可以循环使用的物质有_____ ,为保持流程持续循环,每生成1molCu,理论上需补充CuCl2的物质的量为_____ .
(5)冶炼工艺还可以将精选后的黄铜矿砂与空气在高温下煅烧,使其转变为铜,化学方程式为:6CuFeS2+13O2 3Cu2S+2Fe3O4+9SO2、Cu2S+O2
3Cu2S+2Fe3O4+9SO2、Cu2S+O2 2Cu+SO2此工艺与前一工艺相比主要缺点有
2Cu+SO2此工艺与前一工艺相比主要缺点有_____ .

已知:CuFeS2+3CuCl2=4CuCl+FeCl2+2S
(1)浸取时,若改用FeCl3溶液,也能生成CuCl和S,该反应化学方程式为
(2)若过滤1所得滤液中只含FeCl2,则将其在空气中加热蒸干、灼烧后,所得固体的化学式为
(3)调节溶液的pH后,除生成Cu外,还能产生一种金属离子,此金属离子是
(4)过滤3所得滤液中可以循环使用的物质有
(5)冶炼工艺还可以将精选后的黄铜矿砂与空气在高温下煅烧,使其转变为铜,化学方程式为:6CuFeS2+13O2
 3Cu2S+2Fe3O4+9SO2、Cu2S+O2
3Cu2S+2Fe3O4+9SO2、Cu2S+O2 2Cu+SO2此工艺与前一工艺相比主要缺点有
2Cu+SO2此工艺与前一工艺相比主要缺点有
您最近一年使用:0次
2019-11-27更新
|
557次组卷
|
6卷引用:2016届江苏省清江中学高三下学期考前练习化学试卷
2016届江苏省清江中学高三下学期考前练习化学试卷(已下线)2019高考热点题型和提分秘籍 第三章 金属及其化合物 第4讲 金属材料与矿物 铜及其化合物 (题型专练)江苏省苏州市2020届高三上学期期初调研化学试题广东省深圳市龙岗区龙城高级中学2021届高三第一次模拟考试化学试题重庆市永川景圣中学2020-2021学年高三上学期第二次月考化学试题(已下线)考点12 金属材料(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
解答题-实验探究题
|
适中(0.65)
19. 亚硝酰氯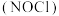 常作催化剂,其沸点为
常作催化剂,其沸点为 ,遇水发生剧烈反应,生成一种氢化物和两种氧化物。某小组设计实验制备亚硝酰氯并测定其纯度,制备原理:
,遇水发生剧烈反应,生成一种氢化物和两种氧化物。某小组设计实验制备亚硝酰氯并测定其纯度,制备原理: ,实验装置如图所示。
,实验装置如图所示。

回答下列问题:
(1)仪器a的名称为____________ ,写出装置A中发生反应的离子方程式____________
(2)请从化学平衡的角度解释饱和NaCl溶液的作用___________________
(3)装置C中装入的化学试剂为______________
(4)装药品之后,关闭________ (填“ ”,“
”,“ ”,“
”,“ ”,下同),打开
”,下同),打开__________ ,引发A中反应,通入一段时间气体,其目的是排除_____________ 对实验产生干扰。然后通过控制止水夹开关,使两种气体在D中反应,当三颈瓶内有少量液体时停止反应。
(5)装置E的作用为___________________
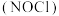 常作催化剂,其沸点为
常作催化剂,其沸点为 ,遇水发生剧烈反应,生成一种氢化物和两种氧化物。某小组设计实验制备亚硝酰氯并测定其纯度,制备原理:
,遇水发生剧烈反应,生成一种氢化物和两种氧化物。某小组设计实验制备亚硝酰氯并测定其纯度,制备原理: ,实验装置如图所示。
,实验装置如图所示。 
回答下列问题:
(1)仪器a的名称为
(2)请从化学平衡的角度解释饱和NaCl溶液的作用
(3)装置C中装入的化学试剂为
(4)装药品之后,关闭
 ”,“
”,“ ”,“
”,“ ”,下同),打开
”,下同),打开(5)装置E的作用为
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、化学与STSE、认识化学科学、化学实验基础、有机化学基础、化学反应原理
试卷题型(共 19题)
题型
数量
单选题
14
填空题
2
计算题
1
解答题
2
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 氯气的实验室制法 海带中碘的提取及检验 | |
| 2 | 0.65 | 物质的转化 一氧化氮的化学性质 含硫化合物之间的转化 | |
| 3 | 0.65 | 二氧化硫的化学性质 物质性质实验方案的设计 | |
| 4 | 0.65 | 氨气的制备 乙炔的制备 常见气体的制备与收集 | |
| 5 | 0.65 | 氨的还原性 酸性氧化物的通性 含镁化合物 与“铁三角”有关的推断 | |
| 6 | 0.94 | 明矾 铝与强碱溶液反应 氧化铝与碱溶液反应 氢氧化铝与强碱反应 | |
| 7 | 0.85 | 焰色试验 | |
| 8 | 0.85 | 钠的化学性质 钠单质的保存与用途 钠与水反应原理 钠与盐溶液的反应 | |
| 9 | 0.85 | 硫、氮氧化物对人体、环境的危害 酸雨 硅酸盐工业 铝制品日常使用的注意事项 煤的综合利用 | |
| 10 | 0.65 | 二氧化硅的用途 过氧化钠的物理性质、组成、结构及用途 氧化铝的物理性质与用途 明矾的净水作用及原理 | |
| 11 | 0.94 | 氯气与碱溶液反应 | |
| 12 | 0.65 | 氧化还原反应有关计算 氧化还原反应方程式的配平 | |
| 13 | 0.65 | 阿伏加德罗常数的应用 结合气体物质与NA相关推算 结合氧化还原反应知识与NA相关推算 | |
| 14 | 0.65 | 铁与铁离子反应 Fe、Cu及相关离子的反应 Fe、Cu与Fe3+反应几种情况分析及判断 | |
| 二、填空题 | |||
| 15 | 0.65 | 阿伏加德罗定律的应用 电离方程式 离子方程式的书写 硅酸盐组成的表示方法 | |
| 16 | 0.85 | 铵根离子的检验 二氧化硅 氢氧化铝的制备 | |
| 三、计算题 | |||
| 17 | 0.65 | 化学方程式计算中物质的量的运用 氢氧化铝与强碱反应 铝盐与强碱溶液反应 偏铝酸钠与盐酸的反应 | |
| 四、解答题 | |||
| 18 | 0.65 | 氧化还原反应方程式的配平 铜的其他化合物 物质分离、提纯综合应用 | 工业流程题 |
| 19 | 0.65 | 氯气的实验室制法 一氧化氮的化学性质 浓度对化学平衡移动的影响 常见无机物的制备 | 实验探究题 |

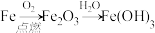
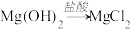 溶液
溶液