湖北省汉川市第二中学2017-2018学年高一下学期期末考试化学试题
湖北
高一
期末
2018-09-19
523次
整体难度:
容易
考查范围:
常见无机物及其应用、有机化学基础、化学与STSE、认识化学科学、物质结构与性质、化学反应原理、化学实验基础
一、单选题 添加题型下试题
| A.蔗糖、果糖和麦芽糖均为双糖 |
| B.商代后期铸造出工艺精湛的司母戊鼎,该鼎属于铜合金制品 |
| C.植物油含不饱和脂肪酸酯,能使Br₂/CCl4褪色 |
| D.汉代烧制出“明如镜、声如磬”的瓷器,其主要原料为黏土 |
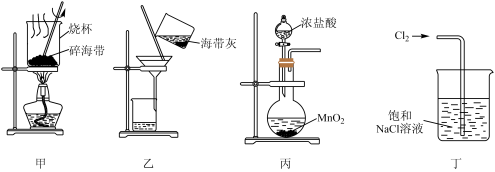
| A.用装置甲灼烧碎海带 |
| B.用装置乙过滤海带灰的浸泡液 |
| C.用装置丙制备用于氧化浸泡液中I−的Cl2 |
| D.用装置丁吸收氧化浸泡液中I−后的Cl2尾气 |
【知识点】 氯气的实验室制法解读 海带中碘的提取及检验解读
| A.16.25 g FeCl3水解形成的Fe(OH)3胶体粒子数为0.1NA |
| B.标准状况下,11.2 L甲烷和乙烯混合物中含氢原子数目为2NA |
| C.密闭容器中,2 mol SO2和1mol O2催化反应后分子总数为2NA |
| D.1.0 mol CH4与Cl2在光照下反应生成的CH3Cl分子数为1.0NA |
【知识点】 阿伏加德罗常数的求算解读
| A.溶解度:Na2CO3<NaHCO3 |
| B.热稳定性:HCl<PH3 |
| C.沸点:C2H5SH<C2H5OH |
| D.碱性:LiOH<Be(OH)2 |
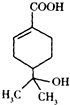
①分子式为C10H18O3
②易溶于水
③分子中含有两种官能团
④可使溴水和酸性高锰酸钾溶液褪色,且褪色原理相同
⑤能发生加成、取代、酯化、消去、催化氧化等反应
⑥所有的原子可能共平面
| A.①②③④⑤ | B.①②⑤⑥ | C.①②④⑤⑥ | D.全部不正确 |
【知识点】 有机官能团的性质及结构 多官能团有机物的结构与性质解读
| A.次氯酸的结构式H-Cl-O | B.CO2的比例模型 |
C.NH4Cl的电子式为: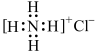 | D.Cl的原子结构示意图: |
| A.0.1 mol·L−1KI 溶液:Na+、K+、ClO− 、OH− |
| B.0.1 mol·L−1Fe2(SO4)3溶液:Cu2+、NH4+ 、NO3−、SO42− |
| C.0.1 mol·L−1HCl 溶液:Ba2+、K+、CH3COO−、NO3− |
| D.0.1 mol·L−1NaOH溶液:Mg2+、Na+、SO42−、HCO3− |
【知识点】 离子共存 限定条件下的离子共存解读
| A.正戊烷和正己烷 | B.新戊烷和2-甲基丙烷 |
| C.环戊烷和乙烷 | D.丙烷和2,3-二甲基丁烷 |
C(石墨) + O2(g) === CO2(g) ,燃烧1 mol C(石墨)放热393.51 kJ。
C(金刚石) + O2(g) === CO2(g),燃烧1 mol C(金刚石)放热395.41 kJ。
可以得出的结论是
| A.金刚石比石墨稳定 | B.1 mol石墨所具有的能量比1 mol金刚石低 |
| C.金刚石转变成石墨是物理变化 | D.石墨和金刚石都是碳的同位素 |
| A.铝片和镁片用导线连接后插入NaOH溶液中,镁片较活泼,作负极 |
| B.铁片和铜片用导线连接后插入浓硝酸中,铜作负极 |
| C.镀锌铁和镀锡铁的镀层破损后,前者较易被腐蚀 |
| D.将反应2Fe3++Fe=3Fe2+设计为原电池,则可用锌片作负极,铁片作正极,FeCl3溶液作电解质 |
【知识点】 原电池 金属的电化学腐蚀与防护 原电池概念及组成 原电池原理的应用
 2AlON+CO合成,下列有关说法合理的是
2AlON+CO合成,下列有关说法合理的是| A.上述反应中氮气作还原剂 |
| B.氮氧化铝中氮元素的化合价是-3 |
| C.氮氧化铝晶体中的作用力是范德华力 |
| D.根据氮氧化铝晶体的硬度可推断其晶体类型可能与石英相同 |
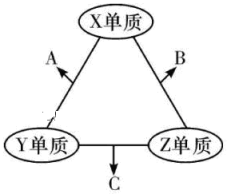
| A.X与Z形成的某种化合物可用来杀菌消毒 | B.C极易溶于B中,溶液呈碱性 |
| C.Y与Z形成的二元化合物只含有极性键 | D.A和C能发生氧化还原反应 |
【知识点】 “位构性”关系理解及应用解读
A.氯气通入水中,溶液呈酸性:Cl2 + H2O  2H+ + Cl+ClO 2H+ + Cl+ClO |
| B.AlCl3溶液中加入过量的浓氨水:Al3+ + 3NH3H2O = Al(OH)3 ↓ + 3NH4+ |
| C.钠和冷水反应:Na+2H2O=Na++2OH+H2↑ |
| D.向FeCl3溶液中加入铁粉:Fe3+ + Fe = 2Fe2+ |
【知识点】 离子方程式的正误判断解读
| 选项 | 气体 | 试剂 | 现象 | 结论 |
| A | SO2 | 氯水 | 溶液褪色 | SO2有漂白性 |
| B | NH3 | 酚酞溶液 | 溶液变为红色 | 氨水显碱性 |
| C | X | 澄清石灰水 | 溶液变浑浊 | X不一定是CO2 |
| D | Cl2 | 紫色石蕊试液 | 溶液先变红后褪色 | 氯水中含酸性和漂白性物质 |
| A.A | B.B | C.C | D.D |
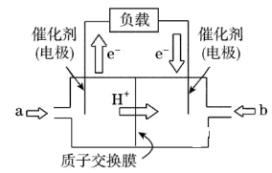
| A.左边的电极为电池的负极,a处通入的是甲醇 |
| B.每消耗3.2 g氧气转移的电子为0.4 mol |
| C.电池负极的反应式为CH3OH+H2O−6e−===CO2+6H+ |
| D.电池的正极反应式为O2+2H2O+4e−===4OH− |
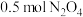 通入容积为5L的真空密闭容器中,立即出现红棕色。反应进行到2s时,
通入容积为5L的真空密闭容器中,立即出现红棕色。反应进行到2s时, 的浓度为
的浓度为 。60s时,反应已达到平衡状态,此时容器内的压强为开始时的1.6倍。下列说法正确的是
。60s时,反应已达到平衡状态,此时容器内的压强为开始时的1.6倍。下列说法正确的是A.0-2s内用 表示的反应速率为 表示的反应速率为 |
| B.在2s时容器内的压强为开始时的1.1倍 |
C.平衡时, |
D.平衡时, 的转化率为40% 的转化率为40% |
二、解答题 添加题型下试题

(1)若A、B、C均为含有同种非金属元素的化合物,A为使湿润的红色石蕊试纸变蓝的气体,B接触空气立刻变为C,则反应①的化学方程式为
(2)若A、B、C为焰色反应均呈黄色的化合物,X为无色无味气体,则反应②的离子方程式为
(3)若A、B、C均为含有同种金属元素的化合物,X是强碱,则反应②的离子方程式为
(4)若A为单质Fe,X为稀硝酸,若向B的溶液中加入氢氧化钠溶液,现象为
(5)若A和X均为单质,B为可使品红溶液褪色的气体,则反应②的化学方程式为

①以上实验中,体现SO2具有氧化性的实验现象为
② D装置的作用是
③ A中反应开始后,试管B中始终无明显现象。现将试管B中溶液分成两份,分别滴加一定量的氯水和氨水,均出现白色沉淀,任选其中一个实验,结合
(2)硫酸工厂的烟气中含有SO2,有多种方法可实现烟气脱硫。
① “钠碱法”用NaOH溶液作吸收剂,向 100 mL 0.3 mol·L-1的NaOH溶液中通入标准状况下0.448 L SO2气体,所得溶液中的溶质是
② 某硫酸厂拟用含Cr2O72的酸性废水处理烟气中SO2,反应后的铬元素以Cr3+形式存在,则反应中氧化剂和还原剂的物质的量之比是
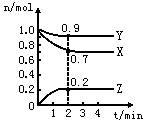
(1)由图中所给数据进行分析,该反应的化学方程式为
(2)反应从开始至2分钟,用Z的浓度变化表示的平均反应速率为V(Z)=
(3)2min反应达平衡,容器内混合气体的平均相对分子质量比起始时
(4)将amolx与bmolY的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n(X)=n(Y)=n(Z),则原混合气体中a:b=
(5)下列措施能加快反应速率的是
A.恒压时充入He; B.恒容时充入He; C.恒容时充入X; D.及时分离出Z;E.升高温度; F.选择高效的催化剂
(6)下列说法正确的是
A.升高温度改变化学反应的限度
B.已知正反应是吸热反应,升高温度平衡向右移动,正反应速率加快,逆反应速率减慢
C.化学反应的限度与时间长短无关
D.化学反应的限度是不可能改变的
E.增大Y的浓度,正反应速率加快,逆反应速率加快,正反应速率大于逆反应速率
F.加入高效催化剂可加快正、逆反应速率,化学平衡正向移动
【知识点】 化学反应速率计算解读 化学平衡的有关计算 化学平衡状态的判断方法解读

(1)操作Ⅰ的名称为
(2)加入试剂C的目的是将Cu2+全部转化为Cu,以便回收铜单质,发生的离子方程式为
(3)操作Ⅲ为加热浓缩、
(4)由于硫酸亚铁溶液露置于空气中容易变质,请设计一个简单的实验方案验证硫酸亚铁是否变质?(请写出必要的实验步骤、现象和结论)
【知识点】 铁 亚铁盐 铜 物质分离、提纯综合应用解读
(1)A 的电子式为
(2)与A 相邻的同系物C使溴的四氯化碳溶液褪色的化学反应方程式:
(3)在碘水中加入B物质,充分振荡、静置后的现象:
(4)B与浓硫酸和浓硝酸在55~60℃条件下反应的化学方程式:
(5)等质量的A、B完全燃烧时消耗O2的物质的量:
试卷分析
试卷题型(共 21题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 硅酸盐 油脂 蔗糖与麦芽糖 常见合金的组成 | |
| 2 | 0.65 | 氯气的实验室制法 海带中碘的提取及检验 | |
| 3 | 0.85 | 阿伏加德罗常数的求算 | |
| 4 | 0.65 | 碳酸钠与碳酸氢钠性质的比较 同周期元素性质递变规律 元素非金属性强弱的比较方法 | |
| 5 | 0.85 | 有机官能团的性质及结构 多官能团有机物的结构与性质 | |
| 6 | 0.65 | 原子结构示意图、离子结构示意图 共价型分子结构式、电子式 原子、离子、原子团及其电子式的书写与判断 | |
| 7 | 0.65 | 离子共存 限定条件下的离子共存 | |
| 8 | 0.85 | 简单有机物同分异构体书写及辨识 同分异构体的数目的确定 | |
| 9 | 0.85 | 化学反应中能量变化的原因 化学能与物质稳定性之间的关系 几组常见同素异形体 | |
| 10 | 0.65 | 原电池 金属的电化学腐蚀与防护 原电池概念及组成 原电池原理的应用 | |
| 11 | 0.65 | 氧化还原反应的几组概念 范德华力对物质性质的影响 原子晶体(旧教材) | |
| 12 | 0.4 | “位构性”关系理解及应用 | |
| 13 | 0.65 | 离子方程式的正误判断 | |
| 14 | 0.65 | 铵根离子的检验 二氧化硫的化学性质 | |
| 15 | 0.65 | 原电池原理理解 原电池电子流向判断及应用 原电池正负极判断 原电池电极反应式书写 | |
| 16 | 0.65 | 化学平衡的有关计算 化学平衡建立的过程 | |
| 二、解答题 | |||
| 17 | 0.65 | 无机综合推断 氨的还原性 铝三角转化 铁的其他化合物 | 无机推断题 |
| 18 | 0.65 | 物质制备的探究 综合实验设计与评价 | 实验探究题 |
| 19 | 0.65 | 化学反应速率计算 化学平衡的有关计算 化学平衡状态的判断方法 | 原理综合题 |
| 20 | 0.85 | 铁 亚铁盐 铜 物质分离、提纯综合应用 | 实验探究题 |
| 21 | 0.85 | 乙烯的加成反应 苯的取代反应 烃燃烧产物的量和烃的组成关系 | 无机推断题 |



