内蒙古巴彦淖尔市乌拉特前旗第一中学2020-2021学年高二下学期期末考试化学试题
内蒙古
高二
期末
2021-07-29
273次
整体难度:
适中
考查范围:
常见无机物及其应用、有机化学基础、物质结构与性质、化学与STSE、化学实验基础、认识化学科学、化学反应原理
内蒙古巴彦淖尔市乌拉特前旗第一中学2020-2021学年高二下学期期末考试化学试题
内蒙古
高二
期末
2021-07-29
273次
整体难度:
适中
考查范围:
常见无机物及其应用、有机化学基础、物质结构与性质、化学与STSE、化学实验基础、认识化学科学、化学反应原理
一、单选题 添加题型下试题
单选题
|
较易(0.85)
1. 化学与生活密切相关。下列叙述错误的是( )
| A.高纯硅可用于制作光感电池 | B.铝合金大量用于高铁建设 |
| C.活性炭具有除异味和杀菌作用 | D.冬季燃煤中掺石灰可降低SO2排放 |
您最近一年使用:0次
2019-12-06更新
|
489次组卷
|
4卷引用:陕西省咸阳市武功县2020届高三上学期第一次模拟考试化学试题
单选题
|
较易(0.85)
2. 国家卫健委公布的新型冠状病毒肺炎诊疗方案指出,乙醚、75%乙醇、含氯消毒剂、过氧乙酸(CH3COOOH)、氯仿等均可有效灭活病毒。对于上述化学药品,下列说法错误的是
| A.CH3CH2OH能与水互溶 |
| B.NaClO通过氧化灭活病毒 |
| C.过氧乙酸相对分子质量为76 |
| D.氯仿的化学名称是四氯化碳 |
您最近一年使用:0次
2020-07-08更新
|
19924次组卷
|
65卷引用:2020年全国统一考试化学试题(新课标Ⅰ)
2020年全国统一考试化学试题(新课标Ⅰ)贵州省铜仁市伟才学校2019-2020学年高一下学期期末考试化学(理)试题甘肃省会宁县第四中学2019-2020学年高二下学期期末考试化学试题(已下线)专题12 有机化合物-2020年高考真题和模拟题化学分项汇编江苏省扬州市扬州中学2021届高三开学检测化学试题辽宁省大连市辽宁师范大学附属中学2019-2020学年高一下学期期末考试化学试题河南省三门峡市第一高级中学2021届高三8月开学考试化学试题(已下线)小题必刷18 氯及其化合物——2021年高考化学一轮复习小题必刷(通用版)山东省泰安市第一实验学校2021届高三10月月考化学试题上海市七宝中学2021届高三上学期期中考试化学试题(已下线)热点1 化学与STSE-2021年高考化学专练【热点·重点·难点】江西省南昌市新建区第二中学2019-2020学年高二下学期期终考试化学试题(已下线)热点1 化学与STSE-2021年高考化学【热点·重点·难点】专练(山东专用)黑龙江省哈尔滨市第三十二中学2021届高三上学期期末考试化学试题 人教版2019必修第二册 第七章 第三~四节综合拔高练(已下线)专题09 常见有机物及其应用——备战2021年高考化学纠错笔记(已下线)小题02 化学与社会生产生活环境(STSE)——备战2021年高考化学经典小题考前必刷(全国通用)上海市行知中学2021届高三下学期3月月考化学试题(已下线)【苏州新东方】2020年10月江苏省苏州市高新区第一中学高二化学独立作业新疆乌鲁木齐市第八中学2020-2021学年高一下学期第一阶段考试化学试题(已下线)押全国卷理综第7题 化学与社会生产生活-备战2021年高考化学临考题号押题(课标全国卷)吉林省长春外国语学校2020-2021学年高一下学期期中考试化学(理科)试题河南省安阳市洹北中学2020-2021学年高二下学期第一次月考化学试题贵州省遵义市务川县汇佳中学2020-2021学年高二下学期第三次月考化学试题(苏教版2019)必修第二册专题8 有机化合物的获得与应用 C 高考挑战区山西省太原市2020-2021学年高一下学期期末考试化学试题西藏自治区拉萨那曲第二高级中学2020-2021学年高二下学期期末考试化学试题内蒙古巴彦淖尔市乌拉特前旗第一中学2020-2021学年高二下学期期末考试化学试题(已下线)课时01 化学与生产、生活和环境-2022年高考化学一轮复习小题多维练(全国通用)内蒙古集宁新世纪中学2020-2021学年高二下学期期末考试化学试题(已下线)考向11 氯及其化合物-备战2022年高考化学一轮复习考点微专题吉林省抚松县泉阳镇抚松县第六中学2021-2022学年高二上学期化学与生活知识竞赛化学试题吉林省吉林市第二中学2020-2021学年高二下学期期中考试化学试卷江苏省常州市武进区礼嘉中学2021-2022学年高二上学期第一阶段教学质量调研化学试卷题(已下线)专题讲座(七) STSE与 化学可持续发展(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)考向30 烃的含氧衍生物-备战2022年高考化学一轮复习考点微专题(已下线)专题01 化学与STSE—2022年高考化学二轮复习讲练测-练习陕西省渭滨中学2021-2022学年高一上学期期中考试化学试题2020年全国卷Ⅰ理综化学高考真题变式题云南省峨山彝族自治县第一中学2021-2022学年高二上学期12月月考化学试题吉林省长春市实验中学2021-2022学年高二下学期4月月考化学试题(已下线)押全国卷理综第7题 化学与社会生产生活及传统文化-备战2022年高考化学临考题号押题(课标全国卷)(已下线)回归教材重难点01 化学与STSE与传统文化-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)查补易混易错点01 物质的组成、性质、分类及化学用语-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题01STSE化学用语-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题01STSE化学用语-五年(2018~2022)高考真题汇编(全国卷)(已下线)第01练 化学与科技社会生产生活、传统文化-2022年【暑假分层作业】高二化学(2023届一轮复习通用)山东省菏泽市鄄城县第一中学2021-2022学年高二下学期第二次月考化学试题黑龙江省双鸭山市集贤县一中、四中等2021-2022学年高二下学期期末考试化学试题专题4 生活中常用的有机物——烃的含氧衍生物 第一~二单元综合拔高练青海省西宁市七校2021-2022年高二下学期期末联考化学试题广东省揭阳华侨高级中学2021-2022学年高三上学期第三次阶段考试化学试题四川省邻水实验学校2021-2022学年高二下学期第二次月考理综化学试题云南省富源县第一中学2021-2022学年高二下学期3月月考化学试题黑龙江省双鸭山市饶河县高级中学2021-2022学年高二下学期期中考试化学试题(已下线)专题01 物质的组成与分类 传统文化-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第一部分 二轮专题突破 专题19 有机选择题题型分析(已下线)题型47 新型消毒剂的制备及用途江苏省苏州市苏州高新区第一中学2022-2023学年高一下学期5月月考化学试题4.1.1醇的性质和应用 课中广东省肇庆市第一中学2020--2021学年高二下学期期中考试化学试题河南省南阳市第一中学校2022-2023学年高二下学期4月月考化学试题(已下线)实验05 探究氯气的性质-【同步实验课】2023-2024学年高一化学教材实验大盘点(人教版2019必修第一册)云南省开远市第一中学校2023-2024学年高二上学期10月月考化学试题宁夏石嘴山市平罗中学2023-2024学年高二上学期第三次月考化学试题
单选题
|
适中(0.65)
真题
名校
3. 下列有关从海带中提取碘的实验原理和装置能达到实验目的的是
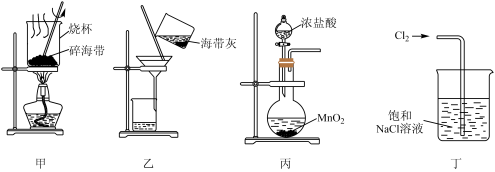

| A.用装置甲灼烧碎海带 |
| B.用装置乙过滤海带灰的浸泡液 |
| C.用装置丙制备用于氧化浸泡液中I−的Cl2 |
| D.用装置丁吸收氧化浸泡液中I−后的Cl2尾气 |
【知识点】 氯气的实验室制法解读 海带中碘的提取及检验解读
您最近一年使用:0次
2018-06-10更新
|
11754次组卷
|
84卷引用:2018年全国普通高等学校招生统一考试化学(江苏卷)
2018年全国普通高等学校招生统一考试化学(江苏卷)【全国百强校】山西省临汾第一中学2017-2018学年高二下学期期末考试化学试题黑龙江省青冈县一中2017-2018学年高一下学期期末考试化学试题江西省南昌三中2019届高二下期末考试 化学(已下线)2018年高考题及模拟题汇编 专题11 化学实验基础【全国百强校】黑龙江省哈尔滨市第三中学2017-2018学年高二下学期期末考试化学试题江苏省盐城市田家炳中学2019届高三上学期开学考试化学试题陕西省城固县第一中学2019届高三上学期第一次月考化学试题辽宁省沈阳市东北育才学校2019届高三上学期第一次模拟考试化学试题湖北省汉川市第二中学2017-2018学年高一下学期期末考试化学试题甘肃省师范大学附属中学2019届高三上学期第一次月考化学试题辽宁省葫芦岛协作校2019届高三上学期第一次月考化学试题甘肃省武威市第二中学2019届高三上学期第二次(10月)月考化学试题【全国百强校】山西省山西大学附属中学2018-2019学年高二上学期9月模块诊断化学试题云南省腾冲市第八中学2018-2019学年高二上学期期中考试化学试题【全国百强校】甘肃省平凉市静宁县第一中学2019届高三上学期第三次模拟考试化学试题江苏师范大学附属实验学校2019届高三上学期10月学情调研化学试题河南省郑州市实验中学2019届高三上学期期中考试化学试题【全国百强校】山东省山东师范大学附属中学2019届高三上学期第五次模拟考试化学试题山西省长治二中2018-2019学年高一下学期第一次月考化学试题【市级联考】陕西省榆林市2019届高三下学期高考模拟第三次测试理科综合化学试题吉林省长春汽车经济开发区第三中学2018-2019学年高一下学期4月月考化学试题(已下线)2019年5月20日 《每日一题》 必修2 海带提碘步步为赢 高一化学暑假作业:作业十六 开发利用金属矿物和海水资源【全国百强校】吉林省延边第二中学2018-2019学年高二下学期第二次月考化学试题黑龙江省大庆市第四中学2018-2019学年高一下学期第三次月考化学试题四川省武胜县烈面中学校2018届高三9月入学考试化学试题湖北省利川市第三中学2019届高三一模化学试题江西省宜春市万载中学2019-2020学年高二上学期期中考试化学试题(衔接班)(已下线)专题10.2 物质的分离、提纯、检验与鉴别(练)-《2020年高考一轮复习讲练测》(已下线)专题10.2 物质的分离、提纯、检验与鉴别(讲)-《2020年高考一轮复习讲练测》河南省南阳市2020届高三上学期期中质量评估化学试题(已下线)考点20 化学基础实验——《备战2020年高考精选考点专项突破题集》福建省莆田第二十五中学2020届高三上学期期末考试化学试题2020届人教版高中化学高三专题基础复习专题1《从实验学化学》测试卷上海市宝山区2020届高三上学期第一次模拟考试(等级考)化学试题广东省2020年普通高中学业水平考试化学合格性考试模拟试题(五)新疆阿克苏市阿瓦提四中2020届高三上学期第二次月考化学试题(已下线)专题3.6 金属材料和无机非金属材料 海水的开发利用 -巅峰冲刺山东省2020年高考化学一轮考点扫描《2020年新高考政策解读与配套资源》江苏省南通市启东市吕四中学2020届高三第一次质量检测化学试题四川省广安市邻水县四川省邻水中学2019-2020学年高一下学期期中考试化学试题(已下线)第02讲 物质的分离和提纯(精讲)——2021年高考化学一轮复习讲练测四川省成都市龙泉中学2021届高三上学期开学考试化学试题(已下线)第6单元 常见的非金属元素(B卷 滚动提升检测)-2021年高考化学一轮复习单元滚动双测卷(已下线)小题必刷18 氯及其化合物——2021年高考化学一轮复习小题必刷(通用版)鲁科版(2019)高一必修第二册 第1章 原子结构 元素周期律微项目 海带提碘与海水提溴高一必修第二册(人教2019版)第八章 化学与可持续发展 素养检测高一必修第一册(苏教2019版)专题3 C 高考挑战区 过模拟 2年模拟精编精练江苏省扬州市江都区大桥高级中学2021届高三上学期期初调研化学试题高一必修第一册(苏教2019)专题3 第三单元 海洋化学资源的综合利用3江苏省邗江中学2020-2021学年高一上学期期中考试化学试题山东师范大学附属中学2021届高三上学期期中考试(11月)化学试题山西省实验中学2019届高三上学期第四次月考化学试题江苏省泰州中学2021届高三上学期第二次月考化学试题专题3 第三单元综合拔高练-高中化学苏教2019版必修第一册(人教版2019)必修第二册 第八章 化学与可持续发展 第一节 自然资源的开发利用云南省普洱市景东县第一中学2021届高三上学期期末考试化学试题(已下线)解密11 化学实验(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密11 化学实验(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)重庆市永川景圣中学2020-2021学年高三上学期第二次月考化学试题吉林省通化县综合高级中学2020-2021学年高一下学期期末考试化学试题内蒙古巴彦淖尔市乌拉特前旗第一中学2020-2021学年高二下学期期末考试化学试题(已下线)考点30 物质的分离、提纯和检验-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点30 物质的分离、提纯和检验-备战2022年高考化学一轮复习考点帮(浙江专用)内蒙古包头市2022届高三上学期起点调研考试化学试题(已下线)课时52 物质的分离、提纯和检验-2022年高考化学一轮复习小题多维练(全国通用)重庆市开州中学高 2021-2022学年高三上学期10月月考化学试题湖北省武汉市蔡甸区实验高级中学2020-2021学年高二上学期10月联合考试化学试题福建省厦门市湖滨中学2021-2022学年高三上学期期中考试化学试题山东省济南市莱芜第一中学2021-2022学年高三上学期期中考试化学试题福建省厦门市翔安第一中学2021-2022学年高一下学期第一次月考(3月)化学试题湖南省浏阳市第一中学2022届高三下学期期中考试化学试题云南省昭通市永善、绥江县2021-2022学年高一上学期期末考试化学试题山东省菏泽市单县第五中学2021-2022学年高一下学期第一次段考化学(A)试题新疆叶城县第八中学2021-2022学年高三上学期第二次月考化学试题贵州省贵阳市2022-2023学年高三上学期10月质量监测化学试题四川省广安市育才学校2022-2023学年高一上学期9月月考化学试题江苏省扬州中学2022-2023学年高一上学期期中检测化学试题湖南省长沙市同升湖实验学校2022-2023学年高三上学期第三次月考化学试题广东省揭阳市惠来县第一中学2022-2023学年高二上学期期中考试化学试题第四章 非金属及其化合物 第19讲 卤素的性质及提取(已下线)题型46 从海水中提取氯、溴、碘广东省广州市越秀区2023-2024学年高二上学期开学考试化学试题河南省焦作第一中学2023-2024学年高三上学期9月化学模拟测试
单选题
|
适中(0.65)
名校
解题方法
4. 某同学用下图装置证明过氧化钠可做呼吸面具中的供氧剂,下列说法不正确 的是


| A.装置B中盛放的液体为浓硫酸 |
| B.装置C发生的反应中,Na2O2既是氧化剂又是还原剂 |
| C.装置D中NaOH溶液的作用是除去多余的CO2 |
| D.将E中试管收集的气体可使带有火星的木条复燃 |
您最近一年使用:0次
2021-06-13更新
|
1043次组卷
|
11卷引用:浙江省温州市2020-2021学年高一下学期期末教学质量统一监测(学考模拟)化学试题
浙江省温州市2020-2021学年高一下学期期末教学质量统一监测(学考模拟)化学试题新疆哈密市第十五中学2020-2021学年高一下学期期末考试化学试题内蒙古巴彦淖尔市乌拉特前旗第一中学2020-2021学年高二下学期期末考试化学试题(已下线)考点13 钠及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点13 钠及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)周末培优2 有关钠和氯的实验题-2021-2022学年高一化学课后培优练(人教版2019必修第一册)安徽省池州市第一中学2021-2022学年高一上学期12月月考化学试题河北省武安市第一中学2021-2022学年高三上学期第五次调研考试化学试题(已下线)考点13 钠及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)【2022】【高一上】【分班考】【67】内蒙古赤峰市红山区2022-2023学年高一上学期期末质量检测化学试题
单选题
|
适中(0.65)
解题方法
5. 下列各组物质中,X是主体物质,Y是少量杂质,Z是为除去杂质所要加入的试剂,其中所加试剂正确的一组是
| 选项 | A | B | C | D |
| X | FeCl2溶液 | FeCl3溶液 | Fe | NaHCO3 |
| Y | FeCl3 | CuCl2 | Al | Na2CO3 |
| Z | Cl2 | Fe | NaOH溶液 | 适量盐酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-04-08更新
|
208次组卷
|
2卷引用:甘肃兰州市第二十七中学2020-2021学年高一上学期期末考试化学试题
单选题
|
适中(0.65)
解题方法
6. 下列反应的离子方程式书写正确的是( )
| A.向CuSO4溶液中通入H2S气体:Cu2++S2-=CuS↓ |
| B.将磁性氧化铁溶于盐酸中:Fe3O4+8H+=3Fe3++4H2O |
C.1 mol·L-1NaAlO2溶液和2.5 mol·L-1HCl溶液等体积混合:2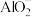 +5H+= Al(OH)3↓+Al3++ H2O +5H+= Al(OH)3↓+Al3++ H2O |
| D.Fe(OH)3和HI的反应:Fe(OH)3+3H+=Fe3++3H2O |
您最近一年使用:0次
2021-02-02更新
|
138次组卷
|
2卷引用:四川省巴中中学、南江中学2020-2021学年高一上学期期末联考化学试题
单选题
|
适中(0.65)
解题方法
7. 为探究铜与浓硫酸反应的还原产物,某化学兴趣小组进行如图实验,实验装置如图所示。(固定装置已略去),下列说法正确的是
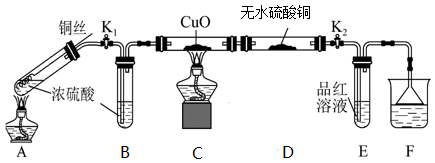

| A.A和B中的浓硫酸都体现了强氧化性 |
| B.若D中无现象,E中品红溶液颜色变浅,则证明浓硫酸的还原产物是SO2不是H2 |
| C.实验结束时,应先熄灭A处酒精灯 |
| D.F中可用氢氧化钠溶液或高锰酸钾溶液吸收尾气,均发生了氧化还原反应 |
您最近一年使用:0次
2021-07-02更新
|
474次组卷
|
3卷引用:河北省五校联盟2020-2021学年高二下学期期末考试(新高三模拟)化学试题
单选题
|
较难(0.4)
解题方法
8. 下列有关S和 的叙述正确的是
的叙述正确的是
 的叙述正确的是
的叙述正确的是A.硫粉在过量的氧气中燃烧可以生成 |
B.空气吹出法提取海水中的溴常用 作氧化剂 作氧化剂 |
C.将 通入 通入 溶液能生成白色沉淀 溶液能生成白色沉淀 |
D. 具有漂白性,所以能使品红溶液和高锰酸钾酸性溶液褪色 具有漂白性,所以能使品红溶液和高锰酸钾酸性溶液褪色 |
您最近一年使用:0次
2020-08-11更新
|
689次组卷
|
3卷引用:山东省聊城市2019-2020学年高一下学期期末考试化学试题
单选题
|
容易(0.94)
解题方法
9. 打赢蓝天保卫战,提高空气质量。下列物质不属于空气污染物的是
| A.PM2.5 | B. | C. | D.NO |
您最近一年使用:0次
2021-01-24更新
|
129次组卷
|
4卷引用:福建省宁德市2020-2021学年高一上学期期末考试化学试题
单选题
|
适中(0.65)
名校
解题方法
10. 检验二氧化硫中是否混有二氧化碳气体,可采用的方法是
| A.通过品红溶液 |
| B.先通过氢氧化钠溶液,再通过澄清石灰水 |
| C.通过澄清石灰水 |
| D.先通过酸性高锰酸钾溶液,再通过澄清石灰水 |
您最近一年使用:0次
2022-03-18更新
|
984次组卷
|
47卷引用:2010-2011学年福建省福州八中高一下学期期中考试化学试卷
(已下线)2010-2011学年福建省福州八中高一下学期期中考试化学试卷(已下线)2013-2014学年江西赣州市四所重点中学高一上学期期末联考化学试卷2014-2015四川省雅安中学高一4月月考化学试卷2015-2016学年广西南宁市上林中学高一上学期期末化学试卷江西省上饶县中学2016-2017学年高一下学期期末考试化学试题甘肃省嘉峪关市一中2017-2018学年高一上学期期末考试化学试题甘肃省武威市第六中学2017-2018学年高一下学期第一次学段考试(理)化学试题【全国百强校】青海省平安县第一高级中学2017-2018学年高一下学期期中考试(A卷)化学试题黑龙江省伊春市第二中学2018-2019学年高一(理)上学期期末考试化学试题陕西省黄陵中学2018-2019学年高一上学期期末考试化学试题浙江省温州市新力量联盟2018-2019学年高一上学期期末考试化学试题河北省雄安新区博奥高级中学2019-2020学年高二上学期开学考试化学试题云南省通海三中2019-2020学年高二上学期期末考试化学试题江苏省盐城市大丰区新丰中学2019-2020学年高一上学期期末考试化学试题鲁教版高中化学必修1第三章《自然界中的元素》测试卷2人教版高一化学必修1第四章《非金属及其化合物》测试卷人教版高中化学必修1第四章《非金属及其化合物》测试卷5贵州省独山县第四中学2019-2020学年高一上学期期末考试化学试题安徽省六安市第一中学2019-2020学年高一下学期延期开学期间辅导作业专题卷(一)化学试题四川省内江市第六中学2019-2020学年高一下学期期中考试化学试题西藏自治区日喀则市南木林高级中学2019-2020学年高一下学期期中考试化学试题四川省棠湖中学2019-2020学年高一下学期第四学月考试化学试题甘肃省兰州市第一中学2020-2021学年高一上学期期末考试化学(文)试题黑龙江伊春林业管理局第二中学2021届高三上学期期中考试化学试题山东省济南市章丘市第一中学2020-2021学年高一上学期12月月考化学试题专题4 第一单元 第1课时二氧化硫的性质和应用-高中化学苏教2019版必修第一册江苏省苏州市苏州大学附属中学2020-2021学年高一上学期月考化学试卷2广东省佛山市顺德李兆基中学2020-2021学年高一3月月考化学试卷江苏省苏州市园区苏州大学附属中学2020-2021学年高一上学期12月月考化学试题黑龙江省哈尔滨市阿城区龙涤中学2020-2021学年高一4月月考化学试题黑龙江省哈尔滨市第一六二中学校2020-2021学年高一下学期4月月考化学试题福建省莆田第七中学2020-2021学年高一下学期期中考试化学试题四川凉山州西昌天立学校2020-2021学年高一下学期第一次月化学试题云南省梁河县第一中学2020-2021学年高一下学期第一次月考化学试题内蒙古巴彦淖尔市乌拉特前旗第一中学2020-2021学年高二下学期期末考试化学试题山西省名校2021-2022学年高一上学期期末考试化学试题四川省达州市第一中学校高2021-2022学年高一下学期入学考试 化学试题河南省新乡市原阳县第一高级中学南街分校2021-2022学年高三上学期12月月考化学试题 上海市西南位育中学2021-2022学年高二下学期期末自测(合格考)化学试题课前-3.2.1自然界中的硫 二氧化硫(课前)-鲁科版2019必修第一册新疆哈密市第十五中学2021-2022学年高一下学期3月月考试卷化学试题河南省周口经济开发区黄泛区高级中学2021-2022学年高一下学期第一次月考化学试题福建省厦门市大同中学2022-2023学年高一上学期第二次月考化学试卷吉林省白城市第十四中学2022届高三上学期期中考试化学试题新疆兵团第三师图木舒克市鸿德实验学校2022-2023学年高一下学期第一次月考化学试题广东实验中学越秀学校2023-2024学年高一3月段考化学试题天津市静海区第一中学2023-2024学年高一下学期3月月考化学试题
单选题
|
较易(0.85)
解题方法
11. 下列说法正确的是
| A.工业上通过电解氯化钠溶液制备金属钠和氯气 |
| B.钢铁厂用热还原法冶炼铁 |
| C.工业上电解熔融状态的Al2O3制备Al不涉及氧化还原反应 |
| D.海水提镁的大致流程:MgCl2(aq)→Mg(OH)2→MgO→Mg |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
12. 含硫煤燃烧会产生大气污染物,为防治该污染,某工厂设计了新的治污方法,同时可得到化工产品,该工艺流程如图所示,下列叙述不正确的是
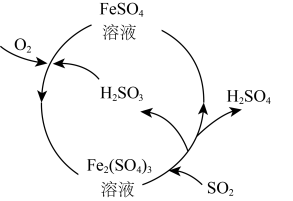

A.该过程中可得到化工产品 |
B.该工艺流程是除去煤燃烧时产生的 |
| C.该过程中化合价发生改变的元素只有O和S |
D.图中涉及的反应之一为: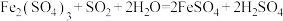 |
您最近一年使用:0次
2021-05-14更新
|
1203次组卷
|
39卷引用:2016-2017学年黑龙江大庆实验中学高一上开学考化学卷
2016-2017学年黑龙江大庆实验中学高一上开学考化学卷2017届湖南省雅礼中学高三上月考二化学试卷甘肃省武威市第六中学2019届高三上学期第二次阶段性复习过关考试化学试题【校级联考】湖南省岳阳县第一中学、汨罗市一中2018-2019学年高一上学期期末考试化学试题(已下线)考点06 典型的非金属元素及其化合物——《备战2020年高考精选考点专项突破题集》步步为赢 高一化学寒假作业:作业十六 阶段检测(四)(已下线)《2020年新高考政策解读与配套资源》模拟试题02-2020年北京新高考化学模拟试题(已下线)专题3.4 硫及其化合物 -巅峰冲刺山东省2020年高考化学一轮考点扫描《2020年新高考政策解读与配套资源》(已下线)专题01 硫及其化合物(核心精讲)-【新教材精创】2019-2020学年高一化学新教材知识讲学(必修第二册)江苏省扬州中学2019-2020学年高二下学期期中考试化学试题辽宁省营口市第二高级中学2019-2020学年高一下学期期末考试化学(理)试题(已下线)第15讲 硫及其化合物(精讲)——2021年高考化学一轮复习讲练测江苏省淮阴中学2021届高三上学期开学练习化学试题高一必修第二册(人教2019版)第五章 第一节 硫及其化合物 课时3 不同价态含硫物质的转化山西省临猗县临晋中学2020-2021学年高一9月月考化学试题浙江省金华市曙光学校2020-2021学年高一上学期第一阶段考试化学试题广东省汕头市金山中学2020-2021学年高一上学期10月月考化学试题安徽省怀宁中学2020-2021学年高一上学期第一次质量检测化学试题安徽师范大学附属中学2020-2021学年高一上学期期中考试化学试题重庆市第八中学2020-2021学年高一上学期第一次月考化学试题山东省济南市章丘市第一中学2020-2021学年高一上学期12月月考化学试题人教版2019必修第二册 第五章 第二节 第3课时 硝酸 酸雨及防治山东省济南市历城第一中学2021届高三上学期10月月考化学试题广东省广州市番禺区洛溪新城中学2020-2021学年高一下学4月月考化学试题山东省济宁市泗水县2020-2021学年高一下学期期中考试化学试题河北饶阳中学2020-2021学年高一下学期第一次月考(实验部)化学试题内蒙古巴彦淖尔市乌拉特前旗第一中学2020-2021学年高二下学期期末考试化学试题广东省惠州市惠城区2021--2022学年高三上学期8月开学摸底化学试题(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第11讲 硫及其化合物(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)考向12 硫及其化合物-备战2022年高考化学一轮复习考点微专题安徽省蚌埠第三中学2021-2022学年高一下学期开学测试化学试题湖南师范大学附属中学2020-2021学年高一下学期期末考试化学试题北京市中国人民大学附属中学丰台学校2022届高三上学期期中考试化学试题山东省淄博市桓台第二中学2021-2022学年高三上学期期中考试化学试题(已下线)河北省石家庄市2022届高三毕业班教学质量检测二(一模)(不定项选择题)宁夏育才中学2022-2023学年高一下学期3月月考化学试题天津市第二十一中学2023-2024学年高三上学期期中质量检测化学试题
单选题
|
适中(0.65)
13. 已知BrCl能发生下列反应(M为+n价的金属元素):
nBrCl + 2M =MCln+ MBrn,BrCl + H2O =HCl + HBrO
以下结论不正确的是:
nBrCl + 2M =MCln+ MBrn,BrCl + H2O =HCl + HBrO
以下结论不正确的是:
| A.BrCl具有和卤素单质相似的化学性质 |
| B.BrCl与M反应时,BrCl只作氧化剂 |
| C.BrCl与NaOH溶液反应生成NaCl和NaBrO两种盐 |
| D.BrCl与H2O的反应中,BrCl既作氧化剂又作还原剂 |
您最近一年使用:0次
2016-12-09更新
|
1070次组卷
|
3卷引用:2012-2013学年广东佛山佛山一中高一下学期第一次段考化学试卷
(已下线)2012-2013学年广东佛山佛山一中高一下学期第一次段考化学试卷夯基提能2020届高三化学选择题对题专练——常见无机物及其性质应用——卤素互化物、拟卤素(基础过关)内蒙古巴彦淖尔市乌拉特前旗第一中学2020-2021学年高二下学期期末考试化学试题
单选题
|
较易(0.85)
名校
14. 下列关于焰色反应的说法正确的是
| A.用洁净铂丝蘸取溶液进行焰色反应,火焰呈黄色,则原溶液中有Na+,无K+ |
| B.用NaOH溶液洗涤并灼烧铂丝后,再进行焰色反应 |
| C.进行钠的焰色反应实验,可用到的实验用品有:铂丝、氯化钠溶液、稀盐酸 |
| D.焰色反应是某些金属单质具有的性质 |
您最近一年使用:0次
2017-08-24更新
|
453次组卷
|
4卷引用:山西省忻州市第一中学2016-2017学年高一必修一:3.2.1几种重要的金属化合物同步练习化学试题
单选题
|
适中(0.65)
名校
15. 下列除去杂质的方法不正确的是( )
| A.镁粉中混有少量铝粉:加入过量烧碱溶液充分反应,过滤、洗涤、干燥 |
| B.用过量氨水除去Fe3+溶液中的少量Al3+ |
| C.Al(OH)3中混有少量Mg(OH)2:加入足量烧碱溶液,充分反应,过滤,向滤液中通入过量CO2后过滤 |
| D.MgO中混有少量Al2O3:加入足量烧碱溶液,充分反应,过滤、洗涤、干燥得到MgO |
您最近一年使用:0次
2018-09-14更新
|
941次组卷
|
16卷引用:2019高考备考一轮复习精品资料 第三章 金属及其化合物 第2讲 镁、铝及其重要化合物【教学案】
(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第2讲 镁、铝及其重要化合物【教学案】【全国百强校】陕西省西安中学2019届高三上学期期中考试化学试题宁夏回族自治区石嘴山市平罗中学2020届高三上学期期中考试化学试题陕西省咸阳百灵中学2020届高三上学期期中考试化学试题内蒙古包头市包钢第四中学2018-2019学年高二下学期期末考试化学试题广东省湛江市第二十一中学2019-2020学年高一下学期开学考试化学试题新疆吾尔自治区乌鲁木齐市第七十中学、哈密二中2019-2020学年高二下学期期末考试化学试题(已下线)【浙江新东方】48陕西省汉中市洋县中学2019--2020学年高一上学期期中考试化学试题内蒙古巴彦淖尔市乌拉特前旗第一中学2020-2021学年高二下学期期末考试化学试题(已下线)课时16 铝及其化合物-2022年高考化学一轮复习小题多维练(全国通用)江苏省苏州市相城区陆慕高级中学2021-2022学年高一下学期4月线上教学质量检测化学试题(已下线)第08讲 金属材料(练)-2023年高考化学一轮复习讲练测(新教材新高考)新疆维吾尔自治区喀什第二中学2021-2022学年高三上学期10月月考化学试题黑龙江省哈尔滨市第十九中学2021-2022学年高三上学期第一次月考化学试题(已下线)考点11 镁、铝及其重要化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
16. 减少向大气中排放硫的氧化物是防治酸雨的重要方法,下列防治方法不合理的是
| A.用消石灰浆液作洗涤剂,吸收火力发电厂烟气中的SO2 |
| B.原煤混入少量石灰石,可减少原煤燃烧排放的SO2 |
| C.用氨水吸收硫酸厂尾气中的SO2,还可得副产品亚硫酸铵 |
| D.寻找高效催化剂,加快汽车尾气中的SO2的氧化 |
您最近一年使用:0次
2020-10-24更新
|
205次组卷
|
3卷引用:浙江省2021届高三上学期高考选考科目9月联考化学试题(B)
单选题
|
适中(0.65)
17. 香豆素-3-羧酸是日用化学工业中的重要香料之一,它可以通过水杨醛经多步反应合成:

下列说法不正确的是

下列说法不正确的是
| A.水杨醛与苯甲酸互为同分异构体 |
| B.水杨醛、中间体、香豆素-3-羧酸都能使酸性高锰酸钾溶液褪色 |
| C.中间体、香豆素-3-羧酸互为同系物 |
| D.1mol香豆素-3-羧酸与NaOH溶液反应最多消耗3molNaOH |
【知识点】 有机官能团的性质及结构 多官能团有机物的结构与性质解读
您最近一年使用:0次
2020-11-10更新
|
123次组卷
|
2卷引用:内蒙古2021届高三上学期10月大联考化学试题
单选题
|
适中(0.65)
名校
18. 分别利用如图装置(夹持装置略)进行相应实验,不能达到实验目的的是


| A.用甲装置制备并收集NH3 | B.用乙装置制备溴苯并验证有HBr产生 |
| C.用丙装置制备无水FeCl3 | D.用丁装置制备Fe(OH)2并能较长时间观察其颜色 |
您最近一年使用:0次
2020-11-10更新
|
241次组卷
|
5卷引用:内蒙古2021届高三上学期10月大联考化学试题
单选题
|
适中(0.65)
名校
解题方法
19. 下列关于卤素(用X表示)的叙述中正确的是( )
| A.卤素单质的颜色从F2→I2随相对分子质量增大而逐渐加深 |
| B.HX都极易溶于水,HX热稳定性随X的核电荷数增加而增强 |
| C.卤素单质与水反应均可用X2+H2O⇌HXO+HX表示 |
| D.X‾离子的还原性依次为:F‾<Cl‾<Br‾<I‾,因此相对分子质量小的卤素单质均可将相对分子质量大的卤素从其盐溶液中置换出来 |
您最近一年使用:0次
2018-05-09更新
|
389次组卷
|
8卷引用:宁夏银川一中2017-2018学年高一下学期期中考试化学试题
单选题
|
适中(0.65)
名校
解题方法
20. 我国著名科学家侯德榜发明的“侯氏制碱法”为世界制碱工业做出了巨大贡献。如图是“侯氏制碱法”在实验室进行模拟实验的流程示意图,则下列叙述不正确的是


| A.A气体是CO2,B气体是NH3 |
| B.侯氏制碱法的工艺流程应用了物质溶解度的差异 |
| C.第III步骤用到的主要玻璃仪器是烧杯、漏斗、玻璃棒,第IV步操作是煅烧 |
| D.侯氏制碱法的最终产品是Na2CO3和NH4Cl |
您最近一年使用:0次
2022-01-17更新
|
119次组卷
|
4卷引用:内蒙古巴彦淖尔市乌拉特前旗第一中学2020-2021学年高二下学期期末考试化学试题
单选题
|
适中(0.65)
21. 北宋沈括《梦溪笔谈》中记载:“信州铅山有苦泉,流以为涧。挹其水熬之则成胆矾,烹胆矾则成铜。熬胆矾铁釜,久之亦化为铜”。下列有关叙述错误的是
| A.胆矾的化学式为CuSO4 |
| B.胆矾可作为湿法冶铜的原料 |
| C.“熬之则成胆矾”是浓缩结晶过程 |
| D.“熬胆矾铁釜,久之亦化为铜”是发生了置换反应 |
您最近一年使用:0次
2020-07-08更新
|
17338次组卷
|
70卷引用:2020年全国统一考试化学试题(新课标Ⅱ)
2020年全国统一考试化学试题(新课标Ⅱ)辽宁省阜新市第二高级中学2019-2020学年高二下学期期末考试化学试题(已下线)专题05 元素及其化合物-2020年高考真题和模拟题化学分项汇编(已下线)第01章 物质及其变化(B卷能力提高篇)——2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)(已下线)小题必刷01 物质的组成、分类和性质 ——2021年高考化学一轮复习小题必刷(通用版)(已下线)小题必刷15 铁、铜及其化合物——2021年高考化学一轮复习小题必刷(通用版)甘肃省平凉市庄浪县第一中学2021届高三上学期第一次模拟化学试题辽宁省葫芦岛市第八高级中学2020-2021学年高一上学期实验班第一次月考化学试题福建省永安市第三中学2021届高三10月月考化学试题江苏省淮安市涟水县第一中学2021届高三上学期10月月考化学试题广东省云浮市郁南县蔡朝焜纪念中学2020-2021学年高一上学期10月月考化学试题(已下线)【浙江新东方】33宁夏青铜峡市高级中学2021届高三上学期期中考试化学试题内蒙古巴彦淖尔市临河三中2020-2021学年高二10月考化学试题(已下线)热点2 化学与传统文化-2021年高考化学专练【热点·重点·难点】(已下线)热点2 化学与传统文化-2021年高考化学【热点·重点·难点】专练(山东专用)黑龙江省鹤岗市绥滨县第一中学2020-2021学年高一上学期期中考试化学试题湖南省长沙市第一中学2020-2021学年高一下学期开学考化学试题广东省汕头市金山中学2021届高三下学期学科素养测试化学试题(已下线)重点3 化学用语-2021年高考化学专练【热点·重点·难点】(已下线)押山东卷第01题 化学与STSE、传统文化-备战2021年高考化学临考题号押题(山东卷)(已下线)押全国卷理综第7题 化学与社会生产生活-备战2021年高考化学临考题号押题(课标全国卷)(苏教版2019)必修第二册专题9 金属与人类文明 C 高考挑战区内蒙古巴彦淖尔市乌拉特前旗第一中学2020-2021学年高二下学期期末考试化学试题(已下线)课时18 铜及其化合物 合金-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第3讲 物质的分类及变化(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)吉林省延边第二中学2020-2021学年高一上学期第一次考试月考化学试题吉林省抚松县泉阳镇抚松县第六中学2021-2022学年高二上学期化学与生活知识竞赛化学试题(已下线)第10周 晚练题-备战2022年高考化学周测与晚练(新高考专用)(已下线)第三单元 金属及其化合物(B卷 真题滚动练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)吉林省长春北师大附属学校2021-2022学年高一上学期第一次月考化学试题浙江省平湖市当湖高级中学2021-2022学年高一上学期第一次月考化学试题山东省潍坊第四中学2022届高三上学期收心考试化学试题(已下线)专题讲座(七) STSE与 化学可持续发展(练) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)专题讲座(七) STSE与 化学可持续发展(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)河南省濮阳市油田第一中学2021年高一上学期第一次月考化学试题(已下线)专题01 化学与STSE—2022年高考化学二轮复习讲练测-讲义2020年全国卷Ⅱ化学真题变式题(已下线)卷01 化学与传统文化-【小题小卷】冲刺2022年高考化学小题限时集训(全国卷专用)(已下线)押全国卷理综第7题 化学与社会生产生活及传统文化-备战2022年高考化学临考题号押题(课标全国卷)(已下线)回归教材重难点01 化学与STSE与传统文化-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)查补易混易错点01 物质的组成、性质、分类及化学用语-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题01STSE化学用语-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题01STSE化学用语-五年(2018~2022)高考真题汇编(全国卷)(已下线)第01练 化学与科技社会生产生活、传统文化-2022年【暑假分层作业】高二化学(2023届一轮复习通用)河北省保定市唐县第一中学2021-2022学年高一下学期6月考试化学试题(已下线)微专题01 “话”中有“化”—化学与传统文化-备战2023年高考化学一轮复习考点微专题(已下线)考点16 铜及其金属材料-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第01讲 物质的分类及转化(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)微专题15 铜及其化合物的性质、制备与实验探究-备战2023年高考化学一轮复习考点微专题(已下线)第10讲 金属材料及金属矿物的开发利用(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)专题03 物质的组成-备战2023年高考化学母题题源解密(广东卷)浙江省东阳中学2021-2022学年高一上学期1月份考试化学试题★综合拔高练宁夏固原市第一中学2023届高三上学期第一次月考化学试题内蒙古彦淖尔市临河区第三中学2022届高三上学期第一次月考化学试题广东省佛山市顺德区第一中学2023届高三 9月月考化学试题甘肃省武威第十八中学2021-2022学年高二下学期期末考试化学试卷天津市北辰区2022-2023学年高三上学期第一次联考化学试题湖南省衡阳县四中2022-2023学年高二上学期开学摸底考试化学试题(B卷)(已下线)专题二 化学与STSE-实战高考·二轮复习核心突破湖北省武汉大学附属中学2021-2022学年高二上学期开学考试化学试题(已下线)第一部分 二轮专题突破 专题7 化学与传统文化(已下线)题型36 铜的冶炼(已下线)第一章 化学物质及其变化 第1练 物质的组成、性质和分类(已下线)题型1 传统文化-高考必备50个题型江苏省常熟中学2023-2024学年高一上学期10月阶段性学业水平调研化学试题安徽省安庆第二中学东区2021-2022学年高三上学期9月月考化学试卷甘肃省平凉市泾川县第三中学2023-2024学年高三上学期第3次月考化学试题陕西省渭南市三贤中学2023-2024学年高三上学期11月月考化学试题
单选题
|
适中(0.65)
名校
解题方法
22. 苯氧乙醇在化妆品、护肤品、疫苗及药品中发挥着防腐剂的功用,其结构为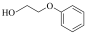 ,下列有关说法不正确的是
,下列有关说法不正确的是
 ,下列有关说法不正确的是
,下列有关说法不正确的是| A.苯氧乙醇的分子式为C8H10O2 |
| B.苯氧乙醇中的所有碳原子不可能处于同一平面内 |
| C.苯氧乙醇既可以发生取代反应和加成反应,也可以使酸性高锰酸钾溶液褪色 |
| D.分子式为C8H8O2,结构中含有苯环且能与饱和NaHCO3溶液反应的物质共有4种(不考虑立体异构) |
【知识点】 有机官能团的性质及结构 根据要求书写同分异构体解读
您最近一年使用:0次
2020-05-04更新
|
323次组卷
|
3卷引用:山西省太原市2020届高三第一次模拟考试理综化学试题
单选题
|
适中(0.65)
名校
23. 将3.48g四氧化三铁完全溶解在100mL 1mol/L硫酸中,然后加K2Cr2O7溶液25mL,恰好使溶液中Fe2+全部转为Fe3+,Cr2O72-全部转化为Cr3+,则K2Cr2O7溶液物质的量浓度是
| A.0.05mol/L | B.0.1mol/L | C.0.2mol/L | D.0.3mol/L |
【知识点】 基于氧化还原反应守恒规律的计算解读 铁的氧化物 亚铁盐
您最近一年使用:0次
2019-07-26更新
|
549次组卷
|
15卷引用:2014-2015内蒙古北方重工业集团三中高一下学期第一次月考化学试卷
2014-2015内蒙古北方重工业集团三中高一下学期第一次月考化学试卷2018届高三一轮复习化学:考点14-氧化还原反应的计算河南省商丘市第一高级中学2017-2018学年高一上学期第二次月考化学试题江西省景德镇市第一中学2017-2018学年高一上学期期末考试化学试题黑龙江省大庆铁人中学2017-2018学年高一下学期开学考试(3月)化学试题山东省德州市夏津县一中2019届高三上学期第一次月考化学试题【全国百强校】陕西省西安中学2019届高三上学期期中考试化学试题吉林省长春市实验中学2018-2019学年高二下学期期末考试化学试题陕西省咸阳百灵中学2020届高三上学期期中考试化学试题(已下线)专题2.3 氧化还原反应 -巅峰冲刺山东省2020年高考化学一轮考点扫描《2020年新高考政策解读与配套资源》山东省新泰市第一中学老校区(新泰中学)2021届高三上学期第一次月考化学试题云南省丽江市2019-2020学年高一下学期期末教学质量监测化学试题河北省石家庄私立第一中学2020-2021学年高一下学期第五次调研考试化学试题内蒙古巴彦淖尔市乌拉特前旗第一中学2020-2021学年高二下学期期末考试化学试题(已下线)专题七 氧化还原反应
单选题
|
适中(0.65)
名校
解题方法
24. 习主席在2020年新年贺词中强调“5G商用加速推出,凝结着新时代奋斗者的心血和汗水,彰显了不同凡响的中国风采、中国力量”,制造芯片用到高纯硅,用SiHCl3与过量H2在1100~1200℃反应制备高纯硅的装置如下图所示(热源及夹持装置略去)。
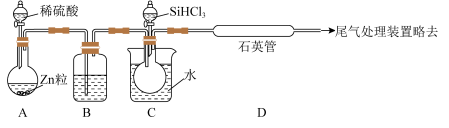
| A.装置 B 中的试剂是浓硫酸 |
| B.实验时先打开装置C中分液漏斗的旋塞 |
| C.装置C中的烧瓶需要加热,其目的是使滴入烧瓶中的SiHCl3气化 |
| D.装置D不能采用普通玻璃管的原因是在反应温度下,普通玻璃管会软化 |
您最近一年使用:0次
2020-05-05更新
|
2338次组卷
|
22卷引用:河南郑州外国语学校2020高三第4次线上调研理综化学试题
河南郑州外国语学校2020高三第4次线上调研理综化学试题四川省攀枝花市第十五中学2019-2020学年高一下学期期中考试化学试题湖北省安陆市第一中学2021届高三8月月考化学试题河南省南阳市2021届高三期中质量评估化学试题河南省南阳市第一中学校2021届高三上期第五次考试化学试题(已下线)专题03 化学实验(制取、除杂、装置等考查)-2021年高考化学必做热点专题人教版2019必修第二册 第五章 第三节 无机非金属材料河南省南阳市2021届高三上期期中考试化学试题山东省济宁市邹城二中2020-2021学年高一下学期6月月考化学试题内蒙古巴彦淖尔市乌拉特前旗第一中学2020-2021学年高二下学期期末考试化学试题四川省攀枝花市成都外国语学校2020-2021学年高一下学期期中考试化学(理)试题甘肃省天水市第一中学2021-2022高三上学期第三次考试化学试题河南省名校联盟2021-2022学年高三上学期第三次诊断考试化学试题广东省珠海市三校2021-2022学年高一下学期期中联考化学试题(已下线)第14练 无机非金属材料-2023年高考化学一轮复习小题多维练(全国通用)广西南宁市宾阳县宾阳中学2021-2022学年高一下学期3月月考化学试题安徽省滁州市定远县民族中学2021-2022学年高一下学期期中考试化学试题(已下线)专题25 化学实验综合性选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)广东省梅州兴宁市沐彬中学2021-2022学年高一下学期 3月月考化学试题5.3.2 新型无机非金属材料 随堂练习天津市耀华中学2023-2024学年高一下学期期中考试化学试卷海南省文昌中学2023-2024学年高一下学期期中段考化学试题
单选题
|
适中(0.65)
名校
解题方法
25. 碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如下:
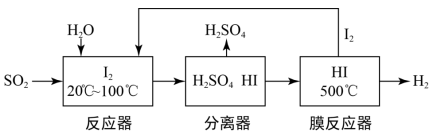
| A.分离器中的物质分离操作为过滤 |
| B.该工艺中I2和HI的相互转化体现了“碘循环” |
| C.该工艺中HI的量没有改变,可视作该工艺的催化剂 |
| D.碘循环工艺的总反应为 2SO2+4H2O+I2=H2+2H2SO4+2HI |
【知识点】 二氧化硫
您最近一年使用:0次
2021-05-23更新
|
326次组卷
|
12卷引用:【全国百强校】江西省抚州市临川第一中学2018-2019学年高一下学期第一次月考化学试题
【全国百强校】江西省抚州市临川第一中学2018-2019学年高一下学期第一次月考化学试题山东省泰安市2019-2020学年高一下学期期末考试化学试题高一必修第二册(人教2019版)全书综合训练辽宁省实验中学东戴河分校2020-2021学年高一10月月考化学试题(已下线)易错21 化学工艺流程类选择题-备战2021年高考化学一轮复习易错题(已下线)【浙江新东方】高中化学20210513-028【2021】【高一下】重庆市凤鸣山中学2020-2021学年高一下学期期中考试化学试题江西省新余市2020-2021学年高一下学期期末质量检测化学试题内蒙古巴彦淖尔市乌拉特前旗第一中学2020-2021学年高二下学期期末考试化学试题江西省萍乡市2021-2022学年高一下学期期末考化学试题黑龙江省齐齐哈尔市恒昌中学校2022-2023学年高一下学期4月月考化学试题山东省泰安市新泰第一中学老校区(新泰中学)2023-2024学年高一下学期第一次月考化学试题
二、解答题 添加题型下试题
解答题-无机推断题
|
较难(0.4)
名校
解题方法
26. A、B、C、D是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去)。

(1)若A是一种黄色单质固体,一定条件下B可以转化为C,则B→C的化学方程式为___________________ 。
(2) 若A是一种活泼金属,C是淡黄色固体,则C的名称为______________ ,C可用在矿山、坑道、潜水或宇宙飞船等缺氧的场合,将人们呼出的CO2再转换成O2,以供呼吸之用,请用化学方程式表示该反应原理_____________________________ 。
若生成1mol O2,该反应转移电子的物质的量为____________ 。
(3)若A为能使湿润的红色石蕊试纸变蓝的气体,C是红棕色气体。回答:
①A为___________ (填写化学式)。实验室用两种固体共热制取A,写出此化学方程式:_____________ 。
②D可以转化为B,则D→B反应的离子方程式:________________________ 。

(1)若A是一种黄色单质固体,一定条件下B可以转化为C,则B→C的化学方程式为
(2) 若A是一种活泼金属,C是淡黄色固体,则C的名称为
若生成1mol O2,该反应转移电子的物质的量为
(3)若A为能使湿润的红色石蕊试纸变蓝的气体,C是红棕色气体。回答:
①A为
②D可以转化为B,则D→B反应的离子方程式:
您最近一年使用:0次
2016-12-09更新
|
1530次组卷
|
4卷引用:2014-2015山西省忻州市第一中学高一上学期期末考试化学试卷
解答题-工业流程题
|
适中(0.65)
解题方法
27. 绿水青山是习近平总书记构建美丽中国的伟大构想,可用化学实现“变废为宝”,碱式硫酸铁是一种用于污水处理的新型高效絮凝剂,可由硫酸亚铁同热的稀硝酸制得,工业上利用废铁屑(含少量氧化铝、铁的氧化物等)生产碱式硫酸铁的工艺流程如图:
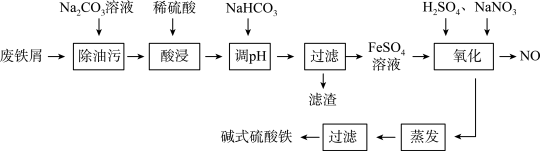
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如表所示。
回答下列问题:
(1)可用Na2CO3溶液除去废铁屑表面油污的原因是___________ (用离子方程式表示)。
(2)“酸浸”后溶液中主要的金属阳离子有___________ (填离子符号)。
(3)“调pH”时加入少量NaHCO3应控制pH的范围是___________ ,理由是______ 。
(4)“氧化”中加入NaNO3和稀H2SO4的目的是氧化Fe2+,写出该反应的离子方程式:___ 。
(5)碱式硫酸铁溶于水后生成的Fe(OH)2+离子可部分水解生成Fe2(OH) 聚合离子,该水解反应的离子方程式为
聚合离子,该水解反应的离子方程式为_____ 。

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如表所示。
沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
开始沉淀的pH | 2.3 | 7.5 | 3.4 |
完全沉淀的pH | 3.2 | 9.7 | 4.4 |
(1)可用Na2CO3溶液除去废铁屑表面油污的原因是
(2)“酸浸”后溶液中主要的金属阳离子有
(3)“调pH”时加入少量NaHCO3应控制pH的范围是
(4)“氧化”中加入NaNO3和稀H2SO4的目的是氧化Fe2+,写出该反应的离子方程式:
(5)碱式硫酸铁溶于水后生成的Fe(OH)2+离子可部分水解生成Fe2(OH)
 聚合离子,该水解反应的离子方程式为
聚合离子,该水解反应的离子方程式为
您最近一年使用:0次
2020-11-10更新
|
710次组卷
|
2卷引用:内蒙古2021届高三上学期10月大联考化学试题
解答题-实验探究题
|
适中(0.65)
名校
解题方法
28. 在实验室中用二氧化锰与浓盐酸在加热条件下反应制备干燥纯净的氯气。进行此实验,所用仪器如图所示:

(1)连接上述仪器的正确顺序(填各接口处的字母):E接___________;___________接___________;___________接___________;___________接F。___________
(2)写出下列反应的化学方程式:NaOH溶液中发生的反应:___________ 。
(3)装置中,饱和食盐水的作用是___________ ;浓硫酸的作用是___________ 。
(4)化学实验中常用湿润的淀粉-KI试纸检验是否有Cl2产生。如果有Cl2产生,可观察到___________ ,反应化学方程式为___________ 。
(5)工业上氯气和石灰乳反应可以制取漂白粉,家庭中使用漂白粉时,为了增强漂白能力,可加入少量的物质是___________
A.食盐B.食醋C.烧碱D.纯碱
该反应放热会使体系温度升高,导致氯气和石灰浆发生副反应产生杂质Ca(ClO3)2,该副反应中还原剂与氧化剂的质量之比为___________ 。

(1)连接上述仪器的正确顺序(填各接口处的字母):E接___________;___________接___________;___________接___________;___________接F。
(2)写出下列反应的化学方程式:NaOH溶液中发生的反应:
(3)装置中,饱和食盐水的作用是
(4)化学实验中常用湿润的淀粉-KI试纸检验是否有Cl2产生。如果有Cl2产生,可观察到
(5)工业上氯气和石灰乳反应可以制取漂白粉,家庭中使用漂白粉时,为了增强漂白能力,可加入少量的物质是
A.食盐B.食醋C.烧碱D.纯碱
该反应放热会使体系温度升高,导致氯气和石灰浆发生副反应产生杂质Ca(ClO3)2,该副反应中还原剂与氧化剂的质量之比为
您最近一年使用:0次
2021-04-02更新
|
142次组卷
|
2卷引用:甘肃省金昌市第一中学2020-2021学年高一上学期期末考试化学试题
解答题-有机推断题
|
适中(0.65)
29. 以葡萄糖为原料制得的山梨醇(A)和异山梨醇(B)都是重要的生物质转化平台化合物。E是一种治疗心绞痛的药物。由葡萄糖为原料合成E的路线如下:
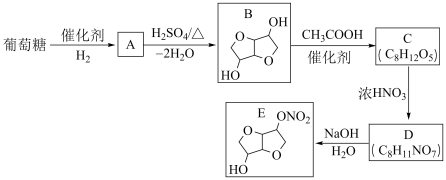
回答下列问题:
(1)葡萄糖的分子式为_____ 。
(2)A中含有的官能团的名称为_____ 。
(3)由B到C的反应类型为_____ 。
(4)C的结构简式为_____ 。
(5)由D到E的反应方程式为_____ 。
(6)F是B的同分异构体,7.30g的F与足量饱和碳酸氢钠反应可释放出2.24L二氧化碳(标准状况),F的可能结构共有_____ 种(不考虑立体异构);其中核磁共振氢谱为三组峰,峰面积比为3:1:1的结构简式为_____ 。

回答下列问题:
(1)葡萄糖的分子式为
(2)A中含有的官能团的名称为
(3)由B到C的反应类型为
(4)C的结构简式为
(5)由D到E的反应方程式为
(6)F是B的同分异构体,7.30g的F与足量饱和碳酸氢钠反应可释放出2.24L二氧化碳(标准状况),F的可能结构共有
您最近一年使用:0次
2018-06-09更新
|
12345次组卷
|
26卷引用:2018年全国普通高等学校招生统一考试化学(新课标II卷)
2018年全国普通高等学校招生统一考试化学(新课标II卷)(已下线)2018年高考题及模拟题汇编 专题17 有机化学合成与推断(选修)四川省攀枝花市第十二中学2019届高三上学期第一次月考化学试题甘肃省靖远县第一中学2019届高三上学期9月月考化学试题【全国百强校】四川省棠湖中学2019届高三上学期第三次月考理综-化学试题(已下线)《2019年高考总复习巅峰冲刺》专题13 有机化学基础应试策略河北省唐山市开滦第二中学2018-2019学年高二6月月考化学试题云南省陇川县一中2020届高三上学期开学考试化学试题云南省文山州广南一中2019-2020学年高二上学期期中考试化学试题广东省北大附中深圳南山分校2020届高三上学期期中考试化学试题四川省自贡市田家炳中学2020届高三上学期期中考试化学试题(已下线)考点17 基本营养物质——《备战2020年高考精选考点专项突破题集》黑龙江省大庆市第四中学2020届高三下学期4月月考理综化学试题河北省张家口市宣化区宣化第一中学2019-2020学年高二下学期6月月考化学试题(已下线)专题讲座(十) 有机综合推断题突破策略(精练)-2021年高考化学一轮复习讲练测高二选择性必修3(人教版2019)第四章 生物大分子 第四章素养检测(已下线)解密13 有机化学基础(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密12 有机化学基础(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(人教2019)选择性必修3第四章 C高考挑战区内蒙古巴彦淖尔市乌拉特前旗第一中学2020-2021学年高二下学期期末考试化学试题吉林省吉林市第二中学2020-2021学年高二下学期期中考试化学试卷山东师范大学附属中学2021-2022学年高二下学期期中考试化学试题(已下线)专题19有机化学基础(选修)-五年(2018~2022)高考真题汇编(全国卷)专题6 生命活动的物质基础——糖类、油脂、蛋白质 第一~二单元综合拔高练期末学业水平检测(二)河北省石家庄市元氏县第四中学2021-2022学年高二下学期第一次月考化学试题
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、有机化学基础、物质结构与性质、化学与STSE、化学实验基础、认识化学科学、化学反应原理
试卷题型(共 29题)
题型
数量
单选题
25
解答题
4
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 二氧化硫 硅的物理性质与用途 铝 | |
| 2 | 0.85 | 漂白粉和漂粉精的用途 乙醇 卤代烃在生活中的应用 氢键对物质性质的影响 | |
| 3 | 0.65 | 氯气的实验室制法 海带中碘的提取及检验 | |
| 4 | 0.65 | 过氧化钠与水的反应 过氧化钠和二氧化碳反应 物质性质的探究 | |
| 5 | 0.65 | 离子反应在混合物分离、除杂中的应用 碳酸钠与碳酸氢钠的相互转化 铁盐、亚铁盐相互除杂 物质分离、提纯的常见化学方法 | |
| 6 | 0.65 | 离子方程式的正误判断 偏铝酸钠与盐酸的反应 铁的氧化物 氢氧化铁化学性质 | |
| 7 | 0.65 | 二氧化硫的漂白性 浓硫酸的强氧化性 物质性质的探究 | |
| 8 | 0.4 | 硫与氧气反应 二氧化硫的漂白性 二氧化硫与其他强氧化剂的反应 | |
| 9 | 0.94 | 硫、氮氧化物对人体、环境的危害 酸雨 大气污染 大气污染来源及危害 | |
| 10 | 0.65 | 二氧化硫与二氧化碳的性质区别 二氧化硫的漂白性 二氧化硫与其他强氧化剂的反应 | |
| 11 | 0.85 | 常见金属的冶炼 | |
| 12 | 0.85 | 含硫化合物之间的转化 硫、氮氧化物对人体、环境的危害 酸雨 二氧化硫与其他强氧化剂的反应 | |
| 13 | 0.65 | 氯气的化学性质 其他含卤化合物 | |
| 14 | 0.85 | 焰色试验 | |
| 15 | 0.65 | 铝与强碱溶液反应 含氧化铝的混合物的提纯 氢氧化铝与强酸反应 铝盐与强碱溶液反应 | |
| 16 | 0.85 | 硫的氧化物对人体、环境的危害 酸雨 大气污染的治理原理及方法 | |
| 17 | 0.65 | 有机官能团的性质及结构 多官能团有机物的结构与性质 | |
| 18 | 0.65 | 氨气的实验室制法 氢氧化亚铁的制备 制备与水解有关的物质 苯的取代反应 | |
| 19 | 0.65 | 同主族元素性质递变规律 同主族元素性质递变规律理解及应用 | |
| 20 | 0.65 | 碳酸氢钠 碳酸氢钠的不稳定性 常见无机物的制备 纯碱的生产 | |
| 21 | 0.65 | 铜 硫酸铜 | |
| 22 | 0.65 | 有机官能团的性质及结构 根据要求书写同分异构体 | |
| 23 | 0.65 | 基于氧化还原反应守恒规律的计算 铁的氧化物 亚铁盐 | |
| 24 | 0.65 | 硅的制备 物质制备的探究 | |
| 25 | 0.65 | 二氧化硫 | |
| 二、解答题 | |||
| 26 | 0.4 | 无机综合推断 氨的还原性 含硫化合物之间的转化 过氧化钠 | 无机推断题 |
| 27 | 0.65 | 氧化还原反应方程式的配平 有关铁及其化合物转化的流程题型 盐类水解在生活、生产中的应用 物质分离、提纯综合应用 | 工业流程题 |
| 28 | 0.65 | 氯气的化学性质 氯气的实验室制法 物质性质的探究 | 实验探究题 |
| 29 | 0.65 | 酯的水解反应机理 有机推断综合考查 | 有机推断题 |



