内蒙古彦淖尔市临河区第三中学2022届高三上学期第一次月考化学试题
内蒙古
高三
阶段练习
2022-10-11
96次
整体难度:
容易
考查范围:
认识化学科学、常见无机物及其应用、化学实验基础、有机化学基础
一、单选题 添加题型下试题
 。下列说法正确的是
。下列说法正确的是A.1L0.1mol· NH4Cl溶液中, NH4Cl溶液中, 的数量为0.1 的数量为0.1 |
B.2.4gMg与H2SO4完全反应,转移的电子数为0.1 |
C.标准状况下,2.24LN2和O2的混合气体中分子数为0.2 |
D.0.1mol H2和0.1mol I2于密闭容器中充分反应后,其分子总数为0.2 |
【知识点】 阿伏加德罗常数 阿伏加德罗定律 氧化还原反应有关计算
| A.物质的摩尔质量等于其相对分子(原子)质量 |
| B.“物质的量”是国际单位制中的一个基本单位 |
| C.0.012 kg12C中所含的碳原子数为NA |
| D.1mol任何物质都含有约6.02×1023个原子 |
【知识点】 物质的量及单位——摩尔 阿伏加德罗常数 摩尔质量 物质的量的含义解读
| A.根据丁达尔效应可将分散系分为溶液、胶体和浊液 |
B. 胶体在电场中可作定向移动,是因为 胶体在电场中可作定向移动,是因为 胶体带电 胶体带电 |
C.将含0.1mol 的饱和溶液滴入沸水中,形成的胶体粒子数目为 的饱和溶液滴入沸水中,形成的胶体粒子数目为 |
D.向 胶体中逐滴滴入 胶体中逐滴滴入  溶液,有沉淀生成,继续滴加,沉淀溶解 溶液,有沉淀生成,继续滴加,沉淀溶解 |

| A.复分解反应、复分解反应、化合反应、置换反应 |
| B.中和反应、置换反应、复分解反应、置换反应 |
| C.复分解反应、复分解反应、置换反应、置换反应 |
| D.分解反应、复分解反应、置换反应、置换反应 |
| A.0.3mol/L | B.0.04mol/L | C.0.03mol/L | D.0.05mol/L |
【知识点】 物质的量浓度的计算 物质的量浓度与溶液稀释的计算解读
| A.10g H2和10gO2 | B.5.6L N2(标准状况)和22g CO2 |
| C.9g H2O和0.5mol Br2 | D.224mL H2(标准状况)和0.1mol N2 |
【知识点】 气体摩尔体积 根据n=m/M进行相关计算解读
| A.KCl、NaCl | B.KCl、MgSO4 |
| C.KCl、CaCO3 | D.MgSO4、NaCl |
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
【知识点】 离子反应的发生条件解读 离子共存 无附加条件的离子共存解读
| A.FeCl3溶液与Cu的反应:Cu+Fe3+=Cu2++Fe2+ |
| B.NO2与水的反应:3NO2+H2O=2NO3-+NO+2H+ |
| C.醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+=Ca2++H2O+CO2↑ |
| D.向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
【知识点】 离子方程式的正误判断解读
| A.950mL 111.2g | B.500mL 117g |
| C.1000mL 117g | D.任意规格 111.2g |
A.某无色溶液中可能大量存在 、 、 、 、 |
B. 的溶液中可能大量存在 的溶液中可能大量存在 、 、 、 、 |
C. 与 与 在酸性溶液中的反应: 在酸性溶液中的反应:  |
D.稀硫酸和氢氧化钡溶液反应:  |
【知识点】 离子反应的发生及书写 离子共存 限定条件下的离子共存解读
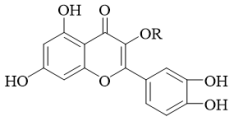
| A.若R为甲基则该物质的分子式可以表示为C16H10O7 |
| B.该物质中有3种官能团 |
| C.该化合物可与FeCl3发生显色反应 |
| D.lmol该化合物与NaOH溶液作用消耗NaOH的物质的量以及与氢气加成所需的氢气的物质的量分别是4mol、6mol |
| A.胆矾的化学式为CuSO4 |
| B.胆矾可作为湿法冶铜的原料 |
| C.“熬之则成胆矾”是浓缩结晶过程 |
| D.“熬胆矾铁釜,久之亦化为铜”是发生了置换反应 |
| A.1∶2 | B.2∶1 | C.1∶3 | D.3∶1 |
【知识点】 与氧化剂、还原剂有关的计算解读
| A.Cu+2FeCl3=2FeCl2+CuCl2 | B.HNO3+KOH=KNO3+H2O |
C.2KMnO4 K2MnO4+MnO2+O2↑ K2MnO4+MnO2+O2↑ | D.C+CO2 2CO 2CO |
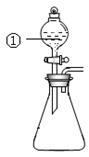
| 选项 | ①中物质 | ②中物质 | 预测②中的现象 |
| A. | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生气泡 |
| B. | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
| C. | 氯化铝溶液 | 浓氢氧化钠溶液 | 产生大量白色沉淀 |
| D. | 草酸溶液 | 高锰酸钾酸性溶液 | 溶液逐渐褪色 |
| A.A | B.B | C.C | D.D |
| A.谷物发酵酿造食醋 | B.小苏打用作食品膨松剂 |
| C.含氯消毒剂用于环境消毒 | D.大气中NO2参与酸雨形成 |
 中,氧化产物与还原产物的物质的量之比是
中,氧化产物与还原产物的物质的量之比是| A.1:2 | B.1:1 | C.2:1 | D.4:1 |
| 物质(括号内为杂质) | 除杂试剂 | |
| A | FeCl2溶液(FeCl3) | Fe粉 |
| B | NaCl溶液(MgCl2) | NaOH溶液、稀HCl |
| C | Cl2(HCl) | H2O、浓H2SO4 |
| D | NO(NO2) | H2O、无水CaCl2 |
| A.A | B.B | C.C | D.D |
【知识点】 氧化还原反应的规律解读 物质分离、提纯的常见化学方法解读
二、解答题 添加题型下试题


 +H2O
+H2O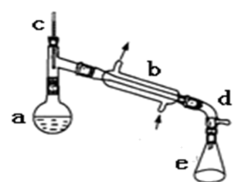
可能用到的有关数据如下:
| 相对分子质量 | 密度/g·cm-3 | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
Ⅰ.合成反应:
在a中加入20 g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1 mL浓硫酸,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90 ℃。
Ⅱ.分离提纯:
反应粗产物倒入分液漏斗中分别用少量5 %碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到纯净环己烯10 g。
回答下列问题:
(1)装置b的名称是
(2)加入碎瓷片的作用是
A.立即补加 B.冷却后补加 C.不需补加 D.重新配制
(3)分液漏斗在使用前须清洗干净并

请回答下列问题:
(1)A的化学名称是
(2)B和A反应生成C的化学方程式为
(3)D的结构简式为
(4)A的同分异构体的结构简式为
三、填空题 添加题型下试题
(1)用双线桥法标出电子转移的方向和数目
(2)该反应的离子方程式为
(3)该反应中氧化剂与还原剂的物质的量之比是
(4)少量的钠应保存在
(1)以上物质中属于混合物的是
(2)向④中逐滴滴加⑦,可观察到的现象是
(3)写出物质⑧在水中的电离方程式:
(4)写出物质①和⑦反应的离子方程式:
(5)8.5g⑥约含有
试卷分析
试卷题型(共 24题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.4 | 阿伏加德罗常数 阿伏加德罗定律 氧化还原反应有关计算 | |
| 2 | 0.65 | 物质的量及单位——摩尔 阿伏加德罗常数 摩尔质量 物质的量的含义 | |
| 3 | 0.94 | 分散系概念及其分类 胶体的定义及分类 胶体的性质和应用 | |
| 4 | 0.85 | 四种基本反应类型 | |
| 5 | 0.85 | 物质的量浓度的计算 物质的量浓度与溶液稀释的计算 | |
| 6 | 0.85 | 气体摩尔体积 根据n=m/M进行相关计算 | |
| 7 | 0.65 | 无机物质的分类 单质和化合物 | |
| 8 | 0.85 | 离子反应在化合物组成的分析、鉴定的应用 焰色试验 无机物的检验 | |
| 9 | 0.85 | 离子反应的发生条件 离子共存 无附加条件的离子共存 | |
| 10 | 0.65 | 离子方程式的正误判断 | |
| 11 | 0.65 | 物质的量浓度与溶液配制的计算 配制一定物质的量浓度的溶液实验的仪器 | |
| 12 | 0.65 | 离子反应的发生及书写 离子共存 限定条件下的离子共存 | |
| 13 | 0.65 | 根据元素种类、原子个数、有机物类别确定分子式 常见官能团名称、组成及结构 含碳碳双键物质的性质的推断 含有酚羟基的物质性质的推断 | |
| 14 | 0.65 | 铜 硫酸铜 | |
| 15 | 0.85 | 与氧化剂、还原剂有关的计算 | |
| 16 | 0.85 | 四种基本反应类型 氧化还原反应基本概念 四种基本反应类型与氧化还原反应的关系 | |
| 17 | 0.65 | 铝的钝化 铝盐与强碱溶液反应 化学实验方案的设计与评价 物质性质实验方案的设计 | |
| 18 | 0.94 | 二氧化氮与水反应 硫的氧化物对人体、环境的危害 酸雨 碳酸氢钠的不稳定性 乙醇与强氧化剂的反应 | |
| 19 | 0.65 | 氧化还原反应的几组概念 氧化还原反应有关计算 与氧化剂、还原剂有关的计算 | |
| 20 | 0.65 | 氧化还原反应的规律 物质分离、提纯的常见化学方法 | |
| 二、解答题 | |||
| 21 | 0.85 | 物质分离、提纯的常见物理方法 蒸馏与分馏 萃取和分液 常见有机物的制备 | 实验探究题 |
| 22 | 0.65 | 乙烯 乙醇 有机物的推断 | 有机推断题 |
| 三、填空题 | |||
| 23 | 0.65 | 物质的量有关计算 单线桥、双线桥分析氧化还原反应 氧化还原反应有关计算 钠与水反应原理 | |
| 24 | 0.65 | 物质的量有关计算 非电解质、电解质物质类别判断 电离方程式 离子方程式的书写 | |



