黑龙江省海林市朝鲜族中学2019-2020学年高一上学期期中考试化学试题
黑龙江
高一
期中
2019-12-02
204次
整体难度:
适中
考查范围:
认识化学科学、化学实验基础、常见无机物及其应用
一、单选题 添加题型下试题
| A.铜丝 | B.熔融的MgCl2 | C.NaCl溶液 | D.蔗糖 |
【知识点】 非电解质、电解质物质类别判断解读 物质水溶液的导电性解读
| A.1 mol Cl2作为氧化剂得到的电子数为NA |
| B.在0 ℃,101 kPa时,22.4 L氢气中含有NA个氢原子 |
| C.25 ℃,1.01×105 Pa,64 g SO2中含有的原子数为3 NA |
| D.NA个一氧化碳分子和0.5 mol甲烷的质量比为7∶4 |
| A.0.3mol/L | B.0.04mol/L | C.0.03mol/L | D.0.05mol/L |
【知识点】 物质的量浓度的计算 物质的量浓度与溶液稀释的计算解读
| A.1molN2的质量是14g | B.H2SO4的摩尔质量是98g |
| C.H2O的摩尔质量是18 g /mol | D.1mol HCl的质量是36.5g/mol |
【知识点】 摩尔质量 摩尔质量与相对原子质量区别与联系解读 物质的量有关计算
①过滤 ②蒸发 ③向容量瓶转移液体
| A.①和③ | B.①和② | C.②和③ | D.①②③ |
| A.分液漏斗 | B.普通漏斗 | C.蒸馏烧瓶 | D.试管 |
【知识点】 仪器使用与实验安全
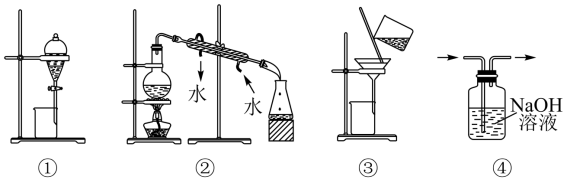
| A.分离植物油和氯化钠溶液选用① |
| B.除去氯化钠晶体中混有的氯化铵晶体选用② |
| C.分离四氯化碳中的溴单质选用③ |
| D.除去二氧化碳气体中的氯化氢气体选用④ |
| A.用过滤的方法除去食盐水中的泥沙 | B.用蒸馏的方法将自来水制成蒸馏水 |
| C.用酒精萃取碘水中的碘 | D.用分液漏斗分离水和苯 |
| A.金属氧化物一定是碱性氧化物 | B.碱性氧化物不一定是金属氧化物 |
| C.酸性氧化物一定是非金属氧化物 | D.非金属氧化物不一定是酸性氧化物 |
【知识点】 酸、碱、盐、氧化物的概念及其相互联系解读
| A.氧化还原反应:元素化合价是否变化 |
| B.纯净物与混合物:是否仅含有一种元素 |
| C.强弱电解质:溶液的导电能力大小 |
| D.溶液与胶体:本质不同的原因是能否发生丁达尔效应 |
【知识点】 分类方法的应用解读 电解质与非电解质 氧化还原反应基本概念
| A.CO32-. H + . Na + . NO3- | B.H + . Ag+ . Cl-. SO42- |
| C.K+ . Na + . OH- .NO 3- | D.Ba2+ .Ca 2+ .SO42- . OH- |
【知识点】 离子共存 无附加条件的离子共存解读
| A.Fe2+、Ba2+、NO3-、Cl- | B.Na+、NH4+、SO42-、Cl- |
| C.Na+、K+、HCO3-、NO3- | D.Na+、K+、MnO4-、Br- |
【知识点】 离子共存 物质共存解读 限定条件下的离子共存解读
| A.5dmol⋅L−1 | B.2.5dmol⋅L−1 | C. mol⋅L−1 mol⋅L−1 | D. mol⋅L−1 mol⋅L−1 |
【知识点】 依据物质的量浓度公式的基础计算解读
| A.2∶1 | B.1∶2 | C.3∶1 | D.1∶3 |
【知识点】 与氧化剂、还原剂有关的计算解读
| A.KClO3在反应中得到电子 | B.ClO2是氧化产物 |
| C.H2C2O4在反应中被还原 | D.1mol KClO3参加反应有2 mol电子转移 |
【知识点】 氧化还原反应的几组概念解读 氧化还原反应有关计算
| A.NH4HCO3 | B.NH4Cl | C.(NH4)2CO3 | D.NH4NO3 |
二、未知 添加题型下试题
三、填空题 添加题型下试题
其中1、2写离子方程式;3、4写水溶液中的电离方程式;5、6写一个对应的化学方程式
(1)碳酸钙和盐酸
(2)氢氧化钡溶液和稀硫酸
(3)NaHSO4
(4)KClO3
(5)H + + OH — = H2O
(6)CO32 —+2H + =CO2↑+H2O
四、计算题 添加题型下试题
(1)含有6.02×1023个氧原子的H2SO4的物质的量是
(2)与标准状况下V LCO2所含氧原子数目相同的水的质量是
(3)将4g NaOH溶解在10mL水中,再稀释成1L,从中取出10mL,这10mL溶液的物质的量浓度为
(4)在一定的温度和压强下,1体积X2(g)跟3体积Y2(g)化合生成2体积化合物,则该化合物的化学式是
(5)将50mL 0.1mol⋅L−1 NaCl和50mL 0.5mol⋅L−1 CaCl2 溶液混合后,若溶液的体积为二者体积之和,则混合溶液中c(Cl −)为
(6)三种正盐的混合溶液中含有0.2mol Na+、0.25mol Mg2+、0.4mol Cl−和SO42−,则n(SO42−)为
五、填空题 添加题型下试题
A .蒸馏 ( 分馏 ) B .萃取 C .过滤 D .重结晶 E .分液。
下列各组混合物的分离或提纯应选用上述哪一种方法最合适?(填方法的标号 )
(1)除去 Ca(OH) 2溶液中悬浮的CaCO3微粒
(2)分离四氯化碳与水的混合物
(3)分离碘水中的碘单质
(4)提纯氯化钠和硝酸钾混合物中的硝酸钾
【知识点】 物质分离、提纯的常见物理方法
六、解答题 添加题型下试题
(1)在下图所示仪器中,配制上述溶液肯定不需要的是

(2)在容量瓶的使用方法中,下列操作不正确的是
| A.使用容量瓶前检验是否漏水 |
| B.容量瓶用水洗净后,再用待配溶液洗涤 |
| C.配制溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。 |
| D.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。 |
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
(3)根据计算用托盘天平称取的NaOH质量为
(4)根据计算得知,需用量筒量取质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为
七、填空题 添加题型下试题
(1)用双线桥标出该反应中电子转移的方向和数目
(2)该反应中还原剂是
(3)若有1molHCl完全反应,则转移的电子得到物质的量是
【知识点】 单线桥、双线桥分析氧化还原反应解读 氧化还原反应有关计算
八、计算题 添加题型下试题
(1)混合后溶液的质量分数
(2)混合后溶液的物质的量浓度
【知识点】 物质的量浓度计算-溶液混合的有关计算解读
试卷分析
试卷题型(共 26题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 非电解质、电解质物质类别判断 物质水溶液的导电性 | |
| 2 | 0.85 | 阿伏加德罗常数的应用 结合气体物质与NA相关推算 结合物质结构基础知识与NA相关推算 | |
| 3 | 0.85 | 物质的量浓度的计算 物质的量浓度与溶液稀释的计算 | |
| 4 | 0.85 | 摩尔质量 摩尔质量与相对原子质量区别与联系 物质的量有关计算 | |
| 5 | 0.85 | 仪器使用与实验安全 常用仪器及使用 配制一定物质的量浓度的溶液的步骤、操作 | |
| 6 | 0.85 | 仪器使用与实验安全 | |
| 7 | 0.65 | 物质分离、提纯的常见物理方法 物质分离、提纯的常见化学方法 | |
| 8 | 0.85 | 物质分离、提纯的常见物理方法 蒸馏与分馏 萃取和分液 过滤 | |
| 9 | 0.65 | 酸、碱、盐、氧化物的概念及其相互联系 | |
| 10 | 0.85 | 分类方法的应用 电解质与非电解质 氧化还原反应基本概念 | |
| 11 | 0.85 | 胶体的定义及分类 胶体的性质和应用 | |
| 12 | 0.85 | 离子方程式的书写 | |
| 13 | 0.85 | 离子共存 无附加条件的离子共存 | |
| 14 | 0.65 | 离子共存 物质共存 限定条件下的离子共存 | |
| 15 | 0.85 | 电解质的电离 离子反应的实际应用 | |
| 16 | 0.65 | 依据物质的量浓度公式的基础计算 | |
| 17 | 0.85 | 与氧化剂、还原剂有关的计算 | |
| 18 | 0.85 | 氧化还原反应的几组概念 氧化还原反应有关计算 | |
| 19 | 0.65 | 铵根离子的检验 离子的检验 常见阳离子的检验 常见阴离子的检验 | |
| 二、未知 | |||
| 20 | 0.65 | 常见氧化剂与还原剂 氧化性、还原性强弱的比较 氧化还原反应的规律 Fe2+的还原性 | 未知 |
| 三、填空题 | |||
| 21 | 0.65 | 电离方程式 离子方程式的书写 | |
| 23 | 0.65 | 物质分离、提纯的常见物理方法 | |
| 25 | 0.65 | 单线桥、双线桥分析氧化还原反应 氧化还原反应有关计算 | |
| 四、计算题 | |||
| 22 | 0.65 | 根据n=m/M进行相关计算 物质的量浓度计算-溶液配制有关计算 物质的量浓度计算-溶液混合的有关计算 | |
| 26 | 0.65 | 物质的量浓度计算-溶液混合的有关计算 | |
| 五、解答题 | |||
| 24 | 0.65 | 一定物质的量浓度的溶液的配制 配制一定物质的量浓度的溶液的步骤、操作 配制一定物质的量浓度的溶液实验的误差分析 配制一定物质的量浓度的溶液实验的仪器 | 实验探究题 |

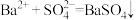 来表示的是
来表示的是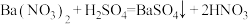
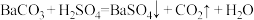
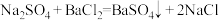
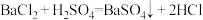
 、
、 、
、 、
、 四种离子,已知前三种离子的个数比为3:2:1,则溶液中
四种离子,已知前三种离子的个数比为3:2:1,则溶液中

