宁夏长庆高级中学2020-2021学年高一上学期第一次月考化学试题
宁夏
高一
阶段练习
2020-11-06
257次
整体难度:
较易
考查范围:
化学实验基础、认识化学科学、常见无机物及其应用、化学与STSE
一、单选题 添加题型下试题
| A.分液漏斗 | B.普通漏斗 | C.蒸馏烧瓶 | D.试管 |
【知识点】 仪器使用与实验安全
| A.用滴管滴加液体时,为防止液体滴到试管外面,滴管应紧贴试管内壁 |
| B.量筒里装一定量水,沿量筒内壁缓缓倒入浓硫酸,配制稀硫酸 |
| C.皮肤上不慎沾洒上了浓硫酸,应先用水冲洗,再涂上一层氢氧化钠溶液 |
| D.称量易潮解的药品时药品应放在干燥洁净的小烧杯等容器中称量 |
| A.过滤操作中,漏斗下端与烧杯内壁不相互接触 |
| B.若发现滤纸漏液,可继续过滤 |
| C.玻璃棒下端应紧靠三层滤纸处 |
| D.为加快过滤速度,可用玻璃棒搅拌漏斗中的液体 |
| A.使蒸发皿盛满滤液,用小火加热 | B.等到蒸发皿中出现较多固体时停止加热 |
| C.待溶液蒸干后,再停止加热 | D.将蒸发皿放在石棉网上,用酒精灯加热 |
| A.萃取、分液前需对分液漏斗检漏 |
| B.进行分液时,分液漏斗中的下层液体从下端流出,上层液体则从上口倒出 |
| C.用酒精萃取溴水中的溴单质的操作可选用分液漏斗,而后静置分液 |
| D.为保证分液漏斗内的液体顺利流出,需将上面的塞子拿下(或使塞上凹槽对准漏斗上的小孔) |
| A.① | B.①② | C.②③ | D.①②③ |
【知识点】 以N=m·NA/M为中心的有关基本粒子的推算解读
| A.1mol CO的质量是28g | B.硝酸的摩尔质量是63g |
| C.2g氢气所含原子数目为1mol | D.铁的摩尔质量等于铁原子的相对原子质量 |
【知识点】 摩尔质量 摩尔质量与相对原子质量区别与联系解读
| A.Wn | B.22.4n | C.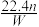 | D. |
【知识点】 阿伏加德罗常数的求算解读
| A.O2 | B.CH4 | C.CO2 | D.SO2 |
【知识点】 阿伏加德罗定律 根据n=m/M的相关计算解读
| A.单位物质的量的气体所占的体积就是气体摩尔体积 |
| B.标准状况下,气体摩尔体积约为22.4L |
| C.同温同压下,相同体积的气体单质,它们的物质的量必相等 |
| D.任何条件下,等物质的量的二氧化碳和一氧化碳所含的分子数必相等 |
| A.常温常压下,11.2L NH3所含的原子数为2NA |
| B.常温常压下,80g SO3含有的氧原子数为3NA |
| C.标准状况下,22.4L H2中所含原子数为NA |
| D.标准状况下,22.4L H2O中含有的氧原子数为NA |
【知识点】 阿伏加德罗常数的应用解读
| A.1molH2O中含有1molH2和1mol O |
| B.等质量的O2和O3中所含的氧原子数相同 |
| C.等质量的CO与CO2中所含碳原子数之比为7︰11 |
| D.98g H2SO4溶解于500mL水中,所得溶液中硫酸的物质的量浓度为2 mol•L-1 |
【知识点】 物质的量的含义解读 物质的量浓度概念、含义解读 物质的量有关计算
A.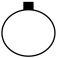 | B. | C. | D. |
【知识点】 阿伏加德罗定律 阿伏加德罗定律及其推论解读 阿伏加德罗定律的应用解读
| A.溶液中含有1mol/L K2SO4 |
| B.1mol/L K2SO4溶于1L水中 |
| C.溶液中c(K+)=2mol/L |
| D.溶液中含2mol K+ |
【知识点】 物质的量浓度概念、含义解读
| A.0.1 mol/L |
| B.1 mol/L |
| C.3 mol/L |
| D.1.5 mol/L |
| A.3mol/L | B.0.2mol/L | C.0.3mol/L | D.0.1mol/L |
【知识点】 物质的量浓度
| A.75 mL 1.5mol·L-1的MgCl2溶液 | B.75 mL 4 mol·L-1的NH4Cl溶液 |
| C.150 mL 2 mol·L-1的KCl溶液 | D.150 mL 1 mol·L-1的NaCl溶液 |
| A.某固体中加入稀盐酸,产生了无色气体,证明该固体中一定含有碳酸盐 |
B.某溶液中滴加BaCl2溶液,生成白色沉淀,证明一定含有 |
| C.用可溶性钡盐检验硫酸根离子的存在时,先在待测溶液中加入盐酸,其作用是排除硫酸根离子以外其他阴离子及银离子的干扰 |
| D.验证某溶液中是否含有Cl-,加入AgNO3溶液,有白色沉淀,证明含Cl- |
①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液
| A.④②⑤ | B.④①②⑤③ | C.②⑤④①③ | D.④②⑤③ |
【知识点】 离子反应在混合物分离、除杂中的应用解读 物质的分离、提纯
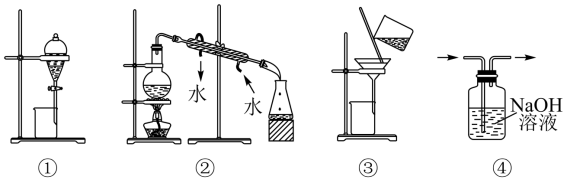
| A.分离植物油和氯化钠溶液选用① |
| B.除去氯化钠晶体中混有的氯化铵晶体选用② |
| C.分离四氯化碳中的溴单质选用③ |
| D.除去二氧化碳气体中的氯化氢气体选用④ |
| A.30g/mol | B.90g/mol | C.30 | D.90 |
| A.0.1 mol·L-1 | B.0.2 mol·L-1 |
| C.0.3 mol·L-1 | D.0.4 mol·L-1 |
【知识点】 物质的量浓度的计算 物质的量浓度与溶质成分有关的计算解读
二、解答题 添加题型下试题
A、萃取分液B、升华C、降温结晶D、分液E、蒸馏F、过滤
①
②
③
④
(II)掌握仪器名称、组装及使用方法是中学化学实验的基础。如图为实验室制取蒸馏水的实验装置
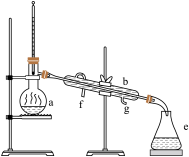
(1)写出下列仪器的名称:a.
(2)若利用该装置分离四氯化碳和酒精的混合物,还缺少的仪器是
(3)实验时a中除加入少量自来水外,还需加入少量
三、计算题 添加题型下试题
(2)同温同压下,同体积的甲烷(CH4)和CO2分子数之比为
(3)标准状况下44.8LHCl气体的物质的量是
(4)标准状况下,1.7gNH3与
(5)标准状况下,1.6g某气态氧化物RO2体积为0.56L,该气体的物质的量为
四、解答题 添加题型下试题
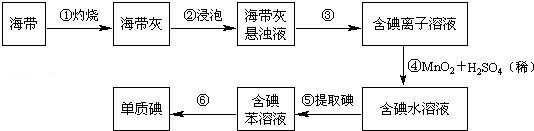
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤③的实验操作名称是
(3)步骤⑤是萃取、分液,某学生选择用苯来提取碘的理由是
A.直接将含碘苯溶液从分液漏斗上口倒出
B.直接将含碘苯溶液从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将含碘苯溶液从下口放出
D.先将水层从分液漏斗的下口放出,再将含碘苯溶液从上口倒出
五、填空题 添加题型下试题

(1)该“84消毒液”的物质的量浓度约为
(2)取用任意体积的该盐溶液时,下列物理量中会随所取体积的多少而变化的是
A.溶液中NaClO的物质的量B.溶液的浓度
C.溶液中NaClO的摩尔质量D.溶液的密度
(3)欲用NaOH固体配制950mL0.1 mol∙L−1的NaOH溶液,用托盘天平称取
六、解答题 添加题型下试题

(1)试剂Ⅰ的化学式为
(2)试剂Ⅱ的化学式为
(3)③中发生反应的化学方程式为
(4)由E得到KCl晶体的实验操作是
【知识点】 物质分离、提纯综合应用解读 离子的检验
试卷分析
试卷题型(共 30题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 实验安全 | |
| 2 | 0.85 | 仪器使用与实验安全 | |
| 3 | 0.85 | 仪器使用与实验安全 化学实验基础操作 | |
| 4 | 0.94 | 仪器使用与实验安全 常用仪器及使用 化学实验基础操作 过滤 | |
| 5 | 0.65 | 常用仪器及使用 化学实验基础操作 蒸发与结晶 | |
| 6 | 0.65 | 物质的分离、提纯 物质分离、提纯的常见物理方法 蒸馏与分馏 萃取和分液 | |
| 7 | 0.94 | 萃取和分液 | |
| 8 | 0.85 | 以N=m·NA/M为中心的有关基本粒子的推算 | |
| 9 | 0.85 | 摩尔质量 摩尔质量与相对原子质量区别与联系 | |
| 10 | 0.65 | 阿伏加德罗常数的求算 | |
| 11 | 0.85 | 阿伏加德罗定律 根据n=m/M的相关计算 | |
| 12 | 0.85 | 阿伏加德罗定律 气体摩尔体积概念 | |
| 13 | 0.85 | 阿伏加德罗常数的应用 | |
| 14 | 0.85 | 物质的量的含义 物质的量浓度概念、含义 物质的量有关计算 | |
| 15 | 0.94 | 阿伏加德罗定律 阿伏加德罗定律及其推论 阿伏加德罗定律的应用 | |
| 16 | 0.94 | 物质的量浓度概念、含义 | |
| 17 | 0.85 | 根据n=N/NA进行相关计算 依据物质的量浓度公式的基础计算 | |
| 18 | 0.65 | 物质的量浓度 | |
| 19 | 0.85 | 物质的量浓度的计算 依据物质的量浓度公式的基础计算 物质的量浓度计算-与溶质成分有关的计算 | |
| 20 | 0.85 | 氯离子的检验 硫酸根离子的检验 离子的检验 常见阴离子的检验 | |
| 21 | 0.4 | 离子反应在混合物分离、除杂中的应用 物质的分离、提纯 | |
| 22 | 0.65 | 物质分离、提纯的常见物理方法 物质分离、提纯的常见化学方法 | |
| 23 | 0.85 | 摩尔质量 物质的量有关计算 | |
| 24 | 0.85 | 摩尔质量 物质的量有关计算 | |
| 25 | 0.85 | 物质的量浓度的计算 物质的量浓度与溶质成分有关的计算 | |
| 二、解答题 | |||
| 26 | 0.85 | 物质分离、提纯的常见物理方法 蒸馏与分馏 萃取和分液 过滤 | 实验探究题 |
| 28 | 0.65 | 常用仪器及使用 物质分离、提纯综合应用 萃取和分液 海带中碘的提取及检验 | 实验探究题 |
| 30 | 0.85 | 物质分离、提纯综合应用 离子的检验 | 实验探究题 |
| 三、计算题 | |||
| 27 | 0.85 | 物质的量有关计算 根据n=N/NA进行相关计算 结合气体物质与NA相关推算 根据n=m/M进行相关计算 | |
| 四、填空题 | |||
| 29 | 0.85 | 物质的量浓度 依据物质的量浓度公式的基础计算 物质的量浓度计算-溶液配制有关计算 | |







