湖北省荆州市沙市区沙市中学2019-2020学年高一化学过关训练9《化学计量在实验中的应用》
湖北
高一
课后作业
2020-02-18
132次
整体难度:
适中
考查范围:
认识化学科学、化学实验基础
一、单选题 添加题型下试题
| A.CH4 | B.CO2 | C.H2S | D.N2 |
【知识点】 阿伏加德罗定律
| A.阿伏加德罗常数是12 g碳中所含的碳原子数 |
| B.阿伏加德罗常数是0.012 kg12C中所含的原子数 |
| C.阿伏加德罗常数是6.02×1023 |
| D.阿伏加德罗常数的符号为NA,近似为6.02×1023 |
【知识点】 阿伏加德罗常数的含义解读
| A.1mol任何纯净物都含有相同的原子数 |
| B.1mol O2中约含有6.02×1023个氧气分子 |
| C.1mol氢中含有2mol氢原子 |
| D.阿伏加 德罗常数就是6.02×1023 |
【知识点】 物质的量及单位——摩尔 物质的量的含义解读 摩尔解读 阿伏加德罗常数的含义解读
| A.ag | B.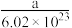 g g | C.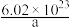 g g | D. g g |
【知识点】 阿伏加德罗常数的含义解读 摩尔质量的概念解读
 2H2↑+O2↑,某同学电解一定量的水,制得8 g H2,则该8 g H2的物质的量为
2H2↑+O2↑,某同学电解一定量的水,制得8 g H2,则该8 g H2的物质的量为| A.2 mol | B.4 mol | C.8 mol | D.89.6 mol |
【知识点】 根据n=m/M进行相关计算解读
| A.16 | B.64 |
| C.32 | D.96 |
| A.23:9 | B.16:9 | C.32:9 | D.46:9 |
| A.一定温度、压强下,气体体积由其分子的大小决定 |
| B.一定温度、压强下,气体体积由其物质的量的多少决定 |
| C.气体摩尔体积是指1mol任何气体所占的体积为22.4L |
| D.不同的气体,若体积不等,则它们所含的分子数一定不等 |
| A.1mol任何气体所占体积都约为22.4L |
| B.1mol H2O在标准状况下体积为22.4L |
| C.1mol气体体积为22.4L,则一定是标准状况 |
| D.气体摩尔体积不一定是22.4L/mol |
| A.在常温常压下,11.2LN2含有的分子数为 0.5NA |
| B.标准状况下,22.4LH2和O2的混合物所含分子数为NA |
| C.标准状况下,18gH2O 的体积是 22.4L |
| D.1molSO2的体积是 22.4L |
| A.3.36 L | B.2.24 L | C.4.48 L | D.6.72 L |
【知识点】 物质的量有关计算
| A.28 | B.60 | C.32 | D.44 |
【知识点】 阿伏加德罗定律的应用解读 根据n=m/M进行相关计算解读
| A.Wn | B.22.4n | C.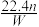 | D. |
【知识点】 阿伏加德罗常数的求算解读
A.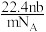 L L | B.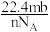 L L | C.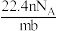 L L | D. L L |
【知识点】 阿伏加德罗定律的应用解读 根据n=N/NA进行相关计算解读
| A.1L水中溶解1mol H2SO4 |
| B.1L溶液中含有1molH+ |
| C.将98g H2SO4溶于1L水中配成溶液 |
| D.1L H2SO4溶液中含有98g H2SO4 |
【知识点】 物质的量浓度的计算 物质的量浓度的基础计算解读
A.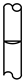 | B. | C. | D.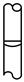 |
【知识点】 配制一定物质的量浓度的溶液的步骤、操作解读
| A.容量瓶用蒸馏水洗净后,可不经干燥直接用于配制溶液 |
| B.用分液的方法分离水和酒精的混合物 |
| C.配制1L0.1mol/L的NaCl溶液时可用托盘天平称量5.85gNaCl固体 |
| D.用滴管滴加液体时,为防止液滴飞溅,滴管紧贴试管内壁 |
| A.称取碳酸钠晶体100 g |
| B.定容时俯视观察刻度线 |
| C.移液时,对用于溶解碳酸钠晶体的烧杯没有进行冲洗 |
| D.定容后将容量瓶振荡均匀,静置发现液面低于刻度线,又加入少量水至刻度线 |
| A.H+ 的物质的量 | B.溶质的质量分数 |
| C.溶质的质量 | D.溶质的物质的量 |
【知识点】 物质的量浓度的基础计算解读
| A.1 000 mL溶液中所含K+、SO42-总数为0.3NA |
| B.500 mL溶液中有0.1NA个K+ |
| C.1 L溶液中K+的浓度为0.4 mol·L-1 |
| D.1 L溶液中SO42-的浓度是0.4 mol·L-1 |
【知识点】 物质的量有关计算
| A.0.5 mol/L | B.0.2 mol/L |
| C.0.45 mol/L | D.0.25 mol/L |
| A.1∶1∶1 | B.1∶2∶3 | C.3∶2∶1 | D.3∶4∶3 |
| A.1 mol∙L−1 | B.0.1 mol∙L−1 | C.0.01 mol∙L−1 | D.10 mol∙L−1 |
| A.12mL | B.25mL | C.20.8mL | D.12.5mL |
【知识点】 物质的量浓度计算-溶液稀释的有关计算解读



