云南省玉溪市江川二中2019-2020学年高一上学期期中考试化学试题
云南
高一
期中
2019-11-29
265次
整体难度:
适中
考查范围:
认识化学科学、化学与STSE、化学实验基础、常见无机物及其应用
一、单选题 添加题型下试题
| A.2.2 g CO2中含有的分子数为0.1NA |
| B.0.5 mol Na2CO3固体中含有的Na+数为0.5NA |
| C.Na2O2与足量水反应时,生成1 mol O2转移的电子数为2NA |
| D.标准状况下,2.24 L CCl4含有的碳原子数为0.2NA |
【知识点】 阿伏加德罗常数的求算解读 结合气体物质与NA相关推算解读
| A.金属材料大多有延展性,可以加工成各种形状 |
| B.金属材料大多有美丽的光泽 |
| C.废弃的金属不会造成土壤污染和水污染 |
| D.金属材料大多数可以回收再利用 |
A.KClO3是氧化剂 | B.H2O既不是氧化产物也不是还原产物 |
| C.HCl是还原剂 | D.KCl既是还原产物也是氧化产物 |
【知识点】 氧化还原反应基本概念 氧化还原反应的规律解读
| A.Fe3+→Fe2+ | B. → Mn2+ → Mn2+ |
| C.Cl-→Cl2 | D.N2O3→HNO2 |
【知识点】 氧化还原反应基本概念 氧化还原反应的定义及实质
| A.③④⑤⑥⑦ | B.①②⑦ | C.①④⑤⑥ | D.①④⑦ |
【知识点】 实验安全解读 化学科学对人类文明发展的意义解读
二、未知 添加题型下试题
三、单选题 添加题型下试题
| A.过滤时,玻璃棒与三层滤纸 |
| B.用量筒从食盐溶液中量出4.3 mL溶液 |
| C.过滤时,烧杯内壁与漏斗下端 |
| D.用胶头滴管向试管内滴加液体时,胶头滴管尖端与试管内壁 |
| A.24g NaH中阴离子所含电子总数为NA |
| B.1mol甲烷分子所含氢原子数为4NA |
| C.1mol碳酸氢钠固体中含有NA个CO32- |
| D.9g水中含有10NA个电子 |
| A.①③②④⑤ | B.①②③④⑤ | C.②③①⑤④ | D.③②①⑤④ |
| A.1.84 g | B.1.38 g | C.2.3 g | D.0.46 g |
| A.它是由Te、Zn、Cd按一定比例混合而成的,无固定的熔、沸点 |
| B.它易导电、导热,具有延展性 |
| C.它的熔、沸点比Zn的低 |
| D.它的硬度和强度比Cd的大 |
| A.CO2→CO | B.Cl﹣→Cl2 | C.Fe3+→Fe2+ | D.CO32—→CO2 |
【知识点】 氧化还原反应定义、本质及特征解读
| A.1 mol任何气体所占的体积都约是22.4 L |
| B.1 mol气体在非标准状况下的体积不可能是22.4 L |
| C.气体摩尔体积不仅适用于纯气体,也适用于混合气体 |
| D.0.3 mol氢气与0.7 mol 氧气的混合气体的体积约是22.4 L |
| A.钠在水层中反应并四处游动 |
| B.钠停留在苯层中不发生反应 |
| C.钠在苯的液面上反应并四处游动 |
| D.钠在苯与水的界面处反应并做上下跳动 |
| A.向试管中滴加溶液时,滴管尖嘴不能伸入试管内 |
| B.不能将滴管水平拿持 |
| C.加完药品后应将滴管洗净后再放回原瓶 |
| D.滴管除了原滴瓶外,不能放在别的地方 |
【知识点】 仪器使用与实验安全
| A.石灰水与盐酸的反应 OH﹣+H+===H2O |
| B.氧化铜与盐酸反应 O2﹣+2H+===H2O |
| C.铜片插入硝酸银溶液中 Cu+Ag+===Cu2++Ag |
| D.碳酸钙溶于醋酸中 CaCO3+2H+===Ca2++H2O+CO2↑ |
| A.100mL | B.500mL | C.1000mL | D.1500mL |
【知识点】 氢氧化铝
| A.1 mol∙L−1 | B.0.1 mol∙L−1 | C.0.01 mol∙L−1 | D.10 mol∙L−1 |
| A.排除碳酸根离子的干扰 | B.排除硫酸根离子的干扰 |
| C.生成白色沉淀 | D.排除硝酸根离子的干扰 |
| A.氧化铁与醋酸:Fe2O3+6H+===2Fe3++3H2O |
| B.碳酸钠与盐酸:Na2CO3+2H+===2Na++CO2↑+H2O |
| C.铁片插入到硫酸铜溶液中:2Fe+3Cu2+===2Fe3++3Cu |
| D.向盐酸中加入适量氨水:H++NH3·H2O===NH4++H2O |
【知识点】 离子方程式的正误判断解读
| A.Fe、Cu、Al、Ag、Mg | B.Mg、Cu、Al、Ag、Fe |
| C.Mg、Cu、Al、Fe、Ag | D.Al、Cu、Mg、Ag、Fe |
| A.盐卤可用于制豆腐 | B.活性炭作吸附剂 |
| C.以无水酒精作外科消毒剂 | D.明矾作净水剂 |
四、填空题 添加题型下试题
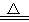 MnCl2 + Cl2↑+ 2H2O
MnCl2 + Cl2↑+ 2H2O(1)用
(2)在该反应中,如有1 mol Cl2生成,被氧化的HCl的物质的量是
(3)某温度下,将Cl2通入NaOH溶液中,反应得到含有ClO-与ClO3-物质的量之比为1∶1的混合液,反应的化学方程式是
(4)报纸报道了多起卫生间清洗时,因混合使用“洁厕灵”(主要成分是盐酸)与“84消毒液”(主要成分是NaClO)发生氯气中毒的事件。试根据你的化学知识分析,原因是(用离子方程式表示)
五、解答题 添加题型下试题

实验记录如下:
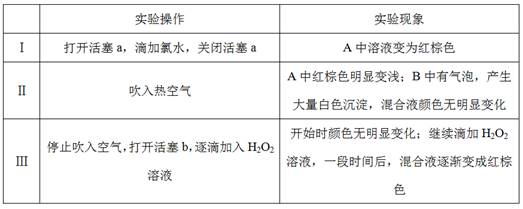
请回答下列问题:
(1)A中反应的离子方程式是
(2)实验操作Ⅱ吹入热空气的目的是
(3)装置C的作用是
(4)实验操作Ⅲ,混合液逐渐变成红棕色,其对应的离子方程式
(5)由上述实验得出的结论是
(6)实验反思:
①有同学认为实验操作Ⅱ吹入的热空气,会干扰(5)中结论的得出,你认为是否干扰,理由是
②实验操作Ⅲ,开始时颜色无明显变化的原因是(写出一条即可):
六、填空题 添加题型下试题

(1)实验甲在加热过程中能观察到产生白色沉淀的烧杯是
(2)实验乙用来探究Na2O2与CO2的反应,观察到的实验现象为包有Na2O2的棉花着火。写出Na2O2与CO2反应的化学方程式:
(3)取10 g碳酸钠和碳酸氢钠的混合物充分加热,将生成的CO2气体通入足量的澄清石灰水中,测得生成沉淀的质量为4.0 g。则原混合物中碳酸钠的质量分数为
七、解答题 添加题型下试题
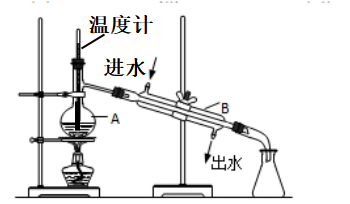
①写出仪器的名称:A.
②实验时A中除加入自来水外,还需加入少量
③改正图中两处明显的错误。
ⅰ
ⅱ
④收集完蒸馏水后,是先撤酒精灯还是先停冷凝水?
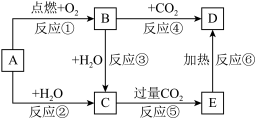
请填写下列空白:
(1)写出化学式:A
(2)以上反应中属于氧化还原反应的有
(3)写出A→C反应的离子方程式
试卷分析
试卷题型(共 30题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 阿伏加德罗常数的求算 结合气体物质与NA相关推算 | |
| 2 | 0.85 | 无机物质的分类 单质和化合物 | |
| 3 | 0.94 | 金属材料 金属与合金性能比较 金属材料的应用 | |
| 4 | 0.85 | 氧化还原反应基本概念 氧化还原反应的规律 | |
| 5 | 0.94 | 氧化还原反应基本概念 氧化还原反应的定义及实质 | |
| 6 | 0.85 | 实验安全 化学科学对人类文明发展的意义 | |
| 8 | 0.85 | 仪器使用与实验安全 化学实验基础操作 | |
| 9 | 0.85 | 阿伏加德罗常数的求算 阿伏加德罗常数的应用 结合物质结构基础知识与NA相关推算 以N=m·NA/M为中心的有关基本粒子的推算 | |
| 10 | 0.85 | 仪器使用与实验安全 蒸发与结晶 | |
| 11 | 0.65 | 钠与水反应原理 铝盐与强碱溶液反应 | |
| 12 | 0.85 | 金属材料的性质及利用 金属与合金性能比较 常见合金的组成 金属材料的应用 | |
| 13 | 0.85 | 氧化还原反应定义、本质及特征 | |
| 14 | 0.85 | 阿伏加德罗定律 22.4L/mol适用条件 阿伏加德罗定律及其推论 | |
| 15 | 0.65 | 钠与水反应原理 | |
| 16 | 0.85 | 分散系概念及其分类 | |
| 17 | 0.94 | 仪器使用与实验安全 | |
| 18 | 0.4 | 离子反应概念 离子反应的发生条件 离子方程式的书写 离子方程式的正误判断 | |
| 19 | 0.65 | 氢氧化铝 | |
| 20 | 0.85 | 物质的量浓度概念、含义 物质的量浓度的计算 依据物质的量浓度公式的基础计算 物质的量浓度计算-溶液稀释的有关计算 | |
| 21 | 0.65 | 离子反应在混合物分离、除杂中的应用 常见阴离子的检验 | |
| 22 | 0.85 | 常见氧化剂与还原剂 | |
| 23 | 0.65 | 离子方程式的正误判断 | |
| 24 | 0.85 | 常见金属的活动性顺序及其应用 铝与强碱溶液反应 铁的物理性质 | |
| 25 | 0.85 | 胶体的性质和应用 明矾的净水作用及原理 化学科学对人类文明发展的意义 | |
| 二、未知 | |||
| 7 | 0.85 | 氧化性、还原性强弱的比较 氧化还原反应的规律 | 未知 |
| 三、填空题 | |||
| 26 | 0.65 | 阿伏加德罗常数的应用 离子方程式的书写 单线桥、双线桥分析氧化还原反应 氧化还原反应在生活、生产中的应用 | |
| 28 | 0.85 | 过氧化钠 碳酸钠 碳酸氢钠 | |
| 四、解答题 | |||
| 27 | 0.65 | 氯气与还原性化合物的反应 溴、碘的性质 物质性质实验方案的设计 | 实验探究题 |
| 29 | 0.65 | 蒸馏与分馏 | 实验探究题 |
| 30 | 0.65 | 无机综合推断 钠 焰色试验 过氧化钠 | 无机推断题 |



