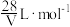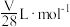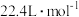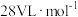陕西省西安市周至县第四中学2021-2022学年高一上学期期中考试化学试题
陕西
高一
期中
2022-12-22
69次
整体难度:
较易
考查范围:
化学实验基础、认识化学科学、常见无机物及其应用
一、单选题 添加题型下试题
| A | B | C | D | |
| 物质化学式 | H2SO4(浓) | C2H5OH(酒精) | Hg(汞) | NaCl |
| 危险警告标签 |  |  |  |  |
| A.A | B.B | C.C | D.D |
| A.同质量、不同密度的N2和CO |
| B.同温度、同体积的H2和N2 |
| C.同体积、同密度的C2H6和NO |
| D.同压强、同体积的N2O和CO2 |
【知识点】 阿伏加德罗定律及其推论解读
| A.在冶金厂和水泥厂常用高压电除去大量的烟尘,以减少其对空气的污染 |
| B.将植物油倒入水中用力振荡形成油水混合物 |
| C.清晨,阳光穿过茂密的林木枝叶所产生的美丽的光柱 |
| D.在Fe(OH)3胶体中滴入稀硫酸,先看到红褐色沉淀生成而后沉淀溶解 |
 2 KCl+ 3 O2↑ ,反应后从剩余物中回收二氧化锰的操作顺序正确的是(已知MnO2为黑色难溶于水的固体)
2 KCl+ 3 O2↑ ,反应后从剩余物中回收二氧化锰的操作顺序正确的是(已知MnO2为黑色难溶于水的固体)| A.溶解、蒸发、洗涤、过滤 | B.溶解、过滤、蒸发、洗涤 |
| C.溶解、过滤、洗涤、干燥 | D.溶解、洗涤、过滤、加热 |
【知识点】 物质分离、提纯综合应用解读
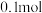 的氯化钠固体配成溶液500ml,所得溶液的物质的量浓度为
的氯化钠固体配成溶液500ml,所得溶液的物质的量浓度为

A.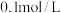 | B.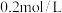 | C. | D. |
【知识点】 物质的量浓度的计算 一定物质的量浓度的溶液的配制
| A.0.3mol·L-1 | B.0.45mol·L-1 | C.0.15mol·L-1 | D.0.2mol·L-1 |
①玻璃棒 ②烧杯 ③烧瓶 ④量筒 ⑤容量瓶
| A.①②③④ | B.①②④⑤ | C.②③④⑤ | D.①③④⑤ |
| A.0.05mol·L-1 | B.0.25mol·L-1 | C.0.1mol·L-1 | D.0.5mol·L-1 |
【知识点】 物质的量浓度计算-溶液稀释的有关计算解读
| A.容量瓶(100mL) | B.托盘天平 | C.烧杯 | D.胶头滴管 |
| A.酸、碱、盐都是电解质,电解质只有酸、碱、盐 |
| B.电离时生成的阴离子全部是OH-的化合物才可能是碱 |
| C.电离时生成的阳离子全部是H+的化合物才可能是酸 |
| D.只要电离时能生成金属阳离子和酸根阴离子的化合物就是盐 |
【知识点】 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系解读
| A.所有蒸馏操作中都必须用到温度计 |
| B.蒸馏自来水可以制得蒸馏水 |
| C.蒸馏烧瓶使用前一般不需要检漏 |
| D.进行蒸馏操作时,应向蒸馏烧瓶中加入几块碎瓷片,防止暴沸 |
| A.1 mol∙L−1 | B.0.1 mol∙L−1 | C.0.01 mol∙L−1 | D.10 mol∙L−1 |
①纯碱 ②食盐水 ③石灰水 ④NaOH ⑤液态氨 ⑥KClO3
| A.碱—①④ | B.纯净物—③④⑤ |
| C.盐—①⑥ | D.混合物—②⑤ |
【知识点】 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系解读
| A.用容量瓶配制溶液前应将其干燥 |
| B.用容量瓶配制溶液前应用欲配制的溶液润洗 |
| C.容量瓶可用来长期贮存溶液 |
| D.容量瓶不能用作溶解固体、稀释浓溶液的容器 |
| A.明矾能生成氢氧化铝胶体,可用作净水剂 |
| B.用可见光束照射可区别溶液和胶体 |
| C.用石膏或盐卤点制豆腐与胶体的性质有关 |
| D.稀豆浆、淀粉溶液、氯化铁溶液都为胶体 |
【知识点】 胶体的性质和应用解读 明矾的净水作用及原理解读
| A.饱和碘水和CCl4加入分液漏斗中后,塞上上口部的塞子,用右手压住分液漏斗上口部,左手握住活塞部分,把分液漏斗倒转过来振荡 |
| B.静置,待分液漏斗中液体分层后,先使分液漏斗内外空气相通(准备放出液体) |
| C.打开分液漏斗的活塞,使全部下层液体沿盛接液体的烧杯内壁慢慢流出 |
| D.最后继续打开活塞,另用容器盛接并保存上层液体 |
| A.汽油和水、四氯化碳和水 | B.汽油和水、苯和水 |
| C.食用油和水、醋酸和水 | D.葡萄糖和水、酒精和水 |
【知识点】 物质分离、提纯的常见物理方法 萃取和分液解读
序号 | A | B | C | D |
实验目的 | 分离食盐水与泥沙 | 分离水和CCl4 | 制取蒸馏水 | 从浓食盐水中得到氯化钠晶体 |
分离方法 | 过滤 | 萃取 | 蒸馏 | 蒸发 |
选用仪器 |
|
|
|
|
| A.A | B.B | C.C | D.D |
【知识点】 物质分离、提纯的常见物理方法
| A.3mol/L | B.0.2mol/L | C.0.3mol/L | D.0.1mol/L |
【知识点】 物质的量浓度
| A.1 mol任何物质都含有阿伏加德罗常数个分子 |
| B.阿伏加德罗常数就是1 mol粒子的粒子数,0.012 kg 12C 中含有约6.02×1023个 12C |
| C.摩尔是一个基本的物理量 |
| D.1 mol水中含有2 mol氢和1 mol氧 |
| A.1 mol CO2的质量为44 g/mol |
| B.CO2的摩尔质量为44 g |
| C.CO2的摩尔质量等于CO2的相对分子质量 |
| D.NA个CO2的质量与CO2的相对分子质量在数值上相同 |
【知识点】 摩尔质量 摩尔质量与相对原子质量区别与联系解读
A.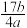 | B.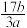 |
C.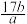 | D.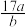 |
| A.静电除尘器除去空气或工厂废气中的飘尘是利用胶体粒子的带电性而加以除去 |
| B.明矾净水是利用胶体的吸附性除去杂质 |
| C.将“纳米材料”分散到某液体中,用滤纸过滤的方法可以将“纳米材料”从此分散系中分离出来 |
| D.烟、雾属于胶体,能产生丁达尔效应 |
| A.2.4g金属镁变成镁离子时失去的电子数为0.1NA |
| B.2g氢气中含有的原子数为NA |
| C.3.01×1023个氮分子中含有的原子数为2NA |
| D.17g氨气中含有的电子数为10NA |
【知识点】 阿伏加德罗常数的求算解读 阿伏加德罗常数的应用解读
| A.丁达尔效应 | B.胶体是混合物 |
| C.胶体粒子大小在1~100nm之间 | D.胶体的分散剂为气体 |
【知识点】 胶体

| A.氯化镁固体是非电解质 |
| B.氯化镁溶液是电解质 |
| C.氯化镁在水溶液中电离产生自由移动的离子 |
| D.氯化镁只有在溶液中才能导电 |
| A.0.21 mol·L-1 | B.0.42 mol·L-1 |
| C.0.56 mol·L-1 | D.0.26 mol·L-1 |
二、解答题 添加题型下试题
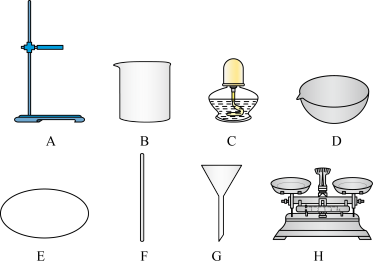
(1)D的名称是
(2)提纯的步骤是:溶解、过滤、
(3)“过滤”操作的要点可概括为“一贴、二低、三靠”,其中“二低”的含义是
(4)实验小组通过正确的计算发现,所得实验结果与该粗盐的实际含量对比,实验测得的结果比实际偏低,请分析可能的原因:
三、填空题 添加题型下试题
(1)实验步骤如下:
①计算:需要NaOH固体质量为
②称量:用托盘天平称取NaOH固体,称量时要注意两个问题:一要装在烧杯里称,二要迅速。
③溶解:用量筒量取蒸馏水注入烧杯里,搅拌。
④冷却:将溶液冷却至室温。
⑤移液:将冷却溶液用
⑥洗涤:用适量蒸馏水洗涤烧杯和玻璃棒
⑦振荡:手持容量瓶轻轻振荡,使溶液充分混合均匀。
⑧定容:继续加蒸馏水至距刻度线
⑨摇匀:盖好玻璃塞,反复上下颠倒,使溶液混合均匀。
(2)在配制过程中,下列实验操作对所配制的NaOH溶液的物质的量浓度有何影响?(在横线上填“偏大”“偏小”或“无影响”)。
①定容时俯视
②定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
③配制溶液前,所用的容量瓶还有少量水
四、计算题 添加题型下试题
(1)用NA表示阿伏加德罗常数的值,则0.2 mol NH3中所含氢原子数与
(2)含0.4 mol Al3+的Al2(SO4)3中所含的
 的物质的量是
的物质的量是(3)已知16 g A和20 g B恰好完全反应生成0.04 mol C和31.76 g D,则C的摩尔质量为
【知识点】 物质的量有关计算 根据n=m/M进行相关计算解读
五、填空题 添加题型下试题
(1)HCl:
(2)H2SO4:
(3)Ca(OH)2:
(4)KOH:
六、计算题 添加题型下试题
(1)生成标况下的氢气的体积是多少升?
(2)盐酸的物质的量的浓度是多少?
试卷分析
试卷题型(共 35题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 仪器使用与实验安全 实验安全 | |
| 2 | 0.65 | 阿伏加德罗定律及其推论 | |
| 3 | 0.94 | 胶体 胶体的性质和应用 | |
| 4 | 0.85 | 气体摩尔体积 气体摩尔体积概念 物质的量有关计算 | |
| 5 | 0.65 | 物质分离、提纯综合应用 | |
| 6 | 0.94 | 物质的量浓度的计算 一定物质的量浓度的溶液的配制 | |
| 7 | 0.65 | 物质的量浓度的计算 物质的量浓度计算-与溶质成分有关的计算 | |
| 8 | 0.85 | 配制一定物质的量浓度的溶液的步骤、操作 配制一定物质的量浓度的溶液实验的仪器 配制一定物质的量浓度溶液的综合考查 | |
| 9 | 0.65 | 物质的量浓度计算-溶液稀释的有关计算 | |
| 10 | 0.85 | 一定物质的量浓度的溶液的配制 配制一定物质的量浓度的溶液实验的仪器 配制一定物质的量浓度溶液的综合考查 | |
| 11 | 0.65 | 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系 | |
| 12 | 0.85 | 仪器使用与实验安全 常用仪器及使用 化学实验基础操作 实验安全 | |
| 13 | 0.85 | 物质的量浓度概念、含义 物质的量浓度的计算 依据物质的量浓度公式的基础计算 物质的量浓度计算-溶液稀释的有关计算 | |
| 14 | 0.85 | 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系 | |
| 15 | 0.85 | 仪器使用与实验安全 配制一定物质的量浓度的溶液实验的仪器 | |
| 16 | 0.85 | 胶体的性质和应用 明矾的净水作用及原理 | |
| 17 | 0.85 | 仪器使用与实验安全 萃取和分液 | |
| 18 | 0.85 | 物质分离、提纯的常见物理方法 萃取和分液 | |
| 19 | 0.85 | 物质分离、提纯的常见物理方法 | |
| 20 | 0.65 | 物质的量浓度 | |
| 21 | 0.65 | 阿伏加德罗常数 物质的量的含义 | |
| 22 | 0.94 | 分散系概念及其分类 | |
| 23 | 0.85 | 摩尔质量 摩尔质量与相对原子质量区别与联系 | |
| 24 | 0.85 | 阿伏加德罗常数 阿伏加德罗常数的求算 结合物质结构基础知识与NA相关推算 | |
| 25 | 0.85 | 分散系概念及其分类 胶体的性质和应用 | |
| 26 | 0.85 | 阿伏加德罗常数的求算 阿伏加德罗常数的应用 | |
| 27 | 0.85 | 胶体 | |
| 28 | 0.65 | 电解质与非电解质 电解质的电离 物质水溶液的导电性 综合实验设计与评价 | |
| 29 | 0.94 | 分散系概念及其分类 胶体的性质和应用 | |
| 30 | 0.65 | 物质的量浓度的计算 物质的量浓度计算-溶液混合的有关计算 | |
| 二、解答题 | |||
| 31 | 0.85 | 常用仪器及使用 化学实验基础操作 蒸发与结晶 过滤 | 实验探究题 |
| 三、填空题 | |||
| 32 | 0.65 | 配制一定物质的量浓度的溶液的步骤、操作 配制一定物质的量浓度的溶液实验的误差分析 | |
| 34 | 0.94 | 电离方程式 | |
| 四、计算题 | |||
| 33 | 0.65 | 物质的量有关计算 根据n=m/M进行相关计算 | |
| 35 | 0.85 | 22.4L/mol适用条件 根据n=m/M进行相关计算 化学方程式计算中物质的量的运用 依据物质的量浓度公式的基础计算 | |