云南省峨山彝族自治县峨山一中2018-2019学年高二入学考试化学试题
云南
高二
阶段练习
2018-09-17
395次
整体难度:
适中
考查范围:
认识化学科学、化学实验基础、常见无机物及其应用、化学反应原理、有机化学基础、物质结构与性质
一、单选题 添加题型下试题
| A.K+、Na+、Br﹣、SO42- | B.Na+、Ba2+、ClO﹣、Cl﹣ |
| C.Ca2+、Cl﹣、HCO3-、K+ | D.NH4+、K+、OH﹣、SO42- |
【知识点】 物质共存解读 限定条件下的离子共存解读
| A.饱和碘水和CCl4加入分液漏斗中后,塞上上口部的塞子,用右手压住分液漏斗上口部,左手握住活塞部分,把分液漏斗倒转过来振荡 |
| B.静置,待分液漏斗中液体分层后,先使分液漏斗内外空气相通(准备放出液体) |
| C.打开分液漏斗的活塞,使全部下层液体沿盛接液体的烧杯内壁慢慢流出 |
| D.最后继续打开活塞,另用容器盛接并保存上层液体 |
| A.RCl | B.RCl2 | C.RCl3 | D.RCl4 |
【知识点】 物质的量有关计算 探究物质组成或测量物质的含量解读
| A.① |
| B.①② |
| C.①③ |
| D.①②③ |
| A.烧碱 | B.干冰 | C.金刚石 | D.75%的酒精 |
【知识点】 电解质与非电解质 非电解质、电解质物质类别判断解读
| A.分子数之比为1∶1 | B.原子数之比为1∶1 | C.电子数之比3∶2 | D.物质的量之比2∶3 |
【知识点】 以N=m·NA/M为中心的有关基本粒子的推算解读
| A.2∶1∶1 | B.4∶2∶1 | C.1∶1∶1 | D.1∶2∶1 |
【知识点】 某溶液与物质的量浓度相关的物理量的判断解读
| A.液态HCl不导电,所以HCl是非电解质 |
| B.NH3的水溶液能导电,所以NH3是电解质 |
| C.铜、石墨均能导电,所以它们都是电解质 |
| D.蔗糖在水溶液中和熔融时都不导电,所以是非电解质 |
【知识点】 电解质、非电解质概念解读 非电解质、电解质物质类别判断解读
| A.用鼻子对着盛有氯气的瓶口,就可以嗅到氯气的气味 |
| B.用向下排空气法可以收集到纯净的氯气 |
| C.贮氯罐意外泄漏,应沿逆风方向疏散群众 |
| D.氯气车间液氯泄漏时,应弯腰逃离氯气泄漏区域 |
【知识点】 氯气的物理性质解读 氯气的化学性质 物质性质实验方案的设计解读

| A.A | B.B | C.B | D.D |
【知识点】 物质的分离、提纯 物质分离、提纯综合应用解读
| A.X为酸、Y为碱 | B.X为碱性氧化物、Y为酸 |
| C.X为盐、Y为碱 | D.X为碱性氧化物、Y为酸性氧化物 |
【知识点】 分类方法的应用解读 化学反应原理综合考查解读
| A.氯化氢 | B.次氯酸钠 | C.高锰酸钾 | D.碳酸钠 |
| A.Al3+、Na+、Cl﹣、OH﹣ | B.Fe2+、Mg2+、SO42—、Cl﹣ |
| C.K+、Na+、CO32—、OH﹣ | D.Na+、Ba2+、HCO3—、OH﹣ |
【知识点】 离子共存 限定条件下的离子共存解读
| A.H+和CO32− | B.HCO3−和HSO4− |
| C.Na+、HCO3−和H+ | D.HCO3−和H+ |
【知识点】 离子反应的发生及书写 离子方程式的书写解读
| A.苯分子中碳原子间形成的碳碳键完全相同 |
| B.苯分子中形成共价键的夹角都是120° |
| C.苯分子中6个碳原子位于同一平面内 |
| D.苯分子中的碳原子与氢原子不在同一平面内 |
【知识点】 苯的组成与结构
| A.1 mol乙醇与足量钠反应放出0.5 mol氢气 |
| B.1 mol乙醇完全燃烧需要3 mol氧气 |
| C.1 mol生成2 mol二氧化碳和3 mol水 |
| D.4.6 g乙醇在标准状况下的体积为2.24 L |
【知识点】 通过定量实验确定有机结构式解读
| A.位于元素周期表ⅡA族左边的元素一定属于主族元素 |
| B.氯元素位于元素周期表中第三周期ⅦA族 |
| C.元素周期表中ⅢB族到ⅡB族10个纵行的元素都是金属元素 |
| D.目前使用的元素周期表中,包含元素种类最多的族为ⅥA |
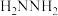 )是一种高能燃料,有关化学反应的能量变化如图所示。已知断裂1mol化学键所需的能量(kJ):N
)是一种高能燃料,有关化学反应的能量变化如图所示。已知断裂1mol化学键所需的能量(kJ):N N键为942、O=O键为500、N-N键为154,则断裂1molN-H键所需的能量是
N键为942、O=O键为500、N-N键为154,则断裂1molN-H键所需的能量是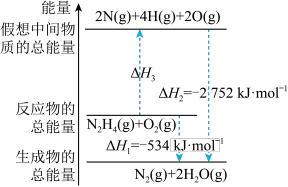
| A.194kJ | B.391kJ | C.516kJ | D.658kJ |
2H2O=2H2↑+O2↑。下列说法正确的是( )
| A.水的分解反应是放热反应 | B.此反应是把化学能转化为热能而储存起来 |
| C.使用氢气作燃料有助于控制温室效应 | D.在这一反应中,热能转化为化学能 |
【知识点】 能量的相互转化
| A.H2SO4、Ba(OH)2、CaCl2、MgO |
| B.NaBr、KNO3、Ca(OH)2、SiO2 |
| C.NaOH、CaO、HCl、CH3COONa |
| D.KOH、(NH4)2SO4、Na2O2、NaH |
【知识点】 酸、碱、盐、氧化物的概念及其相互联系解读
 ,氮原子结构示意图为
,氮原子结构示意图为 。则氮化镓的化学式是( )
。则氮化镓的化学式是( )| A.Ga3N2 | B.Ga2N3 | C.GaN | D.Ga5N3 |
【知识点】 物质结构与性质综合考查解读

| A.最简单气态氢化物的热稳定性:R>Q | B.最高价氧化物对应水化物的酸性:W<Q |
| C.原子半径:T>Q>R | D.T的最高价氧化物水化物具有两性 |
| A.从锂→铯密度逐渐增大 | B.在钠、钾、铯三种单质中,铯的熔点最低 |
| C.铷的密度比钾大,熔点比钾高 | D.金属钫的熔点比金属钠的熔点高 |
| A.用相同浓度但温度较高的盐酸代替常温下的盐酸 |
| B.增大反应体系的压强或减小反应体系的压强 |
| C.改用相同质量但为粉末状态的碳酸钙代替块状碳酸钙 |
| D.改用与原盐酸含有相同氢离子浓度的稀硫酸 |
【知识点】 影响化学反应速率的因素
| A.阴、阳离子间通过静电引力形成离子键 |
| B.阴、阳离子间通过离子键一定能形成离子化合物 |
| C.离子化合物都能导电,它们都是电解质 |
| D.只有活泼金属元素和活泼非金属元素化合时,才能形成离子键 |

A.反应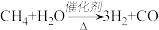 ,每消耗1mol CH4转移12mol 电子 ,每消耗1mol CH4转移12mol 电子 |
| B.电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O |
| C.电池工作时,CO32-向电极B移动 |
| D.电极B上发生的电极反应为:O2+2CO2+4e-=2CO32- |
【知识点】 原电池电极反应式书写解读 燃料电池
 LaNi5+6Ni(OH)2。关于镍氢电池放电时的下列说法中不正确的是( )
LaNi5+6Ni(OH)2。关于镍氢电池放电时的下列说法中不正确的是( )| A.储氢合金作负极 |
| B.正极反应式:6NiO(OH)+6H2O+6e-=6Ni(OH)2+6OH- |
| C.负极反应式:LaNi5H6+6OH--6e-=LaNi5+6H2O |
| D.电子由正极通过外电路流向负极 |
【知识点】 原电池 原电池电极反应式书写解读
| A.C4H10 | B.C5H10 | C.C6H12 | D.C6H14 |
【知识点】 根据元素种类、原子个数、有机物类别确定分子式解读
二、解答题 添加题型下试题

已知:各离子开始沉淀及完全沉淀时的pH如表所示:
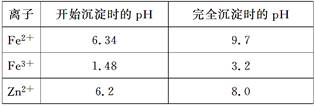
请回答下列问题:
(1)在“酸浸”步骤中,为提高浸出速率,除通入空气“搅拌”外,还可采取的措施是(任写一点即可)
(2)物质A最好使用下列物质中的
A.KMnO4 B.H2O2 C.HNO3
(3)除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在
(4)物质B可直接用作氮肥,则B的化学式是
(5)除铁后得到的氢氧化铁可用次氯酸钾溶液在碱性环境将其氧化得到一种高效的多功能处理剂(K2FeO4),写出该反应的离子方程式:
三、计算题 添加题型下试题
(1)该混合气体倒立于水中发生反应的化学方程式是
(2)若a=
 V,则原混合气体中氮气与二氧化氮的体积之比是
V,则原混合气体中氮气与二氧化氮的体积之比是(3)结合第(2)小题,向aL气体中通入氧气至试管中刚好只有一种气体时,停止通入氧气。
①试管中最终剩余的气体是
②该过程中总反应的化学方程式是
【知识点】 氮氧化物溶解于水的相关计算解读 物质含量的测定
四、解答题 添加题型下试题
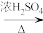 CH2=CH2↑+H2O),将生成的气体直接通入溴水中,发现溶液褪色,即证明乙烯与溴水发生了加成反应。(已知:乙烯可以被浓硫酸氧化,有SO2生成)
CH2=CH2↑+H2O),将生成的气体直接通入溴水中,发现溶液褪色,即证明乙烯与溴水发生了加成反应。(已知:乙烯可以被浓硫酸氧化,有SO2生成)乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量还原性的杂质气体,由此提出必须先除去杂质,再与溴水反应。
请你回答下列问题:
(1)甲同学设计的实验
A.使溴水褪色的反应,未必是加成反应
B.使溴水褪色的反应,就是加成反应
C.使溴水褪色的物质,未必是乙烯
D.使溴水褪色的物质,就是乙烯
(2)乙同学推测此乙烯中必定含有一种杂质气体是
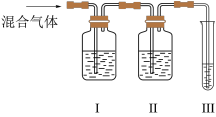
请回答:Ⅰ、Ⅱ、Ⅲ装置中可盛放的试剂是:Ⅰ
A.品红 B.NaOH溶液
C.溴水 D.酸性高锰酸钾溶液
(3)为验证这一反应是加成反应而不是取代反应,丙同学提出可用pH试纸来测试反应后溶液的酸性,理由是

(1)推断各符号所代表的物质的化学式:
A
(2)分别写出反应②、⑤的化学方程式:
②
⑤
(3)写出反应③的离子方程式
【知识点】 无机综合推断 氧化钠物理性质及用途解读
五、填空题 添加题型下试题
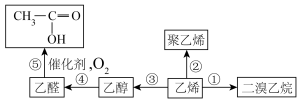
按下列要求写出:
(1)聚乙烯的结构简式是
(2)反应①的化学方程式是
(3)反应③的化学方程式是
(4)反应⑤的化学方程式是
试卷分析
试卷题型(共 35题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 物质共存 限定条件下的离子共存 | |
| 2 | 0.85 | 仪器使用与实验安全 萃取和分液 | |
| 3 | 0.65 | 物质的量有关计算 探究物质组成或测量物质的含量 | |
| 4 | 0.85 | 阿伏加德罗常数 摩尔质量的概念 根据n=N/NA进行相关计算 以N=m·NA/M为中心的有关基本粒子的推算 | |
| 5 | 0.85 | 电解质与非电解质 非电解质、电解质物质类别判断 | |
| 6 | 0.85 | 以N=m·NA/M为中心的有关基本粒子的推算 | |
| 7 | 0.85 | 某溶液与物质的量浓度相关的物理量的判断 | |
| 8 | 0.85 | 电解质、非电解质概念 非电解质、电解质物质类别判断 | |
| 9 | 0.94 | 氯气的物理性质 氯气的化学性质 物质性质实验方案的设计 | |
| 10 | 0.65 | 物质的分离、提纯 物质分离、提纯综合应用 | |
| 11 | 0.65 | 分类方法的应用 化学反应原理综合考查 | |
| 12 | 0.65 | 分类方法的应用 | |
| 13 | 0.94 | 漂白粉和漂粉精 盐类水解的应用 | |
| 14 | 0.65 | 离子共存 限定条件下的离子共存 | |
| 15 | 0.65 | 离子反应的发生及书写 离子方程式的书写 | |
| 16 | 0.85 | 苯的组成与结构 | |
| 17 | 0.65 | 通过定量实验确定有机结构式 | |
| 18 | 0.85 | 元素周期表结构 元素周期表的应用 元素周期表结构分析 | |
| 19 | 0.65 | 根据△H=反应物的键能之和-生成物的键能之和进行计算 | |
| 20 | 0.65 | 能量的相互转化 | |
| 21 | 0.65 | 酸、碱、盐、氧化物的概念及其相互联系 | |
| 22 | 0.85 | 物质结构与性质综合考查 | |
| 23 | 0.65 | 原子的基本构成 | |
| 24 | 0.65 | 金属与非金属在周期表中位置及其性质递变的规律 结合物质计算的元素周期律、元素周期表相关推断 | |
| 25 | 0.65 | 同主族元素性质递变规律 同主族元素性质递变规律理解及应用 | |
| 26 | 0.65 | 影响化学反应速率的因素 | |
| 27 | 0.65 | 化学键基本概念 离子键概念及判断 | |
| 28 | 0.65 | 原电池电极反应式书写 燃料电池 | |
| 29 | 0.4 | 原电池 原电池电极反应式书写 | |
| 30 | 0.65 | 根据元素种类、原子个数、有机物类别确定分子式 | |
| 二、解答题 | |||
| 31 | 0.4 | 溶度积常数相关计算 物质分离、提纯综合应用 物质制备的探究 | 实验探究题 |
| 33 | 0.65 | 乙烯的加成反应 乙烯与溴水反应的实验 乙醇的消去反应 | 实验探究题 |
| 34 | 0.65 | 无机综合推断 氧化钠物理性质及用途 | 无机推断题 |
| 三、计算题 | |||
| 32 | 0.4 | 氮氧化物溶解于水的相关计算 物质含量的测定 | |
| 四、填空题 | |||
| 35 | 0.65 | 乙烯的加成反应 聚乙烯结构及应用 乙醇催化氧化 乙醛的催化氧化反应 | |

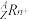 ,则元素R的原子序数是。
,则元素R的原子序数是。

