云南省剑川县第一中学2019-2020学年高一上学期期末考试化学试题
云南
高一
期末
2020-01-17
408次
整体难度:
适中
考查范围:
常见无机物及其应用、认识化学科学、化学实验基础、化学与STSE
一、单选题 添加题型下试题
①Cu+2H2SO4(浓)===CuSO4+SO2↑+2H2O
②C+2 H2SO4(浓)===CO2↑+2SO2↑+2H2O
③8NH3+3Cl2===6NH4Cl+N2
④3NO2+H2O===2HNO3+NO
| A.①② | B.①④ | C.③④ | D.全部 |
| A.酒精灯不使用时,必须盖上灯帽 |
| B.给试管里的固体加热时,试管口应略向下倾斜,外壁干燥后再加热 |
| C.给试管里的液体加热时,试管口略向上倾斜(约45°),外壁干燥后再加热 |
| D.用H2还原CuO时,应先通一会儿H2,再加热CuO |
【知识点】 仪器使用与实验安全
| A.分子数之比为1∶1 | B.原子数之比为1∶1 | C.电子数之比3∶2 | D.物质的量之比2∶3 |
【知识点】 以N=m·NA/M为中心的有关基本粒子的推算解读
| A.S2O32-是还原剂 | B.Y的化学式为Fe2O3 |
| C.a=4 | D.每有1molO2参加反应,转移的电子总数为4mol |
【知识点】 氧化还原反应的应用
| A.因为二氧化硫具有漂白性,所以它能使品红溶液、溴水、高锰酸钾溶液褪色 |
| B.能使品红溶液褪色的不一定是二氧化硫 |
| C.二氧化硫、漂白粉、活性炭、过氧化钠都能使红墨水褪色,其原理相同 |
| D.等物质的量的二氧化硫和氯气相遇在溶液中具有漂白能力 |
| A.“光化学烟雾”主要是由NO2等引起的 |
| B.“酸雨”主要是由空气中CO2浓度增大引起的 |
| C.“白色污染”主要是由聚乙烯塑料等引起的 |
| D.“温室效应”主要是由空气中CO2浓度增大引起的 |
| A.32 g | B.32 g·mol-1 | C.64 g·mol-1 | D.64 g |
| A.它溶于水得到相应的酸 | B.它对应的水化物是可溶性强酸 |
| C.它与强碱反应只生成盐和水 | D.它是非金属氧化物 |
【知识点】 二氧化硅
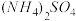 在强热时分解的产物是
在强热时分解的产物是 、
、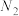 、
、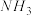 和
和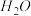 ,则该反应中化合价发生变化和未发生变化的N原子数之比为
,则该反应中化合价发生变化和未发生变化的N原子数之比为| A.1:4 | B.1:2 | C.2:1 | D.4:1 |
【知识点】 氧化还原反应有关计算 氧化还原反应方程式的配平解读
| A.单质、单质 | B.盐、酸 | C.碱、氧化物 | D.氧化物、酸 |
二、未知 添加题型下试题
三、单选题 添加题型下试题
| A.通入二氧化碳气体 | B.加入氢氧化钡溶液 |
| C.加入澄清石灰水 | D.加入稀盐酸 |
【知识点】 碳酸钠与碳酸氢钠的相互转化解读
A.碳酸钙与盐酸反应:CO +2H+=H2O+CO2↑ +2H+=H2O+CO2↑ |
| B.稀H2SO4与铁粉反应:2Fe+6H+=2Fe3++3H2↑ |
C.氢氧化钡溶液与稀H2SO4反应:Ba2++ =BaSO4↓ =BaSO4↓ |
| D.氯化铜溶液与铁粉反应:Cu2++Fe=Fe2++Cu |
【知识点】 离子方程式的正误判断解读
| A.氧化产物为0.1 mol | B.还原产物为0.1 mol |
| C.氧化产物和还原产物共0.2 mol | D.氧化产物为0.2 mol |
【知识点】 氧化还原反应基本概念 氧化还原反应有关计算
| A.24g·mol-1 | B.47.5g·mol-1 | C.80g·mol-1 | D.95g·mol-1 |
【知识点】 物质的量有关计算 根据n=m/M进行相关计算解读
| A.氢氧化铁胶体粒子的直径在1~100 nm之间 |
| B.氢氧化铁胶体具有丁达尔效应 |
| C.氢氧化铁胶体是均一的分散系 |
| D.氢氧化铁胶体的分散质能透过滤纸 |
| A.7.8 g | B.3.9 g | C.3.2 g | D.15.6 g |

| A.化合物与氧化物属于交叉关系 |
| B.单质与非电解质属于包含关系 |
| C.溶液与分散系属于并列关系 |
| D.化合物与电解质属于包含关系 |
| A.1mol N2所含有的原子数为NA |
| B.标准状况下,16g NH3所含有的分子数为NA |
| C.标准状况下,22.4L氯化氢所含的原子数为NA |
| D.500mL 1.0mol/L碳酸钠溶液中所含有的钠离子数为NA |
| A.Fe(NO3)3溶液 | B.MgCl2溶液 |
| C.BaCl2溶液 | D.FeCl3溶液 |
【知识点】 铁盐的检验解读 物质的检验 物质检验和鉴别的基本方法选择及应用解读
| A.Na2SO3是否被氧化(BaCl2) | B.FeCl2是否被氧化(KSCN) |
| C.KI是否被氧化(淀粉溶液) | D.氯水是否失效(pH试纸) |
【知识点】 物质的检验
| A.H2S+2HNO3=S↓+2NO2↑+2H2O |
| B.CuO+2HNO3=Cu(NO3)2+H2O |
| C.3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O |
D.4HNO3 4NO2↑+O2↑+2H2O 4NO2↑+O2↑+2H2O |
| A.晶体硅的结构与金刚石的结构类似 |
| B.晶体硅其熔点高、硬度大、不溶于水 |
| C.硅是灰黑色、具有金属光泽的固体 |
| D.硅广泛存在于自然界中,天然单质硅叫硅石 |
【知识点】 硅单质
| A.S8转化为S6、S4、S2属于物理变化 |
| B.不论哪种硫分子,完全燃烧时都生成二氧化硫 |
| C.S2、S4、S6、S8都是硫元素形成的单质,为同种物质 |
| D.把硫单质在空气中加热到750℃即得S2 |
【知识点】 硫
四、解答题 添加题型下试题
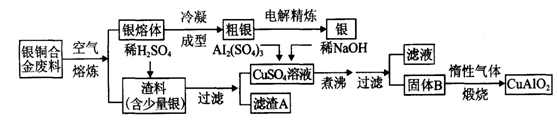
注:Al(OH)3和Cu(OH)2受热易分解成对应的氧化物,且开始分解的温度分别为450 ℃和80 ℃
(1)写出渣料与稀硫酸反应的化学方程式:
(2)固体混合物A的组成为
(3)操作A的名称为
(4)若银铜合金中铜的质量分数为64%,理论上5.0 kg废料中的铜可完全转化为
(5)CuSO4溶液也可用于制备胆矾晶体,其基本操作是
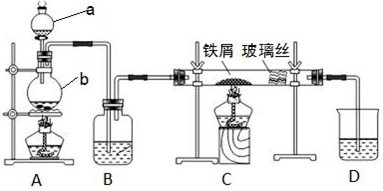
(1)写出仪器的名称:a
(2)A中反应的化学方程式为
(3)装置B中加入的试剂是
(4)已知:向热铁屑中通入氯化氢气体可以生产无水氯化亚铁。为防止有杂质FeCl2生成,可在装置
(5)装置D的作用是
(6)反应结束后,取少量装置C中的固体于试管中,加入足量盐酸,固体完全溶解,得到溶液X。证明溶液X中含有FeCl3的试剂是
(1)某课外活动小组欲探究某过氧化钠样品是否已经变质,取少量样品,溶解,加入
(2)该课外活动小组为了粗略测定过氧化钠的纯度,他们称取a g样品,并设计用下图装置来测定过氧化钠的质量分数。
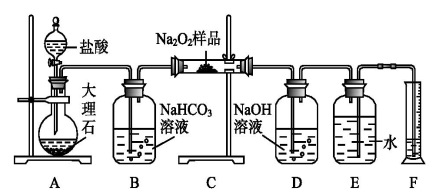
①A中发生反应离子方程式为
②将仪器连接好以后,必须进行的第一步操作是
③B装置出来的气体是否需要干燥
④写出装置C中发生的所有反应的化学方程式
⑤D中NaOH溶液的作用
⑥实验结束时,读取实验中生成气体的体积时,不合理的是
a.直接读取气体体积,不需冷却到室温
b.上下移动量筒,使得E、F中液面高度相同
c.视线与凹液面的最低点相平读取量筒中水的体积
⑦读出量筒内水的体积后,折算成标准状况下氧气的体积为V mL,则样品中过氧化钠的质量分数为
⑧实验完成后E到F之间导管内残留水的体积会使测量结果
假设一:Na2O2+2NO2===2NaNO2+O2↑
假设二:Na2O2+2NO2===2NaNO3
[查阅资料]
2NaNO2+2HCl===2NaCl+NO↑+NO2↑+H2O
2NO2+2NaOH===NaNO2+NaNO3+H2O
[实验探究]
Ⅰ.按图示装置进行实验。

Ⅱ.通入二氧化氮至过氧化钠反应完全,然后对玻璃管中的固体物质进行检验。
[实验结论] 实验表明,过氧化钠与二氧化氮按“假设二”反应。
(1)过氧化钠与二氧化氮的反应中,氧化剂是
(2)装置A中反应的离子方程式是
(3)装置C的作用是
(4)请设计实验证明装置B中的反应不符合“假设一”。
①实验操作:取玻璃管中的固体置于试管中,
②实验现象是
(5)有同学认为:只要直接观察C中导管口是否有气泡冒出,就可以判断B中的反应符合哪一种假设,这种想法
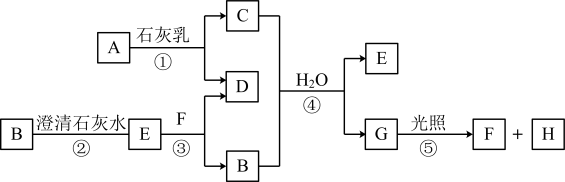
请回答以下问题:
(1)B是
(2)工业上常利用反应①制取漂白粉,该反应的化学方程式:
(3)A中元素的原子结构示意图为
(4)F在溶液中的电离方程式为
(5)上述反应中属于氧化还原反应的是
试卷分析
试卷题型(共 33题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 氯气的物理性质 | |
| 2 | 0.65 | 氧化还原反应的应用 氧化还原反应的规律 | |
| 3 | 0.85 | 仪器使用与实验安全 | |
| 4 | 0.85 | 以N=m·NA/M为中心的有关基本粒子的推算 | |
| 5 | 0.85 | 自然界氮的固定 | |
| 6 | 0.94 | 物质的量的含义 | |
| 7 | 0.65 | 氧化还原反应的应用 | |
| 8 | 0.65 | 漂白粉和漂粉精 二氧化硫的漂白性 过氧化钠的强氧化性 | |
| 9 | 0.65 | 大气污染来源及危害 | |
| 10 | 0.85 | 摩尔质量与相对原子质量区别与联系 阿伏加德罗定律的应用 | |
| 11 | 0.65 | 二氧化硅 | |
| 12 | 0.65 | 氧化还原反应有关计算 氧化还原反应方程式的配平 | |
| 13 | 0.85 | 酸、碱、盐、氧化物的概念及其相互联系 四种基本反应类型 | |
| 15 | 0.65 | 碳酸钠与碳酸氢钠的相互转化 | |
| 16 | 0.65 | 离子方程式的正误判断 | |
| 17 | 0.85 | 氧化还原反应基本概念 氧化还原反应有关计算 | |
| 18 | 0.85 | 物质的量有关计算 根据n=m/M进行相关计算 | |
| 19 | 0.85 | 胶体 分散系概念及其分类 | |
| 20 | 0.65 | 过氧化钠的相关计算 | |
| 21 | 0.85 | 分类方法的应用 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系 分散系概念及其分类 | |
| 22 | 0.85 | 根据n=N/NA进行相关计算 结合气体物质与NA相关推算 根据n=m/M进行相关计算 结合物质结构基础知识与NA相关推算 | |
| 23 | 0.65 | 铁盐的检验 物质的检验 物质检验和鉴别的基本方法选择及应用 | |
| 24 | 0.65 | 物质的检验 | |
| 25 | 0.85 | 氧化还原反应基本概念 氧化还原反应的几组概念 氧化还原反应定义、本质及特征 常见氧化剂与还原剂 | |
| 26 | 0.85 | 焰色试验 | |
| 27 | 0.85 | 硅单质 | |
| 28 | 0.65 | 硫 | |
| 二、未知 | |||
| 14 | 0.65 | 决定物质体积大小的微观因素 | 未知 |
| 三、解答题 | |||
| 29 | 0.65 | 物质分离、提纯综合应用 常见无机物的制备 探究物质组成或测量物质的含量 | 工业流程题 |
| 30 | 0.65 | 氯气 铁盐 物质性质的探究 物质制备的探究 | 实验探究题 |
| 31 | 0.4 | 过氧化钠 物质含量的测定 综合实验设计与评价 | 实验探究题 |
| 32 | 0.65 | 物质性质的探究 综合实验设计与评价 | 实验探究题 |
| 33 | 0.65 | 无机综合推断 氨的还原性 | 无机推断题 |



