云南省普洱市墨江县民族学校2019—2020学年高一上学期期末考试化学试题
云南
高一
期末
2020-02-08
328次
整体难度:
适中
考查范围:
常见无机物及其应用、认识化学科学、化学实验基础、化学与STSE、化学反应原理、有机化学基础
一、单选题 添加题型下试题
| A.稀硫酸 | B.稀盐酸 | C.浓硫酸 | D.氢氧化钠溶液 |
【知识点】 铝
二、未知 添加题型下试题
 、OH-这6种离子中的3种(两种溶液中的离子不重复),已知甲溶液呈蓝色,则乙溶液中大量存在的离子是
、OH-这6种离子中的3种(两种溶液中的离子不重复),已知甲溶液呈蓝色,则乙溶液中大量存在的离子是| A.Cu2+、H+、Cl- | B.K+、H+、Cl- |
C. 、OH-、Cl﹣ 、OH-、Cl﹣ | D.K+、OH-、 |
【知识点】 离子共存 离子反应在化合物组成的分析、鉴定的应用解读
三、单选题 添加题型下试题
| A.3种 | B.4种 | C.5种 | D.6种 |
【知识点】 限定条件下的离子共存解读
| A.它溶于水得到相应的酸 | B.它对应的水化物是可溶性强酸 |
| C.它与强碱反应只生成盐和水 | D.它是非金属氧化物 |
【知识点】 二氧化硅
A.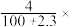 100% 100% | B.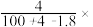 100% 100% |
C. 100% 100% | D. 100% 100% |
【知识点】 化学方程式计算中物质的量的运用解读 钠与水反应原理解读
| A.含氧酸 | B.硅酸盐 | C.铝酸盐 | D.碱类物质 |
【知识点】 硅酸盐组成的表示方法解读
| A.只能有一种分类标准 |
| B.可能有多种分类标准 |
| C.分类标准不同,物质所属类别不同 |
| D.能用交叉分类法进行分类的物质,也可以用树状分类法进行分类 |
①HCl ②H2SO4③HNO3④NaHSO4
| A.①③ | B.①④ | C.① | D.②④ |
【知识点】 电离方程式解读 离子反应的发生及书写 离子方程式的书写解读
| A.标准状况下,22.4 L H2O中含有氢原子数目为2NA |
| B.17 g NH3所含质子数为10NA |
| C.0.1 mol Cu(NO3)2中含有的离子数目为0.2NA |
| D.28 g N2体积为22.4L |
四、未知 添加题型下试题
五、单选题 添加题型下试题
| A.ag | B.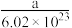 g g | C.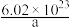 g g | D. g g |
【知识点】 阿伏加德罗常数的含义解读 摩尔质量的概念解读
| A.钠与水反应的离子方程式:Na+H2O=Na++OH-+H2↑ |
B.铁与水蒸气反应的化学方程式:3Fe+4H2O(g) Fe3O4+4H2 Fe3O4+4H2 |
| C.镁、铝与沸水不可能反应 |
| D.钠和硫酸铜溶液反应的离子方程式:2Na+Cu2+=2Na++Cu |
【知识点】 离子方程式的正误判断解读
| A.32 g | B.34 g | C.32 g·mol-1 | D.34 g·mol-1 |
【知识点】 摩尔质量与相对原子质量区别与联系解读
六、多选题 添加题型下试题
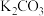 和
和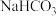 两种白色固体,有四位同学为鉴别它们,分别设计了下列四种不同的方法,其中不可行的是
两种白色固体,有四位同学为鉴别它们,分别设计了下列四种不同的方法,其中不可行的是| A.分别加入过量的盐酸,看有无气泡产生 |
| B.分别取样在试管中加热,将可能产生的气体通入澄清石灰水中,观察有无浑浊出现 |
| C.分别取样配成溶液,滴加Ba(OH)2溶液,观察有无白色沉淀生成 |
| D.分别配成溶液,用铂丝蘸取溶液在酒精灯火焰上灼烧,观察火焰的颜色 |
【知识点】 碳酸钠与碳酸氢钠鉴别的实验解读
七、单选题 添加题型下试题
| A.1 mol氧原子的质量是16 g· mol-1 |
| B.钠离子的摩尔质量是22 g· mol-1 |
| C.二氧化碳的摩尔质量是44 g· mol-1 |
| D.氢的摩尔质量是2 g· mol-1 |
| A.若管道漏气遇氨就会产生白烟 | B.该反应利用了Cl2的强氧化性 |
| C.该反应属于复分解反应 | D.生成1molN2有6mol电子转移 |
【知识点】 四种基本反应类型解读 氧化还原反应的几组概念解读
| A.冷却硝酸钾的饱和溶液 |
| B.常温下使水蒸发 |
| C.先加热蒸发掉一部分水,然后降温 |
| D.升高饱和溶液的温度 |
【知识点】 物质分离、提纯综合应用解读 蒸发与结晶解读
| A.金属钠和氧气反应,条件不同,产物不同 |
| B.实验室中将少量的钠保存在四氯化碳溶剂中 |
| C.钠与酸和水都能发生置换反应,生成盐和氢气 |
| D.钠能从硫酸铜溶液中置换出金属铜 |
【知识点】 钠
| A.2∶1∶2 | B.5∶5∶4 | C.1∶1∶1 | D.无法确定 |
【知识点】 氨的喷泉实验解读 氮氧化物溶解于水的相关计算解读
| A.0.5 mol·L-1 | B.0.6 mol·L-1 | C.1.0 mol·L-1 | D.2 mol·L-1 |
【知识点】 物质的量浓度计算-溶液混合的有关计算解读
| A.2.8 g | B.5.6 g | C.4.2 g | D.11.2 g |
【知识点】 铁与强氧化性酸的反应解读
| A.Na2SiO3→H2SiO3 | B.H2SiO3→SiO2 |
| C.SiO2→H2SiO3 | D.SiO2→Na2SiO3 |
| A.检验自来水中是否含有氯离子 | B.用闻气味的方法鉴别酒精和水 |
| C.检验食盐和纯碱 | D.探究铁在潮湿的空气中是否生锈 |
| A.3.2 g | B.4.0 g | C.4.2 g | D.4.6 g |
【知识点】 镁与混合气体燃烧相关计算解读
| A.常温常压下,8g O2含有4NA个电子 |
| B.1L 0.1mol•L﹣1的氨水中有NA个NH4+ |
| C.标准状况下,22.4L盐酸含有NA个HCl分子 |
| D.1mol Na被完全氧化生成Na2O2,失去2NA个电子 |
| A.a∶b等于A与B的相对分子质量之比 |
| B.a∶b等于等质量的A与B的分子数之比 |
| C.a∶b等于同温同压下A与B的密度之比 |
| D.b∶a等于同温同体积等质量的A与B的压强比 |
【知识点】 阿伏加德罗定律及其推论解读 阿伏加德罗定律的应用解读
八、解答题 添加题型下试题


(1)试剂①应选用
a.盐酸 b.H2SO4溶液
c.氨水 d.NaOH溶液
(2)易拉罐溶解过程中主要反应的化学方程式为
(3)溶液B中溶质的主要成分为
(4)从溶液C中得到明矾的实验操作步骤为蒸发浓缩、
(5)该小组在实验完成之后,得到118.5 g明矾,则明矾的回收率为
①在上述三种方法中,最好的方法是
②上述反应c中NaNO2作
(2)现用金属钠和空气制备纯度较高的Na2O2,可利用的装置如下。回答下列问题(注:Na2O2可以与H2O、CO2反应):
①装置Ⅳ中盛放的药品是
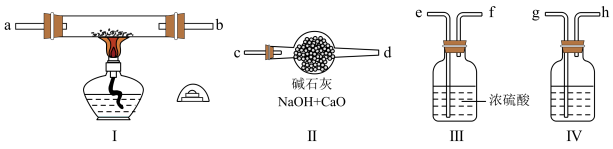
②若规定气体的气流方向从左到右,则组合实验装置时各仪器接口的标号字母(a、b……)顺序:空气进入
③装置Ⅱ的作用
④操作中通空气和加热的顺序为
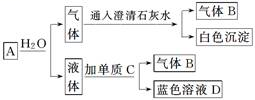
(2)气体B为
(3)单质M与浓硝酸反应的化学方程式是
(4)单质C与稀硝酸反应的化学方程式是
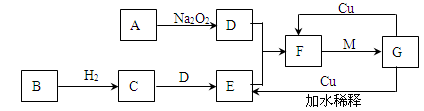
(1)写出C→E的化学方程式:
(2)实验室常用加热两种固体混合物的方法制备物质C,其化学方程式为:
(3)E物质遇到D物质时,会观察到
(4)写出A→D的化学方程式:
九、填空题 添加题型下试题
(1)标准状况下,将500L氨气溶于水形成1L氨水,则此氨水的物质的量浓度为
(2)氨氧化法是工业生产中合成硝酸的主要途径。合成的第一步是将氨和空气的混合气通过灼热的铂铑合金网,在合金网的催化下,氨被氧化成一氧化氮,该反应的化学方程式为
下列反应中的氨与氨氧化法中的氨作用相同的是
A.2Na+2NH3=2NaNH2+H2↑ B.2NH3+3CuO=3Cu+N2+3H2O
C.4NH3+6NO=5N2+6H2O D.HNO3+NH3=NH4NO3
工业中的尾气(假设只有NO和NO2)用烧碱进行吸收,反应的离子方程式为2NO2+2OH-=NO2-+NO3-+H2O和NO+NO2+2OH-=
(3)向27.2gCu和Cu2O的混合物中加入某浓度的稀HNO3500mL,反应过程中产生的气体只有NO。固体完全溶解后,在所得溶液(金属阳离子只有Cu2+)中加入1L1mol·L-1的NaOH溶液使金属离子恰好完全沉淀,此时溶液呈中性,所得沉淀质量为39.2g。
①Cu与稀HNO3反应的离子方程式为
②Cu与Cu2O的物质的量之比为
③HNO3的物质的量浓度为
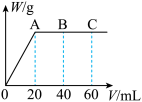
(4)有H2SO4和HNO3的混合溶液20mL,加入0.25mol•L-1Ba(OH)2溶液时,生成沉淀的质量w(g)和Ba(OH)2溶液的体积V(mL)的关系如图所示(C点混合液呈中性)。则原混合液中H2SO4的物质的量浓度为
试卷分析
试卷题型(共 33题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 铝 | |
| 3 | 0.85 | 限定条件下的离子共存 | |
| 4 | 0.65 | 二氧化硅 | |
| 5 | 0.85 | 化学方程式计算中物质的量的运用 钠与水反应原理 | |
| 6 | 0.65 | 硅酸盐组成的表示方法 | |
| 7 | 0.94 | 分类方法的应用 无机物质的分类 | |
| 8 | 0.94 | 电离方程式 离子反应的发生及书写 离子方程式的书写 | |
| 9 | 0.65 | 阿伏加德罗常数的应用 结合气体物质与NA相关推算 结合物质结构基础知识与NA相关推算 | |
| 11 | 0.65 | 阿伏加德罗常数的含义 摩尔质量的概念 | |
| 12 | 0.65 | 离子方程式的正误判断 | |
| 13 | 0.65 | 无机物的检验 | |
| 14 | 0.94 | 常见合金的组成 金属材料的应用 | |
| 15 | 0.85 | 摩尔质量与相对原子质量区别与联系 | |
| 17 | 0.85 | 摩尔质量的概念 | |
| 18 | 0.65 | 四种基本反应类型 氧化还原反应的几组概念 | |
| 19 | 0.65 | 物质分离、提纯综合应用 蒸发与结晶 | |
| 20 | 0.85 | 钠 | |
| 21 | 0.65 | 氨的喷泉实验 氮氧化物溶解于水的相关计算 | |
| 22 | 0.85 | 物质的量浓度计算-溶液混合的有关计算 | |
| 23 | 0.65 | 铁与强氧化性酸的反应 | |
| 24 | 0.85 | 物质的转化 二氧化硅的化学性质 硅酸的化学性质 | |
| 25 | 0.85 | 氯离子的检验 金属的电化学腐蚀与防护 乙醇的物理性质 乙酸具有酸的通性 | |
| 26 | 0.65 | 镁与混合气体燃烧相关计算 | |
| 27 | 0.85 | 阿伏加德罗常数的求算 结合物质结构基础知识与NA相关推算 | |
| 28 | 0.65 | 阿伏加德罗定律及其推论 阿伏加德罗定律的应用 | |
| 二、未知 | |||
| 2 | 0.85 | 离子共存 离子反应在化合物组成的分析、鉴定的应用 | 未知 |
| 10 | 0.85 | 分散系概念 胶体 分散系概念及其分类 | 未知 |
| 三、多选题 | |||
| 16 | 0.65 | 碳酸钠与碳酸氢钠鉴别的实验 | |
| 四、解答题 | |||
| 29 | 0.65 | 含氧化铝的混合物的提纯 物质分离、提纯的常见化学方法 物质分离、提纯综合应用 | 工业流程题 |
| 30 | 0.65 | 钠 过氧化钠 化学实验探究 物质制备的探究 | 实验探究题 |
| 31 | 0.65 | 二氧化氮与水反应 硝酸的强氧化性 | 无机推断题 |
| 32 | 0.65 | 无机综合推断 氨气 氨气的实验室制法 | 无机推断题 |
| 五、填空题 | |||
| 33 | 0.65 | 物质的量浓度的计算 氧化还原反应有关计算 氧化还原反应方程式的配平 氨的还原性 | |



