云南省富宁县一中2019-2020学年高二上学期开学考试化学试题
云南
高二
开学考试
2019-09-18
250次
整体难度:
适中
考查范围:
常见无机物及其应用、化学实验基础、物质结构与性质、认识化学科学、化学反应原理、有机化学基础
一、单选题 添加题型下试题
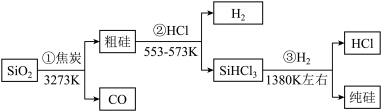
| A.①②③均属于氧化还原反应 | B.氢气和氯化氢均可循环利用 |
| C.二氧化硅是一种坚硬难熔的固体 | D.三氯甲硅烷(SiHCl3)摩尔质量为135.5 g |
 )具有相同数目的电子的分子是( )
)具有相同数目的电子的分子是( )| A.CH4 | B.OH- | C.NO | D.H3O+ |
【知识点】 原子中相关数值及其之间的相互关系解读
| A.2Na+2H2O=2NaOH+H2↑ | B.2F2+2H2O=4HF+O2↑ |
| C.CaO+H2O=Ca(OH) 2 | D.3NO2+H2O=2HNO3+NO |
| A.所有卤族元素的微粒都易得电子 |
| B.和氟同一主族的元素都是非金属元素 |
| C.化合物中卤族元素都显负价 |
| D.卤族元素原子的原子半径从上到下逐渐减小 |
 O2+H2O+2e-=2OH-,可以判断石墨电极是
O2+H2O+2e-=2OH-,可以判断石墨电极是| A.负极,发生还原反应 | B.正极,发生氧化反应 |
| C.负极,发生氧化反应 | D.正极,发生还原反应 |
二、未知 添加题型下试题
三、单选题 添加题型下试题
| A.Na2SO3与BaCl2溶液作用,有白色沉淀生成,加稀HNO3后沉淀消失 |
| B.将SO2气体分别通入Ba(OH)2溶液、FeCl3与BaCl2的混合溶液、HNO3酸化的BaCl2溶液中,均可有白色沉淀生成 |
| C.将SO2气体通入BaCl2溶液中没有白色沉淀生成,将SO2气体通入Ba(NO3)2溶液中有白色沉淀生成 |
| D.将SO2气体、Cl2一起通入BaCl2溶液中,或将SO2气体、NO2气体一起通入BaCl2溶液中,均有白色沉淀生成 |
| A.氟 | B.氯 | C.溴 | D.碘 |
【知识点】 同主族元素性质递变规律

| A.电极A为电池负极 |
| B.电极B表面上发生还原反应 |
| C.工作一段时间溶液pH保持不变 |
| D.燃料电池工作时不会出现火焰 |
| A.少量的浓硫酸沾到皮肤上时,可以直接用大量的水冲洗 |
| B.凡是给玻璃仪器加热时,都要加垫石棉网,以防仪器炸裂 |
| C.取用化学药品时,应特别注意观察药品包装容器的安全警示标记 |
| D.闻任何化学药品的气味都不能使鼻子凑近药品 |
| A.豆腐 | B.馒头 | C.西红柿 | D.豆油 |
【知识点】 蛋白质的来源及作用
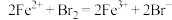 ②
② ③
③ 由此判断下列说法正确的是( )
由此判断下列说法正确的是( )| A.铁元素在反应①中被还原,在③中被氧化 |
| B.反应②中当有1molCl2被氧化时,有2molBr—被还原 |
C.氧化性强弱顺序为: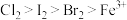 |
D.还原性强弱顺序为: |
【知识点】 氧化性、还原性强弱的比较解读 氧化还原反应的规律解读
| A.SO2、H2SO4、H2SO3、H2S、S | B.SO2、H2SO3、H2SO4、SO2、SO3 |
| C.SO2、H2SO4、H2SO3、SO2、S | D.SO2、H2SO3、H2SO4、H2S、S |
【知识点】 二氧化硫 含硫化合物之间的转化解读 硫单质的化学性质
| A.400 mL | B.450 mL | C.500 mL | D.550 mL |
| A.次氯酸钙不稳定,易分解 |
| B.次氯酸钙易吸收水分而潮解 |
| C.次氯酸钙与空气中的水和二氧化碳反应 |
| D.次氯酸钙与空气中的二氧化碳反应 |
【知识点】 漂白粉的变质原因及检验解读
| A.23g Na 与足量H2O反应完全后可生成nA个H2分子 |
| B.1 molCu和足量热浓硫酸反应可生成nA个SO3分子 |
| C.标准状况下,22.4L N2和H2混合气中含nA个原子 |
| D.3mol单质Fe完全转变为Fe3O4,失去8nA个电子 |
【知识点】 阿伏加德罗常数的求算解读 物质的量有关计算
| A.该元素与卤素化合时一定形成离子键 |
| B.该元素与卤素化合时一定不能形成离子键 |
| C.该元素与氯元素形成的化合物一定是离子化合物 |
| D.该元素与氯元素形成的化合物的水溶液能导电 |
【知识点】 元素周期律、元素周期表的推断
| A.含4 g NaOH的溶液1 L |
| B.含0.1 g NaOH的溶液1 L |
| C.含0.2 mol H2SO4的溶液0.5 L |
| D.将98 g的H2SO4倒入1 L水中 |
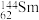 与
与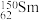 的说法正确的是( )
的说法正确的是( )A.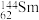 与 与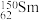 互为同位素 互为同位素 | B.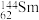 与 与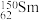 的质量数相同 的质量数相同 |
C.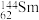 与 与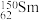 是同一种核素 是同一种核素 | D.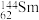 与 与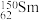 核外电子数和中子数都为62 核外电子数和中子数都为62 |
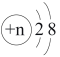 ,若该粒子为离子,则它所带的电荷数可能为。
,若该粒子为离子,则它所带的电荷数可能为。①8-n ②n-8 ③10-n ④n-10
| A.①② | B.①③ | C.③④ | D.②④ |
【知识点】 原子核外电子的排布
| A.在25 ℃、1.01×105Pa的条件下,2.24 L H2中含有的分子数小于0.1NA |
| B.1 L 1 mol·L-1的CaCl2溶液中含Cl-的数目为NA |
| C.在标准状况下,22.4 L H2O的质量约为18 g |
| D.22 g CO2与标准状况下11.2 L H2O含有相同的分子数 |
| A.原子半径:甲>丙 |
| B.单质的还原性:丁>丙 |
| C.乙的氢化物是同族中氢化物还原性最强的 |
| D.乙、丙、丁的最高价氧化物对应的水化物能相互反应 |
| A.苯 | B.乙烷 | C.乙烯 | D.氯化铁 |
【知识点】 苯 乙烯的加成反应解读 乙烯与强氧化性物质的反应解读
四、解答题 添加题型下试题
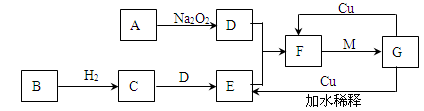
(1)写出C→E的化学方程式:
(2)实验室常用加热两种固体混合物的方法制备物质C,其化学方程式为:
(3)E物质遇到D物质时,会观察到
(4)写出A→D的化学方程式:
五、填空题 添加题型下试题
(1)下列制备氯乙烷的反应中原子经济性最高的是
A.CH2=CH2+HCl→CH3CH2Cl
B.CH3CH2OH+HCl
 CH3CH2Cl+H2O
CH3CH2Cl+H2OC.CH3CH3+Cl2
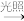 CH3CH2Cl+HCl
CH3CH2Cl+HClD.CH2=CHCl+H2
 CH3CH2Cl
CH3CH2Cl由上述四个反应可归纳出,原子经济性最高的是
(2)有毒物质的无害化处理也是绿色化学研究的内容之一。ClO2是一种性能优良的消毒剂,它可将废水中少量的CN-等有毒的酸根离子氧化而除去。请写出用ClO2将废水中的CN-氧化成无毒气体的离子方程式:
(3)某饮用水厂由天然水制备纯净水(去离子水)的工艺流程示意图如图:
活性炭的作用是
六、解答题 添加题型下试题
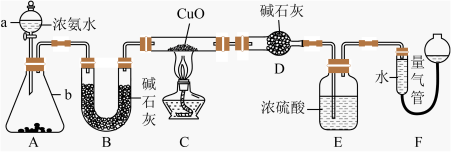
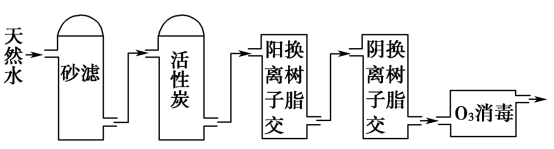
(1)仪器a的名称为
(2)实验室中,利用装置A,还可制取的无色气体是
A.Cl2 B.O2 C.CO2 D.NO2
(3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管有无色无味的气体,上述现象证明NH3具有
(4)E装置中浓硫酸的作用
(5)读取气体体积前,应对装置F进行的操作:
(6)实验完毕,若测得干燥管D增重mg,装置F测得气体的体积为nL(已折算成标准状况),则氨分子中氮、氢的原子个数比为
 的分子组成,测定装置图所示(夹持仪器、酒精灯等已略去)。
的分子组成,测定装置图所示(夹持仪器、酒精灯等已略去)。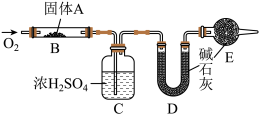
取
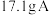 放入装置中,通入过量
放入装置中,通入过量 燃烧,生成
燃烧,生成 和
和 ,请回答下列有关问题:
,请回答下列有关问题:(1)通入过量
 的目的是
的目的是(2)
 装置的作用是
装置的作用是 装置的作用是
装置的作用是(3)通过该实验能否确定
 中是否含有氧原子
中是否含有氧原子(4)若
 的摩尔质量为
的摩尔质量为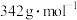 ,
, 装置增重
装置增重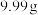 ,
, 装置增重
装置增重 ,则
,则 的分子式为
的分子式为(5)写出
 燃烧的化学方程式:
燃烧的化学方程式:(6)
 可发生水解反应,
可发生水解反应,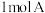 可水解生成2种互为同分异构体的产物,且这两种产物均为
可水解生成2种互为同分异构体的产物,且这两种产物均为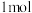 ,则
,则 在催化剂作用下水解的化学方程式为
在催化剂作用下水解的化学方程式为【知识点】 有机物实验式的确定解读 探究物质组成或测量物质的含量解读
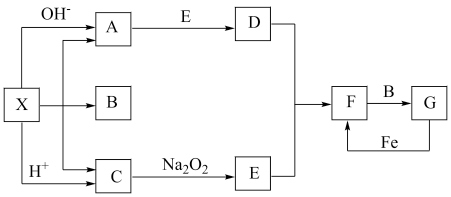
(1)写出化学式:X
(2)实验室收集气体D和F的方法依次是
(3)写出C→E的化学方程式:
(4)请写出A与E反应生成D的化学方程式:
(5)检验物质A的方法和现象是
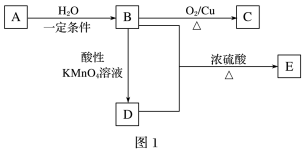

(1)由B生成C的反应类型是
(2)A的结构简式为
(3)B与D反应生成E的化学方程式为
(4)请写出B的一种用途:
试卷分析
试卷题型(共 32题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 硅的制备 二氧化硅的物理性质 常见无机物的制备 | |
| 2 | 0.85 | 原子中相关数值及其之间的相互关系 | |
| 3 | 0.94 | 氧化还原反应基本概念 氧化还原反应定义、本质及特征 四种基本反应类型与氧化还原反应的关系 | |
| 4 | 0.94 | 同主族元素性质递变规律 元素周期律的应用 同主族元素性质递变规律理解及应用 | |
| 5 | 0.85 | 原电池正负极判断 | |
| 7 | 0.4 | 二氧化氮 二氧化硫的化学性质 | |
| 8 | 0.94 | 同主族元素性质递变规律 | |
| 9 | 0.85 | 原电池 烃燃料电池 | |
| 10 | 0.65 | 仪器使用与实验安全 化学实验基础操作 实验安全 | |
| 11 | 0.94 | 蛋白质的来源及作用 | |
| 12 | 0.65 | 氧化性、还原性强弱的比较 氧化还原反应的规律 | |
| 13 | 0.94 | 分散系概念及其分类 | |
| 14 | 0.4 | 酯化反应 醛类的银镜反应 有机物的推断 多官能团有机物的结构与性质 | |
| 15 | 0.85 | 二氧化硫 含硫化合物之间的转化 硫单质的化学性质 | |
| 16 | 0.65 | 物质的量有关计算 基于氧化还原反应守恒规律的计算 硝酸的强氧化性 铁及铁的氧化物混合物反应的相关计算 | |
| 17 | 0.85 | 漂白粉的变质原因及检验 | |
| 18 | 0.65 | 阿伏加德罗常数的求算 物质的量有关计算 | |
| 19 | 0.85 | 元素周期律、元素周期表的推断 | |
| 20 | 0.85 | 物质的量浓度 物质的量浓度的计算 | |
| 21 | 0.94 | 原子的构成 原子的基本构成 原子中相关数值及其之间的相互关系 元素、核素、同位素 | |
| 22 | 0.85 | 原子核外电子的排布 | |
| 23 | 0.65 | 阿伏加德罗常数的求算 阿伏加德罗定律及其推论 物质的量有关计算 | |
| 24 | 0.65 | 元素金属性与非金属性递变规律的理解及应用 微粒半径大小的比较方法 根据原子结构进行元素种类推断 | |
| 25 | 0.85 | 乙烯的加成反应 苯的加成反应 | |
| 26 | 0.65 | 苯 乙烯的加成反应 乙烯与强氧化性物质的反应 | |
| 二、未知 | |||
| 6 | 0.85 | 原电池原理理解 原电池电子流向判断及应用 燃料电池 | 未知 |
| 三、解答题 | |||
| 27 | 0.65 | 无机综合推断 氨气 氨气的实验室制法 | 无机推断题 |
| 29 | 0.65 | 氨的还原性 氨气的实验室制法 物质性质的探究 | 实验探究题 |
| 30 | 0.65 | 有机物实验式的确定 探究物质组成或测量物质的含量 | 实验探究题 |
| 31 | 0.4 | 无机综合推断 氨的还原性 硝酸的强氧化性 过氧化钠和二氧化碳反应 | 无机推断题 |
| 32 | 0.65 | 乙烯的加成反应 乙醇催化氧化 乙酸的酯化反应 | 有机推断题 |
| 四、填空题 | |||
| 28 | 0.65 | 离子方程式的书写 氧化还原反应方程式的配平 加成反应 | |