云南省玉溪市通海县第二中学2019-2020学年高一上学期12月月考化学试题
云南
高一
阶段练习
2019-12-11
263次
整体难度:
适中
考查范围:
常见无机物及其应用、认识化学科学、有机化学基础、化学实验基础、化学与STSE
一、单选题 添加题型下试题
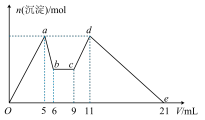
| A.X是盐酸,Y是NaOH溶液,且c(Y)=2c(X) |
| B.原混合液中,c(Al3+)∶c(Mg2+)∶c(Cl-)=1∶1∶5 |
| C.X是NaOH溶液,Y是盐酸,且c(NaOH)∶c(HCl)=2∶1 |
| D.从b至c相应的离子方程式为H++OH-===H2O |
| A.稀H2SO4 | B.盐酸 | C.CO2 | D.氨水 |
【知识点】 偏铝酸钠与二氧化碳的反应解读 铝三角转化解读
| A.钠与水反应的离子方程式:Na+H2O===Na++OH-+H2↑ |
| B.铁与水蒸气反应的化学方程式:2Fe+3H2O(g)===Fe2O3+3H2 |
| C.钠跟氯化钾溶液反应的离子方程式:2Na+2H2O===2Na++2OH-+H2↑ |
| D.钠和硫酸铜溶液反应的离子方程式:2Na+Cu2+===2Na++Cu |
【知识点】 离子反应的发生及书写 离子方程式的书写解读 离子方程式的正误判断解读
| A.产生白色沉淀 |
| B.开始生成白色沉淀,后逐渐减少 |
| C.没有明显变化 |
| D.开始生成白色沉淀,后逐渐减少,最后得到无色溶液 |
A.KClO3是氧化剂 | B.H2O既不是氧化产物也不是还原产物 |
| C.HCl是还原剂 | D.KCl既是还原产物也是氧化产物 |
【知识点】 氧化还原反应基本概念 氧化还原反应的规律解读
| A.2∶1 | B.1∶2 | C.1∶7 | D.7∶1 |
| A.SO2、SiO2、CO均为酸性氧化物 |
| B.稀豆浆、硅酸、氯化铁溶液均为胶体 |
| C.硫酸、盐酸、氢氟酸均为强酸 |
| D.氯水、水玻璃、氨水均为混合物 |
| A.转移电子的数目为0.2NA |
| B.所得溶液中溶质的质量分数为2.3% |
| C.产生气体的体积为1.12 L |
| D.产生的气体含有0.1 mol电子 |
| A.0.01 mol | B.0.02 mol | C.0.03 mol | D.0.04 mol |
| A.大于6.0 mL | B.等于6.0 mL |
| C.小于6.0 mL | D.无法判断 |
【知识点】 配制一定物质的量浓度的溶液实验的误差分析解读
| A.蒸馏 | B.分液 | C.过滤 | D.蒸发 |
【知识点】 有机物分离提纯的几种常见操作 蒸馏与分馏解读
| A.金属铜 | B.碳酸钠晶体 | C.硝酸钠溶液 | D.熔融氯化钠 |
| A.硝酸 | B.过氧化氢 | C.氯酸钾 | D.过氧化钠 |
| A.④⑤ | B.②③ | C.①② | D.①③ |
【知识点】 钠的化学性质
| A.所有蒸馏操作中都必须用到温度计 |
| B.蒸馏自来水可以制得蒸馏水 |
| C.蒸馏烧瓶使用前一般不需要检漏 |
| D.进行蒸馏操作时,应向蒸馏烧瓶中加入几块碎瓷片,防止暴沸 |
A.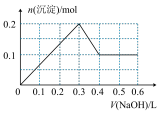 |
B. |
C.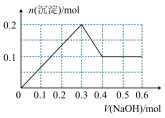 |
D. |
| A.一定质量溶液里所含溶质的质量 | B.溶液中溶质质量与溶液质量之比 |
| C.1L溶液里所含溶质的质量 | D.100g溶剂里所含溶质的质量 |
| A.氨溶于水可导电,所以氨是电解质 |
| B.氧化钠熔融时能导电,所以氧化钠是电解质 |
| C.液态的铜导电性很好,所以铜是电解质 |
| D.二氧化硫水溶液的导电性很好,所以二氧化硫是电解质 |
【知识点】 电解质、非电解质概念解读 非电解质、电解质物质类别判断解读
二、未知 添加题型下试题
| A.BaCl2 Na2CO3 AgNO3 盐酸 |
| B.BaCl2 Na2CO3 盐酸 AgNO3 |
| C.Na2CO3 盐酸 AgNO3 BaCl2 |
| D.AgNO3 盐酸 BaCl2 Na2CO3 |
【知识点】 物质共存解读 离子反应在化合物组成的分析、鉴定的应用解读
三、单选题 添加题型下试题
| A.胶体是纯净物 |
| B.胶体与溶液的本质区别是有丁达尔效应 |
| C.将饱和氯化铁溶液滴入稀氢氧化钠溶液中加热,可得氢氧化铁胶体 |
| D.胶体属于介稳体系 |
| A.粗盐溶解时用玻璃棒搅拌,加快粗盐的溶解 |
| B.将溶液转移至过滤器时,使用玻璃棒引流 |
| C.蒸发滤液时用玻璃棒搅拌,使滤液受热均匀 |
| D.蒸发滤液时用玻璃棒搅拌,加快晶体的析出 |
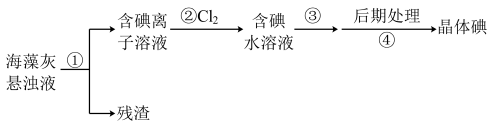
下列判断正确的是( )
| A.步骤①③的操作分别是过滤、萃取 |
| B.可用淀粉溶液检验步骤②的反应是否进行完全 |
| C.步骤③中加入的有机溶剂是四氯化碳或乙醇 |
| D.步骤④的操作是过滤 |
四、填空题 添加题型下试题
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2+H2O
C.2H2O2=2H2O+O2
D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(1)H2O2仅体现氧化性的反应是(填代号)
(2)H2O2既体现氧化性又体现还原性的反应是(填代号)
(3)在稀硫酸中,KMnO4和H2O2能发生氧化还原反应。
氧化反应:H2O2-2e-===2H++O2↑
还原反应:MnO
 +5e-+8H+===Mn2++4H2O
+5e-+8H+===Mn2++4H2O写出该氧化还原反应的化学方程式:
(4)请配平以下化学方程式:
 Al+
Al+ NaNO3+
NaNO3+ NaOH===
NaOH=== NaAlO2+
NaAlO2+ N2↑+
N2↑+ H2O
H2O五、解答题 添加题型下试题
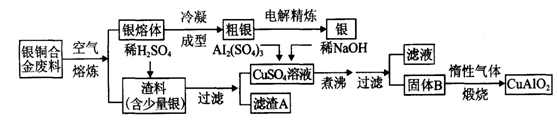
注:Al(OH)3和Cu(OH)2受热易分解成对应的氧化物,且开始分解的温度分别为450 ℃和80 ℃
(1)写出渣料与稀硫酸反应的化学方程式:
(2)固体混合物A的组成为
(3)操作A的名称为
(4)若银铜合金中铜的质量分数为64%,理论上5.0 kg废料中的铜可完全转化为
(5)CuSO4溶液也可用于制备胆矾晶体,其基本操作是








 ―→
―→
某化学兴趣小组将上述流程②、③设计成如下图所示操作。
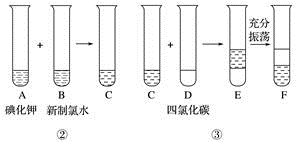
已知过程②发生反应的化学方程式为Cl2+2KI===2KCl+I2
回答下列问题:
(1)写出提取过程①、③中实验操作的名称:①
(2)在灼烧过程中,使用到的实验仪器有酒精灯、
(3)F中下层液体的颜色为
(4)从F中得到固态碘还需进行的操作是
【知识点】 海带中碘的提取及检验解读
六、填空题 添加题型下试题
(1)Fe2O3固体(红棕色)属于
(2)用上述所得溶液进行下列实验,取少量溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀产生,反应的离子方程式
(3)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向烧杯中加入几滴FeCl3溶液,继续煮沸至出现
(4)另取一小烧杯也加入20mL蒸馏水,向烧杯中加入1mL FeCl3溶液,振荡摇匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到
七、解答题 添加题型下试题
(1)某课外活动小组欲探究某过氧化钠样品是否已经变质,取少量样品,溶解,加入
(2)该课外活动小组为了粗略测定过氧化钠的纯度,他们称取a g样品,并设计用下图装置来测定过氧化钠的质量分数。
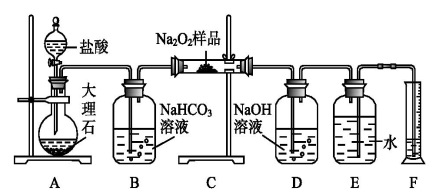
①A中发生反应离子方程式为
②将仪器连接好以后,必须进行的第一步操作是
③B装置出来的气体是否需要干燥
④写出装置C中发生的所有反应的化学方程式
⑤D中NaOH溶液的作用
⑥实验结束时,读取实验中生成气体的体积时,不合理的是
a.直接读取气体体积,不需冷却到室温
b.上下移动量筒,使得E、F中液面高度相同
c.视线与凹液面的最低点相平读取量筒中水的体积
⑦读出量筒内水的体积后,折算成标准状况下氧气的体积为V mL,则样品中过氧化钠的质量分数为
⑧实验完成后E到F之间导管内残留水的体积会使测量结果
①在上述三种方法中,最好的方法是
②上述反应c中NaNO2作
(2)现用金属钠和空气制备纯度较高的Na2O2,可利用的装置如下。回答下列问题(注:Na2O2可以与H2O、CO2反应):
①装置Ⅳ中盛放的药品是
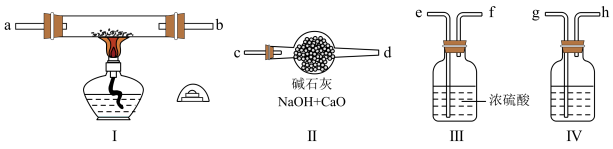
②若规定气体的气流方向从左到右,则组合实验装置时各仪器接口的标号字母(a、b……)顺序:空气进入
③装置Ⅱ的作用
④操作中通空气和加热的顺序为
试卷分析
试卷题型(共 32题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 氢氧化铝与强碱反应 铝盐与强碱溶液反应 偏铝酸钠与盐酸的反应 | |
| 2 | 0.94 | 交叉分类法 分类方法的应用 | |
| 3 | 0.65 | 偏铝酸钠与二氧化碳的反应 铝三角转化 | |
| 4 | 0.4 | 离子反应的发生及书写 离子方程式的书写 离子方程式的正误判断 | |
| 5 | 0.85 | 氢氧化铝与强碱反应 铝盐与强碱溶液反应 | |
| 6 | 0.85 | 氧化还原反应基本概念 氧化还原反应的规律 | |
| 7 | 0.65 | 烃燃烧相关计算 烃燃烧产物的量和烃的组成关系 烃燃烧前后反应物与生成物的分子数关系的有关计算 | |
| 8 | 0.85 | 分类方法的应用 酸、碱、盐、氧化物的概念及其相互联系 | |
| 9 | 0.65 | 物质的量有关计算 钠与水反应原理 | |
| 10 | 0.65 | 化学方程式计算中物质的量的运用 钠与水反应原理 铝与强碱溶液反应 | |
| 11 | 0.85 | 配制一定物质的量浓度的溶液实验的误差分析 | |
| 12 | 0.85 | 有机物分离提纯的几种常见操作 蒸馏与分馏 | |
| 13 | 0.65 | 电解质、非电解质概念 非电解质、电解质物质类别判断 物质水溶液的导电性 | |
| 14 | 0.85 | 过氧化钠 过氧化钠的物理性质、组成、结构及用途 过氧化钠和二氧化碳反应 | |
| 15 | 0.94 | 钠的化学性质 | |
| 16 | 0.85 | 仪器使用与实验安全 常用仪器及使用 化学实验基础操作 实验安全 | |
| 17 | 0.65 | 铝盐与强碱溶液反应 | |
| 18 | 0.85 | 溶液的含义和组成 | |
| 19 | 0.94 | 电解质、非电解质概念 非电解质、电解质物质类别判断 | |
| 20 | 0.94 | 分散系概念及其分类 | |
| 22 | 0.94 | 胶体 胶体的定义及分类 胶体的性质和应用 胶体的制备 | |
| 23 | 0.65 | 萃取和分液 | |
| 24 | 0.65 | 酸、碱、盐、氧化物 | |
| 25 | 0.85 | 化学实验基础操作 蒸发与结晶 | |
| 26 | 0.85 | 物质分离、提纯综合应用 物质的检验 海水资源综合利用 海带中碘的提取及检验 | |
| 二、未知 | |||
| 21 | 0.65 | 物质共存 离子反应在化合物组成的分析、鉴定的应用 | 未知 |
| 三、填空题 | |||
| 27 | 0.65 | 氧化还原反应的几组概念 氧化还原反应的应用 氧化还原反应方程式的配平 氧化还原反应的规律 | |
| 30 | 0.65 | 胶体的性质和应用 胶体的制备 几种铁的氧化物的化学性质 | |
| 四、解答题 | |||
| 28 | 0.65 | 物质分离、提纯综合应用 常见无机物的制备 探究物质组成或测量物质的含量 | 工业流程题 |
| 29 | 0.85 | 海带中碘的提取及检验 | 实验探究题 |
| 31 | 0.4 | 过氧化钠 物质含量的测定 综合实验设计与评价 | 实验探究题 |
| 32 | 0.65 | 钠 过氧化钠 化学实验探究 物质制备的探究 | 实验探究题 |




