云南省通海县三中2019-2020学年高二9月份(开学考试)化学试题
云南
高二
开学考试
2019-09-18
216次
整体难度:
适中
考查范围:
常见无机物及其应用、认识化学科学、化学反应原理、化学与STSE、物质结构与性质、有机化学基础、化学实验基础
一、单选题 添加题型下试题
| A.两者都污染环境,危害健康 |
| B.两者都是形成酸雨的主要物质 |
| C.两者都能使品红溶液褪色 |
| D.两者都易溶于水 |
【知识点】 二氧化硫与二氧化碳的性质区别解读
| A.探究SO2和Na2O2反应可能有Na2SO4生成 |
| B.探究NO和N2O可能化合生成NO2 |
| C.探究NO2可能被NaOH溶液完全吸收生成NaNO2和NaNO3 |
| D.探究向滴有酚酞试液的NaOH溶液中通入Cl2,酚酞红色褪去的原因是溶液的酸碱性改变还是HClO的漂白作用 |
【知识点】 氧化还原反应基本概念 氧化还原反应的应用
| A.除去水中氯离子 | B.除去水中钙离子 |
| C.除去水中悬浮物 | D.消毒杀菌 |
【知识点】 明矾 明矾的净水作用及原理解读
| A.构成原电池的正极和负极材料必须是两种活泼性不同的金属 |
| B.原电池是将化学能转变为电能的装置 |
| C.在原电池中,电子流出的一极是负极,该电极被还原 |
| D.原电池放电时,电流的方向是从负极到正极 |
【知识点】 原电池
| A.64 g SO2含有氧原子数为1NA |
| B.物质的量浓度为0.5 mol·L-1的MgCl2溶液,含有Cl-数为1NA |
| C.标准状况下,22.4 L H2O的分子数为1NA |
| D.常温常压下,14 g N2含有分子数为0.5NA |
| A.铁锅价格便宜 | B.铸铁锅的铁熔点高 |
| C.使用铁锅烹饪的食物中留有铁元素 | D.铁锅含有有机物必含的碳元素 |
| A.同温、同压下,相同质量的气体都占有相同的体积 |
| B.同温、同压下,相同体积的气体都含有相同数目的分子 |
| C.1 mol O2中含有1.204×1024个氧原子,在标准状况下占有体积22.4 L |
| D.由0.2 g H2和8.8 g CO2、5.6 g CO组成混合气体,其密度是相同状况下O2密度的0.913倍 |

| A.烧瓶B中制备氯气的反应物为MnO2和稀盐酸 |
| B.装置C、D中分别盛有浓硫酸、饱和食盐水 |
| C.装置E和装置F之间需要增加一个干燥装置,才能制得无水氯化铁 |
| D.装置F的目的是检验有无氯气逸出 |
二、未知 添加题型下试题
①将硫酸钡放入水中不能导电,所以硫酸钡是非电解质
②氨溶于水得到的溶液氨水能导电,所以氨水是电解质
③固态HCl不导电,熔融态的HCl可以导电
④NaHSO4电离时生成的阳离子有氢离子,所以是酸
⑤电解质溶于水中一定能导电,非电解质溶于水中一定不导电
| A.①④ | B.①④⑤ | C.①②③④ | D.①②③④⑤ |
三、单选题 添加题型下试题
 、Cl-四种离子其物质的量浓度之比为c(Na+):c(Mg2+):c(Cl-)=3:5:5,若Na+浓度为3mol·L-1。则SO
、Cl-四种离子其物质的量浓度之比为c(Na+):c(Mg2+):c(Cl-)=3:5:5,若Na+浓度为3mol·L-1。则SO 的浓度为
的浓度为| A.2mol·L-1 | B.3mol·L-1 | C.4mol·L-1 | D.8mol·L-1 |
【知识点】 物质的量浓度概念、含义解读
| A.22.4 L | B.44.8 L | C.11.2 L | D.4.48 L |
【知识点】 阿伏加德罗定律 阿伏加德罗定律及其推论解读
| A.正极的电极反应为Ag2O+2e-+H2O===2Ag+2OH- |
| B.Zn极发生氧化反应,Ag2O极发生还原反应 |
| C.使用时电子由Zn极经外电路流向Ag2O极,Zn是负极 |
| D.使用时溶液中电流的方向是由Ag2O极流向Zn极 |
| A.32g | B.32g·mol-1 | C.64mol | D.64g·mol-1 |
【知识点】 物质的量有关计算 根据n=m/M进行相关计算解读
| A.碘升华 | B.酒精溶于水 | C.冰融化成水 | D.HCl气体溶于水 |
【知识点】 化学键与分子间作用力解读
| A.随着原子序数的增加,元素的非金属性逐渐增强 |
| B.随着原子序数的减小,单质的氧化性逐渐增强 |
| C.通常呈黄绿色的也是氧化性最强的 |
| D.易升华的也是相对分子质量最大的 |
| A.乙烯、氯乙烯、聚乙烯均可使酸性高锰酸钾溶液褪色 |
| B.乙酸与乙醇可以发生酯化反应,又均可与金属钠发生置换反应 |
| C.葡萄糖、纤维素和蛋白质在一定条件下都能发生水解反应 |
| D.石油经过分馏得到多种烃,煤经过分馏可制得焦炭、煤焦油等产品 |
| A.卤素原子序数越大,其氢化物越稳定 |
| B.卤素原子序数越大,其氢化物越不稳定 |
| C.卤化氢稳定性的顺序为HF>HCl>HBr>HI |
| D.卤素单质与氢气越难反应,生成的氢化物越不稳定 |
| A.属于盐 | B.难溶于水 | C.属于硅酸盐 | D.易溶于水 |
| A.它位于周期表的第四周期第IA族 |
| B.氢氧化铷是弱碱 |
| C.在钠、钾、铷三种单质中,铷的熔点最高 |
| D.硝酸铷是离子化合物 |
【知识点】 同主族元素性质递变规律
| A.石油是混合物,汽油是纯净物 | B.石油中只含有液态烷烃 |
| C.石油含有碳、氢、硫、氧、氮等元素 | D.石油具有固定的沸点 |
【知识点】 石油物理性质及组成成分解读 石油分馏解读
| A.1∶5 | B.5∶1 | C.1∶3 | D.3∶1 |
【知识点】 蔗糖与麦芽糖 葡萄糖、果糖的组成与结构 蔗糖与麦芽糖的水解 淀粉、纤维素的水解
| A.含有共价键的化合物一定是共价物 |
| B.气态单质分子中一定存在共价键 |
| C.共价化合物中一定存在共价键 |
| D.离子化合物中只含有离子键 |
【知识点】 化学键基本概念 化学键概念理解及判断解读

| A.若②中为浓盐酸,产生大量气体:说明硫酸的酸性比盐酸强 |
| B.若②中为铜片,有气泡产生,底部生成灰白色固体:说明浓硫酸有强氧化性 |
| C.若②中为蓝色硫酸铜晶体,蓝色晶体变为白色:说明浓硫酸有吸水性,发生物理变化 |
| D.若②为蔗糖,白色固体变为黑色海绵状,有气体放出:说明浓硫酸有脱水性、强氧化性 |
| A.电解熔融NaCl制取金属钠的反应中,钠离子被还原,氯离子被氧化 |
| B.湿法炼铜与火法炼铜的反应中,铜元素都发生还原反应 |
| C.用磁铁矿炼铁的反应中,1 mol Fe3O4被CO还原成Fe,转移9 mol e− |
| D.铝热法还原铁的反应中,放出的热量能使铁熔化 |
| A.d元素的非金属性最强 |
| B.它们均存在两种或两种以上的氧化物 |
| C.只有a与其他元素生成的化合物都是离子化合物 |
| D.b、c、d与氢形成的化合物中化学键均为极性共价键 |
| A.二氧化碳溶于水且能反应生成碳酸,二氧化硅不溶于水不能与水反应生成硅酸 |
B.在高温下,二氧化硅与碳酸钠能发生反应:SiO2+Na2CO3 Na2SiO3+CO2↑ Na2SiO3+CO2↑ |
| C.二氧化硅的熔点比二氧化碳的熔点高 |
| D.二氧化碳通入硅酸钠溶液中,生成白色胶状沉淀 |
【知识点】 硅酸钠与二氧化碳反应解读
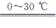 2K2FeO4+6KCl+8H2O,下列有关该反应说法正确的是( )
2K2FeO4+6KCl+8H2O,下列有关该反应说法正确的是( )| A.钾元素化合价降低 | B.Fe(OH)3发生氧化反应 |
| C.该反应是置换反应 | D.Cl2是还原剂 |
| A.加入过量碳酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸 |
| B.加入过量硫酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸 |
| C.加入过量硫酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸 |
| D.加入过量碳酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸 |
四、解答题 添加题型下试题

(1)由于O2和H2O(g)的存在对该实验有较大影响,实验中应通入气体X作为保护气,试管中的固体药品可选用
A.石灰石 B.锌粒 C.纯碱
(2)实验开始时,必须先通一段时间X气体,再加热反应物,其理由是
(3)反应结束后,待冷却至常温时,往反应后的混合物中加入稀盐酸,可观察到闪亮的火星,产生此现象的原因是副产物Mg2Si遇盐酸迅速反应生成SiH4(硅烷)气体,然后SiH4自燃。用化学方程式表示这两个反应①
(1)某课外活动小组欲探究某过氧化钠样品是否已经变质,取少量样品,溶解,加入
(2)该课外活动小组为了粗略测定过氧化钠的纯度,他们称取a g样品,并设计用下图装置来测定过氧化钠的质量分数。
①A中发生反应离子方程式为
②将仪器连接好以后,必须进行的第一步操作是
③B装置出来的气体是否需要干燥
④写出装置C中发生的所有反应的化学方程式
⑤D中NaOH溶液的作用
⑥实验结束时,读取实验中生成气体的体积时,不合理的是
a.直接读取气体体积,不需冷却到室温
b.上下移动量筒,使得E、F中液面高度相同
c.视线与凹液面的最低点相平读取量筒中水的体积
⑦读出量筒内水的体积后,折算成标准状况下氧气的体积为V mL,则样品中过氧化钠的质量分数为
⑧实验完成后E到F之间导管内残留水的体积会使测量结果
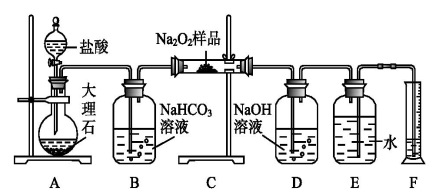
 2CH3COOH。现以A为主要原料合成化合物E,其合成路线如图1所示。回答下列问题:
2CH3COOH。现以A为主要原料合成化合物E,其合成路线如图1所示。回答下列问题: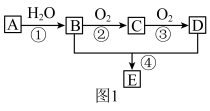
(1)写出下列物质的官能团名称:B:
(2)反应④的化学方程式为
(3)某学习小组设计物质B催化氧化的实验装置如下,根据图2装置回答问题。
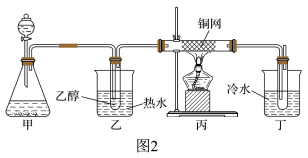
①装置甲锥形瓶中盛放的固体药品可能为
A.Na2O2 B.KClC.Na2CO3 D.MnO2
②实验过程中,丙装置硬质玻璃管中发生反应的化学方程式为
③物质B的催化氧化产物与葡萄糖具有相同的特征反应,将所得的氧化产物滴加到新制氢氧化铜悬浊液中加热,现象为
 R-NH2;②苯环上原有的取代基对新导入的取代基进入苯环的位置有显著影响。以下是用苯作原料制备一系列化合物的转化关系图:
R-NH2;②苯环上原有的取代基对新导入的取代基进入苯环的位置有显著影响。以下是用苯作原料制备一系列化合物的转化关系图: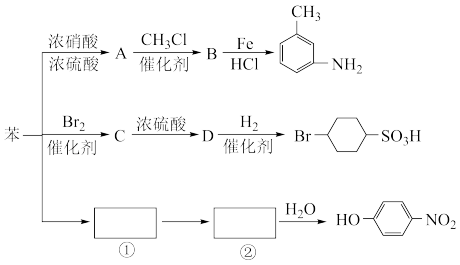
(1)A转化为B的化学方程式是
(2)图中“苯→①→②”省略了反应条件,请写出①②物质的结构简式:①
(3)苯的二氯代物有
(4)有机物
 的所有原子
的所有原子试卷分析
试卷题型(共 34题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 二氧化硫与二氧化碳的性质区别 | |
| 2 | 0.65 | 氧化还原反应基本概念 氧化还原反应的应用 | |
| 3 | 0.85 | 明矾 明矾的净水作用及原理 | |
| 4 | 0.85 | 原电池 | |
| 5 | 0.65 | 气体摩尔体积 阿伏加德罗常数的应用 结合气体物质与NA相关推算 结合物质结构基础知识与NA相关推算 | |
| 6 | 0.85 | 铁 人体健康基本维护 | |
| 7 | 0.65 | 阿伏加德罗定律及其推论 结合物质结构基础知识与NA相关推算 | |
| 8 | 0.85 | 氯气的实验室制法 | |
| 10 | 0.85 | 物质的量浓度概念、含义 | |
| 11 | 0.94 | 氧化还原反应定义、本质及特征 氧化还原反应的规律 铁盐 铁盐的检验 | |
| 12 | 0.4 | 阿伏加德罗定律 阿伏加德罗定律及其推论 | |
| 13 | 0.65 | 原电池原理理解 原电池电子流向判断及应用 原电池电极反应式书写 新型电池 | |
| 14 | 0.94 | 物质的量有关计算 根据n=m/M进行相关计算 | |
| 15 | 0.85 | 化学键与分子间作用力 | |
| 16 | 0.65 | 同主族元素性质递变规律 同主族元素性质递变规律理解及应用 | |
| 17 | 0.65 | 聚乙烯结构及应用 糖类综合 石油分馏 煤的干馏 | |
| 18 | 0.85 | 同主族元素性质递变规律 元素周期律的应用 同主族元素性质递变规律理解及应用 元素非金属性强弱的比较方法 | |
| 19 | 0.85 | 化学物质的分类方法 无机物质的分类 硅酸盐组成的表示方法 几种常见硅酸盐矿物 | |
| 20 | 0.85 | 同主族元素性质递变规律 | |
| 21 | 0.85 | 石油物理性质及组成成分 石油分馏 | |
| 22 | 0.85 | 蔗糖与麦芽糖 葡萄糖、果糖的组成与结构 蔗糖与麦芽糖的水解 淀粉、纤维素的水解 | |
| 23 | 0.65 | 钠 钠的化学性质 钠与水反应原理 | |
| 24 | 0.65 | 化学键基本概念 化学键概念理解及判断 | |
| 25 | 0.85 | 浓硫酸的吸水性 浓硫酸的脱水性 浓硫酸的强氧化性 | |
| 26 | 0.85 | 氧化还原反应方程式的配平 氧化还原反应在生活、生产中的应用 铝热反应 常见金属的冶炼 | |
| 27 | 0.65 | 元素周期律、元素周期表的推断 元素金属性与非金属性递变规律的理解及应用 根据原子结构进行元素种类推断 | |
| 28 | 0.85 | 硅酸钠与二氧化碳反应 | |
| 29 | 0.65 | 氧化还原反应的应用 氧化还原反应在生活、生产中的应用 氧化还原反应的规律 铁的其他化合物 | |
| 30 | 0.85 | 离子反应在混合物分离、除杂中的应用 物质分离、提纯的常见化学方法 | |
| 二、未知 | |||
| 9 | 0.85 | 酸、碱、盐、氧化物的概念及其相互联系 电解质与非电解质 非电解质、电解质物质类别判断 | 未知 |
| 三、解答题 | |||
| 31 | 0.4 | 二氧化硅 镁 综合实验设计与评价 | 实验探究题 |
| 32 | 0.4 | 过氧化钠 物质含量的测定 综合实验设计与评价 | 实验探究题 |
| 33 | 0.65 | 乙烯的加成反应 乙醇催化氧化 乙醛与新制氢氧化铜悬浊液的反应 有机物的合成 | 有机推断题 |
| 34 | 0.4 | 同分异构体的数目的确定 苯的取代反应 芳香烃空间结构 根据题给物质选择合适合成路线 | 有机推断题 |



