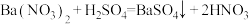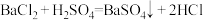云南省镇康县第一中学2019-2020学年高一12月月考化学试题
云南
高一
阶段练习
2020-01-11
375次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、化学实验基础
一、单选题 添加题型下试题
| A.1mol氢气含有的原子数为2NA |
| B.NA个水分子中含有氢原子的物质的量为2 mol |
| C.1 mol 氧气中含有的分子数为2NA |
| D.含有NA个氧原子的硫酸的物质的量是0.25 mol |
A.①能控制气体发生速度 |
B.若气体不纯而万一发生爆炸,②具有保护装置的作用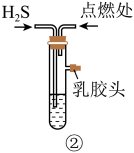 |
C.③用于硫化氢的干燥和收集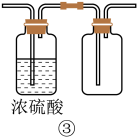 |
D.④用于硫化氢的尾气处理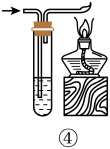 |
| A.纯净的铁是光亮的银白色金属 |
| B.铁能被磁铁吸引,在磁场作用下,铁自身也能产生磁性 |
| C.铁是地壳中含量最多的金属元素,所以分布在地壳的铁有游离态也有化合态 |
| D.纯铁的抗蚀能力相当强,在干燥的空气里不易被氧化 |
| A.1:1 | B.2:1 | C.1:2 | D.1:3 |
【知识点】 阿伏加德罗定律及其推论解读 阿伏加德罗定律的应用解读
| A.酚酞溶液 | B.氯化钡溶液 | C.氢氧化钠溶液 | D.硝酸银溶液 |
| A.同温同压下,相同体积的物质,其物质的量必然相等 |
| B.任何条件下,等物质的量的乙烯和一氧化碳所含的分子数必然相等 |
| C.1 L一氧化碳气体一定比1 L氧气的质量小 |
| D.同温同压下,等体积的物质所含的分子数一定相等 |
【知识点】 阿伏加德罗定律及其推论解读 阿伏加德罗定律的应用解读
①试管 ②烧杯 ③酒精灯 ④试管夹 ⑤石棉网 ⑥泥三角 ⑦坩埚 ⑧铁架台(带铁圈)
| A.③⑥⑦⑧ | B.②③⑤⑧ | C.①③④⑤ | D.②③⑤⑥ |
【知识点】 仪器使用与实验安全
| A.Ba2++SO42—=BaSO4↓可表示氯化钡溶液与硫酸钠溶液的反应 |
| B.H++OH-=H2O可表示强碱氢氧化钠、氢氧化钾分别与盐酸、硫酸间的反应 |
| C.CO32—+2H+=CO2↑+H2O表示可溶性碳酸盐与强酸之间的复分解反应 |
| D.BaCO3+2H+=Ba2++CO2↑+H2O表示碳酸钡与强酸之间的复分解反应 |
【知识点】 离子反应的发生及书写 离子方程式的书写解读 离子方程式的正误判断解读
| A.都是酸性氧化物 | B.都能与水反应 |
| C.都与氢氧化钠溶液反应 | D.高温下都与单质碳反应 |
| A.氯气溶于水:Cl2+H2O===2H++Cl-+ClO- |
| B.FeSO4溶液与氨水反应的离子方程式:Fe2++2NH3·H2O===Fe(OH)2↓+NH4+ |
| C.酸性溶液中KIO3与KI反应生成I2:IO3-+I-+6H+===I2+3H2O |
| D.NaHCO3溶液中加足量Ba(OH)2溶液:2HCO3-+Ba2++2OH-===BaCO3↓+2H2O+CO2↑ |
【知识点】 离子反应的发生及书写
| A.CO2→CO | B.Cl﹣→Cl2 | C.Fe3+→Fe2+ | D.CO32—→CO2 |
【知识点】 氧化还原反应定义、本质及特征解读
| A.盐酸、烧碱、胆矾 | B.硫酸、纯碱、食盐 |
| C.碳酸、乙醇、醋酸钠 | D.磷酸、熟石灰、苛性钠 |
【知识点】 树状分类法解读 酸、碱、盐、氧化物的概念及其相互联系解读
| A.蒸发 | B.萃取 | C.液体过滤 | D.升华 |
【知识点】 仪器使用与实验安全 物质分离、提纯的常见物理方法
| A.分液、萃取、蒸馏 | B.萃取、蒸馏、分液 |
| C.分液、蒸馏、萃取 | D.蒸馏、萃取、分液 |
| A.金属镁与稀盐酸反应:Mg+2HCl === Mg2++2Cl-+H2↑ |
B.氯化钡溶液与硫酸反应:Ba2++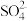 === BaSO4↓ === BaSO4↓ |
| C.碳酸钠溶液与盐酸反应:Na2CO3+2H+=== 2Na++CO2↑+H2O |
D.盐酸与大理石反应:2H++ ===CO2↑+H2O ===CO2↑+H2O |
| A.氢氧化钠的摩尔质量为40 g |
| B.氢原子的摩尔质量是1 g·mol-1 |
| C.1 mol水的质量是18 g·mol-1 |
| D.二氧化碳的摩尔质量为44 g |
【知识点】 摩尔质量
| A.稀硫酸 | B.稀盐酸 | C.浓硫酸 | D.氢氧化钠溶液 |
【知识点】 铝
 溶液中,金属恰好溶解,分别转化成
溶液中,金属恰好溶解,分别转化成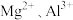 和
和 ;还原产物为NO,在标准状况下体积为6.72L。在反应后的溶液中加入300mL某浓度的NaOH溶液,金属阳离子恰好全部沉淀,干燥后测得质量为27.2g。下列有关推断正确的是
;还原产物为NO,在标准状况下体积为6.72L。在反应后的溶液中加入300mL某浓度的NaOH溶液,金属阳离子恰好全部沉淀,干燥后测得质量为27.2g。下列有关推断正确的是A.参加反应的 的物质的量为0.9mol 的物质的量为0.9mol | B.NaOH的物质的量浓度为6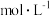 |
| C.参加反应的金属的质量为11.9g | D. 的物质的量浓度为3 的物质的量浓度为3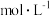 |
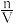 中,n是指( )
中,n是指( )| A.溶液的物质的量 | B.溶质的物质的量 |
| C.溶剂的物质的量 | D.物质的量 |
【知识点】 物质的量浓度概念、含义解读
| A.氧化铝固体不溶于水,不导电,它是非电解质 |
| B.氧化铝熔点很高,是一种较好的耐火材料 |
| C.氧化铝是一种白色的固体,是冶炼铝的原料 |
| D.铝表面形成的氧化铝薄膜可防止铝被腐蚀 |
【知识点】 氧化铝
| A.6.05 g | B.5.35 g | C.12.10 g | D.16.40 g |
| A.0.2 mol·L-1 | B.0.01 mol·L-1 | C.0.1 mol·L-1 | D.0.02 mol·L-1 |
【知识点】 物质的量浓度计算-溶液混合的有关计算解读
A.浓硫酸的装运包装箱应贴如图所示的标识 |
| B.取用任何试剂时,没用完的试剂均不可以放回原试剂瓶 |
| C.金属钠保存在煤油中 |
| D.液溴易挥发,保存时需加水液封 |
| A.二氧化碳或二氧化硫通入氯化钙溶液中 |
| B.过量二氧化碳通入澄清石灰水中 |
| C.过量二氧化硫通入氢氧化钡溶液中 |
| D.过量二氧化碳通入硅酸钠溶液中 |
| A.物质的量是表示物质质量的物理量 |
| B.物质的量是表示物质多少的物理量 |
| C.物质的量是含有一定数目粒子集合体的物理量 |
| D.物质的量既可表示物质的质量又可表示物质的数量 |
二、解答题 添加题型下试题
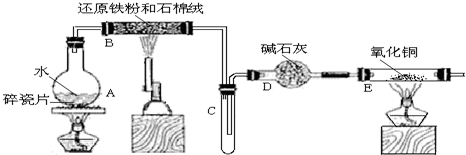
(1)装置B中发生反应的化学方程式是
(2)装置E中的现象是
(3)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。写出可能发生的有关反应化学方程式:
(4)该小组学生利用上述滤液制取FeCl3•6H2O晶体,设计流程如图所示:
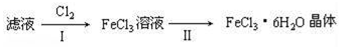
①步骤I中通入Cl2的作用是
②简述检验滤液中Fe3+的操作方法
③步骤Ⅱ从FeCl3稀溶液中得到FeCl3•6H2O晶体的主要操作包括:

请填写下列空白:
(1)写出下列物质的化学式A
(2)若C→D为化合反应,则此时的化学方程式
(3)写出E→F的化学方程式
(4)写出反应④的离子方程式
【知识点】 无机综合推断 铝 与“铁三角”有关的推断解读
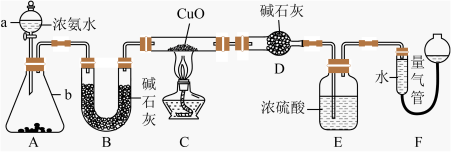
(1)仪器a的名称为
(2)实验室中,利用装置A,还可制取的无色气体是
A.Cl2 B.O2 C.CO2 D.NO2
(3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管有无色无味的气体,上述现象证明NH3具有
(4)E装置中浓硫酸的作用
(5)读取气体体积前,应对装置F进行的操作:
(6)实验完毕,若测得干燥管D增重mg,装置F测得气体的体积为nL(已折算成标准状况),则氨分子中氮、氢的原子个数比为
 4NO2↑+O2↑+2H2O)。
4NO2↑+O2↑+2H2O)。
请回答下列问题:
(1)检查装置气密性后,将燃烧匙中的木炭在酒精灯上加热至炽热状态,伸入三颈烧瓶中,生成的气体的颜色为
(2)装置C中盛有足量Ba(OH)2溶液,炽热的木炭与浓硝酸反应后可观察到C中出现白色沉淀,该白色沉淀为
(3)装置B的作用是
(4)装置D中收集到了无色气体,有同学认为是NO,还有同学认为是O2。
①下列对该气体的检验方法合适的是
A.敞口观察装置D中集气瓶内气体的颜色变化
B.将湿润的蓝色石蕊试纸伸入集气瓶内,观察蓝色石蕊试纸是否变红
C.将带火星的木条伸入集气瓶中,观察木条是否复燃
②如果D中集气瓶内收集到的无色气体是氧气,则氧气的来源是
【知识点】 硝酸 一氧化氮 二氧化氮 物质性质实验方案的设计解读

(1)写出A~F各物质的化学式:
A
(2)写出A、B跟水反应的离子方程式:
试卷分析
试卷题型(共 33题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 阿伏加德罗常数的应用 根据n=N/NA进行相关计算 结合气体物质与NA相关推算 结合物质结构基础知识与NA相关推算 | |
| 2 | 0.65 | 硫化氢 综合实验设计与评价 | |
| 3 | 0.65 | 铁的物理性质 | |
| 4 | 0.65 | 阿伏加德罗定律及其推论 阿伏加德罗定律的应用 | |
| 5 | 0.85 | 氯气的化学性质 氯水的性质 | |
| 6 | 0.65 | 阿伏加德罗定律及其推论 阿伏加德罗定律的应用 | |
| 7 | 0.85 | 仪器使用与实验安全 | |
| 8 | 0.65 | 离子反应的发生及书写 离子方程式的书写 离子方程式的正误判断 | |
| 9 | 0.65 | 二氧化硅 二氧化硅的化学性质 二氧化硅与二氧化碳结构与性质的比较 | |
| 10 | 0.65 | 离子反应的发生及书写 | |
| 11 | 0.85 | 氧化还原反应定义、本质及特征 | |
| 12 | 0.65 | 树状分类法 酸、碱、盐、氧化物的概念及其相互联系 | |
| 13 | 0.85 | 仪器使用与实验安全 物质分离、提纯的常见物理方法 | |
| 14 | 0.85 | 蒸馏与分馏 萃取和分液 | |
| 15 | 0.65 | 离子反应的发生条件 离子方程式的书写 离子方程式的正误判断 | |
| 16 | 0.94 | 摩尔质量 | |
| 17 | 0.85 | 铝 | |
| 18 | 0.4 | 基于氧化还原反应守恒规律的计算 硝酸的强氧化性 有关酸性环境下硝酸根氧化性的有关计算 铁及铁的氧化物混合物反应的相关计算 | |
| 19 | 0.65 | 金属与非金属 | |
| 20 | 0.94 | 物质的量浓度概念、含义 | |
| 21 | 0.65 | 氧化铝 | |
| 22 | 0.65 | 化学方程式计算中物质的量的运用 依据物质的量浓度公式的基础计算 碳酸钠、碳酸氢钠混合物的有关求算 | |
| 23 | 0.65 | 铵盐的不稳定性 碳酸氢钠 | |
| 24 | 0.85 | 物质的量浓度计算-溶液混合的有关计算 | |
| 25 | 0.65 | 钠单质的保存与用途 化学实验基础操作 实验安全 | |
| 26 | 0.65 | 二氧化硫与二氧化碳的性质区别 酸性氧化物的通性 硅酸钠与二氧化碳反应 | |
| 27 | 0.65 | 物质的量的含义 摩尔 | |
| 28 | 0.94 | 离子方程式的书写 | |
| 二、解答题 | |||
| 29 | 0.65 | 铁与水蒸气的反应 化学实验探究 物质制备的探究 综合实验设计与评价 | 实验探究题 |
| 30 | 0.65 | 无机综合推断 铝 与“铁三角”有关的推断 | 无机推断题 |
| 31 | 0.65 | 氨的还原性 氨气的实验室制法 物质性质的探究 | 实验探究题 |
| 32 | 0.65 | 硝酸 一氧化氮 二氧化氮 物质性质实验方案的设计 | 实验探究题 |
| 33 | 0.65 | 无机综合推断 氯气 二氧化硫的化学性质 | 无机推断题 |

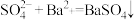 表示的是
表示的是