2015-2016学年广东省惠州市高一上学期期末质检化学试卷
广东
高一
期末
2017-07-27
652次
整体难度:
适中
考查范围:
常见无机物及其应用、认识化学科学、化学与STSE、化学实验基础、化学反应原理
一、单选题 添加题型下试题
| A.单质钠 | B.氯化钠 | C.次氯酸钠 | D.碳酸钠 |
【知识点】 钠
| A.NaOH | B.Na2SO4 | C.酒精(C2H5OH) | D.Cl2 |
【知识点】 非电解质、电解质物质类别判断解读
| A.次氯酸钙 | B.氯化钙 |
| C.次氯酸 | D.次氯酸钙与氯化钙 |
【知识点】 漂白粉和漂粉精的制备原理解读
| A.NH3→ NO | B.HCl→H2 | C.NaCl→AgCl | D.Fe3+ → Fe2+ |
【知识点】 氧化还原反应的几组概念解读
| A.易溶于水 | B.能与碱反应 | C.受热易分解 | D.在水中易发生电离 |
【知识点】 铵盐
| A.均为白色固体 | B.都能与水反应生成碱 |
| C.都具有漂白作用 | D.都为碱性氧化物 |
| A.盐酸 | B.Fe (OH)3胶体 | C.氯化钠溶液 | D.CuSO4溶液 |
【知识点】 分散系
| A.Cl2+H2O==HCl+HClO | B.Fe2O3+3CO 2Fe+3CO2 2Fe+3CO2 |
| C.2F2+2H2O==4HF+O2 | D.2Na+2H2O==2NaOH+H2↑ |
| A.①② | B.①③ | C.③④ | D.①②③④ |
【知识点】 氧化性、还原性强弱的比较解读
| A.1 | B.2 | C.3 | D.4 |
【知识点】 化学与环境保护
| A.形成均匀的无色溶液 |
| B.形成均匀的紫红色溶液 |
| C.液体分层,下层呈紫红色 |
| D.液体分层,上下层均呈无色 |
| A.0.01mol/L | B.0.1mol/L | C.1mol/L | D.10mol/L |
【知识点】 化学计量
| A.钠与水反应放出氢气 | B.钠与水反应放出氧气 |
| C.实验室中钠常保存在煤油中 | D.Na2O2与水反应放出氧气 |
| A.KSCN | B.BaCl2 | C.HCl | D.NaOH |
| A.将BaCl2溶液分别滴入两种液体中,变浑浊的是硫酸溶液 |
| B.将两种液体分别滴入碳酸氢钠粉末中,有气泡产生的是硫酸溶液 |
| C.将酚酞溶液分别滴入两种液体中,变红色的是硫酸溶液 |
| D.测试这两种液体的导电性,导电性强的是硫酸溶液 |
① 过滤 ② 蒸发 ③ 溶解 ④ 向细口瓶中转移液体
| A.①和② | B.①和③ | C.③和④ | D.①和④ |
| A.可以从海水中制取Br2 | B.可以从海水中制取金属Mg |
| C.可以从海水中直接提取NaCl | D.可以从海水中直接提取金属Na |
| 选项 | 待提纯的物质 | 选用的试剂 | 操作方法 |
| A | NaOH(Na2CO3) | 盐酸 | - |
| B | CO2(CO) | CuO | 加热 |
| C | Fe (Zn) | 稀硫酸 | 过滤 |
| D | CO2(HCl) | Na2CO3溶液 | 洗气 |
| A.A | B.B | C.C | D.D |
| A.燃煤的煤渣用于制造建筑材料 |
| B.焚烧垃圾的烟气直接排入空气中 |
| C.用废弃的泡沫包装材料制取液体燃料 |
| D.用CaCO3除去燃煤烟气中的S02,并制得石膏 |
【知识点】 化学与环境保护
| A.分液、萃取、蒸馏 | B.萃取、蒸馏、分液 |
| C.分液、蒸馏、萃取 | D.蒸馏、萃取、分液 |
| A.两者都易溶于水 | B.两者都污染环境,危害健康 |
| C.两者都能使品红溶液褪色 | D.两者都是形成酸雨的主要原因 |
| A.部分铁粉被氧化 | B.全部Fe3+被还原 |
| C.溶液质量减轻 | D.溶液质量增加 |
| A.溶液的导电性与溶液中离子的浓度有关 |
| B.溶液的导电性与溶液中离子数目的多少有关 |
| C.灯泡最暗时溶液中无自由移动的离子 |
| D.往氢氧化钡溶液中滴加盐酸与滴加硫酸时现象相同 |
二、多选题 添加题型下试题
| A.金属钠着火,用泡沫灭火器扑灭 |
| B.实验台上的酒精灯碰翻着火,立即用湿抹布扑灭 |
| C.皮肤溅上浓H2SO4,立即用大量水冲洗 |
| D.汞洒落地面,应立即撒上一层硫黄粉 |
【知识点】 仪器使用与实验安全
三、单选题 添加题型下试题
| A.钠跟水反应:2Na + 2H2O = 2Na+ + 2OH-+ H2↑ |
| B.铁粉跟稀硫酸反应:2Fe + 6H+ = 2Fe3++ 3H2↑ |
| C.氢氧化钡溶液跟稀硫酸反应:Ba2+ + SO42-= BaSO4↓ |
| D.碳酸钙跟盐酸反应:CO32-+ 2H+ = H2O + CO2↑ |
【知识点】 离子反应的发生及书写 离子方程式的书写解读 离子方程式的正误判断解读
| A.浓硫酸和浓硝酸都不能用来直接跟锌粒反应制氢气 |
| B.浓硫酸和浓硝酸都能与金属铜反应 |
| C.浓硫酸和浓硝酸加水稀释后都能与金属铜反应 |
| D.浓硫酸和浓硝酸在常温下都能用金属铝或铁制容器盛放 |
| A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32— |
| B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42— |
| C.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
| D.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ |
| A.Na+、K+、HCO3-、NO3- | B.NH4+、Al3+、SO42-、NO3- |
| C.K+、Fe2+、NH4+、NO3- | D.NH4+、Na+、NO3-、OH- |
【知识点】 离子共存
| A.①③ | B.②③ | C.①④ | D.②④ |
【知识点】 氧化还原反应基本概念 氧化还原反应的应用 碘与淀粉的显色反应解读
 的物质的量为
的物质的量为| A.0.1mol | B.0.5mol | C.0.15mol | D.0.25mol |
四、多选题 添加题型下试题
| A.Cl2是氧化剂,反应中Cl原子得到电子 |
| B.当1molCl2完全反应时,有2mol电子发生转移 |
| C.NaBr是还原剂,反应中溴离子得到电子 |
| D.当1molNaBr完全反应时,有1mol电子发生转移 |
【知识点】 氧化还原反应基本概念
五、单选题 添加题型下试题
| A.标准状况下,22.4LH2O含有的分子数为NA |
| B.标准状况下,22.4L 氖气含有的氖原子数为2 NA |
| C.常温常压下,22.4L CO2气体含有的分子数为NA |
| D.在1L的0.5mol·/L的MgCl2溶液中,含Cl-数为NA |
【知识点】 化学计量
| A.先加入BaCl2溶液,后再加入HNO3 |
| B.先加入HCl,后再加AgNO3溶液 |
| C.先加入Ba(NO3)2溶液,后再加入HCl |
| D.先加入HCl,后再加入BaCl2溶液 |
【知识点】 化学实验基础
| A.NaHCO3比Na2CO3热稳定性差 |
| B.NaHCO3比Na2CO3与稀盐酸反应的速度快 |
| C.在相同温度下,Na2CO3的溶解度大于NaHCO3 |
| D.Na2CO3能使澄清石灰水变浑浊,而NaHCO3不行 |
【知识点】 碳酸钠与碳酸氢钠性质的比较解读
| A.1 :3 | B.3 :1 | C.1 :1 | D.3 :2 |
【知识点】 钠及其化合物
六、解答题 添加题型下试题
(1)写出浓硫酸与木炭反应方程式,并标明电子转移的方向和数目:
【装置设计】组装如下的实验装置,然后进行实验探究。

(2)装入反应物之前,必须先
【实验探究】
(3)观察实验,完成实验现象的部分记录:
| 实验装置 | ① | ③ |
| 实验现象 |


实验操作和现象:打开分液漏斗的活塞,缓缓滴加一定量浓盐酸,点燃酒精灯;一段时间后,关闭分液漏斗的活塞,熄灭酒精灯。
(1)烧瓶中所进行反应的离子方程式为
(2)图1中饱和食盐水的作用是
(3)若用图Ⅱ装置收集多余的氯气,请在虚线框内画出该装置简图
(4)修改方案后,该小组同学制得了较高浓度的NaClO溶液。他们把漂白液和滴有酚酞的红色Na2SO3溶液混合后,得到无色溶液。
提出猜想:
Ⅰ.NaClO把Na2SO3氧化成Na2SO4
Ⅱ.NaClO把酚酞氧化了
Ⅲ.NaClO把Na2SO3和酚酞都氧化了
① 下列实验方案中,可以证明NaClO氧化了Na2SO3的是
a.向混合后的溶液中加入过量盐酸
b.向混合后的溶液中加入过量盐酸,再加入氯化钡溶液
c.向混合后的溶液中加入过量硝酸,再加入硝酸银溶液
d.向混合后的溶液中加入氢氧化钡溶液,再加入过量盐酸
② 为证明NaClO氧化了酚酞,可进行的实验是
七、填空题 添加题型下试题

(已知:氧化性强弱顺序: ClO3-> MnO2 > Fe3+)
(1)铝与二氧化锰在高温下发生置换反应,该反应的化学方程式为
(2)请配平第②步反应的离子方程式:
(3)第③步蒸发操作必需的仪器有铁架台(含铁圈)、玻璃棒、
第③步蒸发得到的固体中除了含有NaClO3和NaOH外,还一定含有
(4)若粗MnO2样品质量为23.0g,标准状况下,第①步反应收集448mLCO2气体,则原样品中MnCO3的质量百分含量为
【知识点】 化学实验基础 氧化还原反应方程式的配平解读
八、解答题 添加题型下试题
Ⅰ、他们先把铜粉放在空气中灼烧,再与稀硝酸反应制取硝酸铜。
(1)如果直接用铜屑与稀硝酸反应来制取硝酸铜:
①铜屑与稀硝酸反应的化学反应方程式为
②可能导致的两个不利因素是
(2)实验中,欲从反应后的溶液中得到硝酸铜晶体,实验操作步骤按顺序是
Ⅱ、为了探究Cu(NO3)2在酸性条件下跟铁单质的反应。他们取一支试管,加入Cu(NO3)2溶液,滴入适量稀硫酸酸化,再加入一定量铁粉,实验后没有固体残留物质。
(3)该探究小组对反应后溶液中铁元素的价态进行探究,他们设计了实验方案,并进行实验。请按下表格式补充写出实验操作步骤、预期现象与结论。
| 实验操作步骤 | 预期现象与结论 |
| 步骤1:观察样品 | 溶液呈蓝绿色,① |
| 步骤2:取少量溶液,滴加酸性KMnO4溶液 | ② |
| 步骤3:③另取少量溶液,滴加KSCN溶 | ③ |
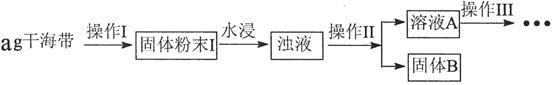
(1) 操作I为灼烧,则灼烧时用
(2) 水浸时通常要将悬浊液煮沸2-3min,目的是
(3) 操作III是某同学对溶液A中碘元素的存在形式进行的探究实验。
[推测]:① 以
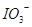 形式存在; ② 以
形式存在; ② 以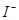 形式存在
形式存在[查阅资料]:IO3- 和H2O2都具有较强的氧化性;
将上述溶液稀释配制成200mL溶液,请完成下列实验探究。
限选试剂:
 溶液、KSCN溶液、
溶液、KSCN溶液、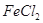 溶液、稀硫酸
溶液、稀硫酸| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 取少量稀释后的溶液A加入淀粉后再用硫酸酸化,分装于试管I、II | 无现象 |  |
| ② | 往试管I中加入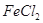 溶液,后加入2滴KSCN溶液并振荡; 溶液,后加入2滴KSCN溶液并振荡; | ||
| ③ | 溶液变蓝 |
(4) 通过定量的检测实验操作和方法,测定某些数据,计算上述海带样品中碘元素的含量。
【知识点】 物质含量的测定 实验方案设计的基本要求解读 综合实验设计与评价解读
试卷分析
试卷题型(共 54题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 钠 | |
| 2 | 0.85 | 物质的分类 | |
| 3 | 0.85 | 非电解质、电解质物质类别判断 | |
| 4 | 0.85 | 漂白粉和漂粉精的制备原理 | |
| 5 | 0.65 | 氧化还原反应的几组概念 | |
| 6 | 0.85 | 硫 硫单质的化学性质 硫与金属单质的反应 | |
| 7 | 0.85 | 铵盐 | |
| 8 | 0.64 | 氧族元素及其化合物 | |
| 9 | 0.85 | 硫酸盐 碳酸钠 | |
| 10 | 0.94 | 氧化钠物理性质及用途 氧化钠的化学性质 过氧化钠与水的反应 过氧化钠的强氧化性 | |
| 11 | 0.64 | 化学计量 | |
| 12 | 0.64 | 卤素及其化合物 | |
| 13 | 0.85 | 分散系 | |
| 14 | 0.85 | 氧化还原反应基本概念 氧化还原反应的几组概念 常见氧化剂与还原剂 | |
| 15 | 0.65 | 氧化性、还原性强弱的比较 | |
| 16 | 0.94 | 食品添加剂 | |
| 17 | 0.85 | 氧化还原反应的规律 过氧化钠 | |
| 18 | 0.64 | 化学与环境保护 | |
| 19 | 0.65 | 溴、碘的性质 萃取和分液 | |
| 20 | 0.64 | 化学计量 | |
| 21 | 0.65 | 钠单质的保存与用途 钠与水反应原理 过氧化钠与水的反应 | |
| 22 | 0.85 | 离子反应在混合物分离、除杂中的应用 离子反应在化合物组成的分析、鉴定的应用 离子的检验 | |
| 23 | 0.64 | 化学计量 阿伏加德罗定律 | |
| 24 | 0.64 | 化学实验基础 氧族元素及其化合物 | |
| 25 | 0.64 | 化学实验基础 氮族元素及其化合物 钠及其化合物 | |
| 26 | 0.65 | 常用仪器及使用 化学实验基础操作 | |
| 27 | 0.94 | 海水资源综合利用 海水提取溴 海水提取镁 | |
| 28 | 0.65 | 吸氧腐蚀 金属的防护 金属腐蚀与防护 | |
| 29 | 0.85 | 次氯酸及其性质 氯气的化学性质 氯水的性质 过氧化钠与水的反应 | |
| 30 | 0.85 | Fe2+的还原性 铁盐的检验 | |
| 31 | 0.85 | 离子反应在混合物分离、除杂中的应用 物质的分离、提纯 物质分离、提纯的常见化学方法 物质分离、提纯综合应用 | |
| 32 | 0.94 | 化学与环境保护 | |
| 33 | 0.85 | 蒸馏与分馏 萃取和分液 | |
| 34 | 0.4 | 钠及其化合物 | |
| 35 | 0.65 | 二氧化硫 硫、氮氧化物对人体、环境的危害 酸雨 大气污染来源及危害 | |
| 36 | 0.65 | 铁盐的检验 依据Fe3+与其他物质氧化性强弱关系的相关计算 | |
| 37 | 0.65 | 物质水溶液的导电性 | |
| 39 | 0.4 | 离子反应的发生及书写 离子方程式的书写 离子方程式的正误判断 | |
| 40 | 0.94 | 硝酸的强氧化性 酸的通性 浓硫酸的强氧化性 | |
| 41 | 0.65 | 铵根离子的检验 硫酸根离子的检验 离子的检验 常见阳离子的检验 | |
| 42 | 0.64 | 离子共存 | |
| 43 | 0.85 | 氧化还原反应基本概念 氧化还原反应的应用 碘与淀粉的显色反应 | |
| 44 | 0.85 | 物质的量浓度与溶液混合的计算 离子反应的实际应用 限定条件下的离子共存 | |
| 46 | 0.4 | 化学计量 | |
| 47 | 0.64 | 化学实验基础 | |
| 48 | 0.65 | 碳酸钠与碳酸氢钠性质的比较 | |
| 49 | 0.4 | 钠及其化合物 | |
| 二、多选题 | |||
| 38 | 0.65 | 仪器使用与实验安全 | |
| 45 | 0.64 | 氧化还原反应基本概念 | |
| 三、解答题 | |||
| 50 | 0.4 | 氧族元素及其化合物 探究性实验 | 实验探究题 |
| 51 | 0.4 | 卤素及其化合物 探究性实验 | 实验探究题 |
| 53 | 0.65 | 物质性质的探究 | 实验探究题 |
| 54 | 0.4 | 物质含量的测定 实验方案设计的基本要求 综合实验设计与评价 | 实验探究题 |
| 四、填空题 | |||
| 52 | 0.4 | 化学实验基础 氧化还原反应方程式的配平 | |