云南省腾冲市第八中学2018-2019学年高一上学期期中考试化学试题
云南
高一
期中
2018-12-08
398次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、化学实验基础、化学与STSE
一、未知 添加题型下试题
二、单选题 添加题型下试题
| A.0.15 mol•L﹣1 | B.0.2 mol•L﹣1 | C.0.25 mol•L﹣1 | D.0.30 mol•L﹣1 |
【知识点】 物质的量浓度计算-溶液混合的有关计算解读
| A.某固体中加入稀盐酸,产生了无色气体,证明该固体一定是碳酸盐 |
| B.某溶液中滴加BaCl2溶液,生成不溶于稀硝酸的白色沉淀,该溶液中一定含SO42- |
| C.某无色溶液滴入无色酚酞试液显红色,该溶液一定显碱性 |
| D.验证烧碱溶液中是否含有Cl-,先加稀盐酸除去OH-,再加硝酸银溶液,有白色沉淀出现,证明含Cl- |
| A.④③①②⑤ | B.④⑤③②① | C.④③②①⑤ | D.④②③①⑤ |
| A.BaCl2溶液和稀硫酸 | B.BaCl2溶液 |
| C.Ba(NO3)2溶液 | D.BaCl2溶液和稀盐酸 |
| A.蒸发皿 | B.试管 | C.烧杯 | D.坩埚 |
【知识点】 仪器使用与实验安全
| A.凡是给玻璃仪器加热,都要加垫石棉网 |
| B.给试管里的液体加热,液体的体积一般不超过试管容积的2/3 |
| C.试管和烧杯都可以直接在火焰上加热 |
| D.加热后的蒸发皿,要用坩埚钳夹取 |
①取少量溶液滴加Ba(NO3)2溶液,产生白色沉淀
②然后继续加入稀盐酸至溶液呈酸性,产生无刺激性气味且能使澄清石灰水变浑浊的无色气体;白色沉淀部分溶解
③取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加AgNO3溶液,产生白色沉淀。
根据实验,以下推测不正确的是( )
A.一定有 | B.一定有 |
| C.不能确定Cl-是否存在 | D.不能确定 是否存在 是否存在 |
| A.加入适量Na2SO4溶液后过滤 | B.加入适量NaOH溶液后过滤 |
| C.加入过量NaOH溶液后蒸发 | D.加入过量Na2CO3溶液后过滤 |
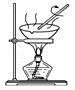
| A.组装实验装置时,应先固定好铁圈,放上蒸发皿,再放酒精灯 |
| B.给蒸发皿内所盛液体加热时,必须垫上石棉网 |
| C.玻璃棒的作用是搅拌,防止因局部过热而使固体迸溅 |
| D.蒸发的过程中,用酒精灯一直加热到全部固体析出,没有水分 |
| A.加热溶解 | B.趁热过滤 | C.蒸发结晶 | D.降温结晶 |
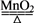 2KCl+3O2↑,反应后从剩余固体中回收二氧化锰的操作顺序正确的是( )
2KCl+3O2↑,反应后从剩余固体中回收二氧化锰的操作顺序正确的是( )| A.溶解、过滤、蒸发、洗涤 | B.溶解、过滤、洗涤、加热 |
| C.溶解、蒸发、洗涤、过滤 | D.溶解、洗涤、过滤、加热 |
【知识点】 物质分离、提纯综合应用解读 过滤解读
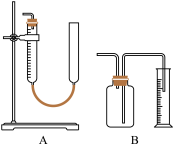
| A.使用A装置量气前,其右管中应充满相应的液体 |
| B.量气前,B装置中广口瓶通常应盛满相应的液体 |
| C.A装置收集完气体后,在读数前应使盛液管内液面与集气管内液面相平 |
| D.A装置是直接测量气体体积,而B装置直接测量的是所排出液体的体积 |
【知识点】 常见气体的制备与收集解读 实验方案设计的基本要求解读
| A.氯化镁晶体 | B.氯化钠溶液 | C.液态氯化氢 | D.熔融氢氧化钾 |
【知识点】 电解质与非电解质 电解质的电离 电解质、非电解质概念解读
| A.Cu(OH)2+HCl; Cu(OH)2+CH3COOH |
| B.CaCO3+H2SO4; Na2CO3+HCl |
| C.H2SO4+NaOH; H2SO4+Ba(OH)2 |
| D.BaCl2+H2SO4; Ba(OH)2+Na2SO4 |
【知识点】 离子反应的发生及书写 离子方程式的书写解读
| A.过滤 | B.蒸馏 | C.蒸发 | D.干燥 |
| A.氯化钠溶液(氯化钡):加硫酸溶液,过滤 |
| B.硝酸钾溶液(硝酸银):加氯化钠溶液,过滤 |
| C.氯化钠溶液(单质碘):加酒精,分液 |
| D.硝酸钾溶液(单质碘):加四氯化碳,萃取分液 |
A.称量NaOH 固体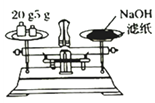 |
B.配制100mL0.1mol/L 的H2SO4 溶液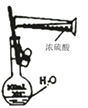 |
C.家里的食用胡麻油不小心混入了大量的水采取的分离方法 |
D.提纯Fe(OH)3 胶体 |
三、未知 添加题型下试题
四、单选题 添加题型下试题
| 目的 | 分离方法 | 原理 | |
| A | 分离溶于水的碘 | 乙醇萃取 | 碘在乙醇中的溶解度较大 |
| B | 分离汽油和四氯化碳 | 分液 | 四氯化碳和汽油的密度不同 |
| C | 除去KNO3固体中混的NaCl | 结晶 | NaCl在水中的溶解度很大 |
| D | 除去乙醇中的水 | 蒸馏 | 乙醇与水的沸点相差较大 |
| A.A | B.B | C.C | D.D |
| A.在常温常压下,28 g N2与CO混合物气体中所含的分子数目一定为NA |
| B.标准状况下,17 g氨气所含原子数目为NA |
| C.在常温常压下,11.2 L氮气所含的原子数目为NA |
| D.NA个氢分子所占有的体积一定为22.4 L |
【知识点】 物质的量及单位——摩尔 阿伏加德罗常数 摩尔质量 气体摩尔体积
| A.1 mol H+含有的电子数 |
| B.标准状况下,22.4 L酒精所含的分子数 |
| C.1.6 g CH4含有的质子数 |
| D.1 L 1 mol·L-1的硫酸钠溶液所含的Na+数 |
A. | B. | C. | D. |
【知识点】 阿伏加德罗定律 阿伏加德罗定律及其推论解读 阿伏加德罗定律的应用解读
| A.AB3 | B.AB2 | C.A3B | D.A2B3 |
【知识点】 阿伏加德罗定律及其推论解读 阿伏加德罗定律的应用解读
①具有相同的密度 ②具有相同的体积 ③具有相同的原子数 ④具有相同的分子数
| A.①③ | B.②④ | C.①④ | D.③④ |
【知识点】 阿伏加德罗定律
| A.未冷却就转移、定容 | B.容量瓶中有少量蒸馏水 |
| C.用量筒量取浓硫酸时,俯视读数 | D.定容时俯视刻度线观察液面 |
| A.950mL 30.4g | B.950mL 47.5g | C.1000mL 50.0g | D.1000mL 32.0g |
| A.50 mL 0.2 mol·L-1的NaCl溶液 |
| B.100 mL 0.2 mol·L-1的NaCl溶液 |
| C.25 mL 0.1 mol·L-1的Na2SO4溶液 |
| D.50 mL 0.1 mol·L-1的NaNO3溶液 |
| A.0.75 mol·L-1 | B.0.5 mol·L-1 | C.1 mol·L-1 | D.0.25 mol·L-1 |
【知识点】 物质的量浓度
 的物质的量浓度为
的物质的量浓度为 | A.0.3mol/L | B.0.4mol/L |
| C.0.45mol/L | D.0.5mol/L |
【知识点】 物质的量浓度计算-溶液混合的有关计算解读
| A.0.03mol/L | B.0.3mol/L | C.0.05mol/L | D.0.04mol/L |
| A.食盐溶液静置会分层,上层比下层咸 |
| B.“冰水混合物”是一种分散系 |
| C.黄河入海口处三角洲的形成与胶体性质有关 |
| D.电泳现象说明胶体带电 |
| A.Fe(OH)3胶体有丁达尔效应是Fe(OH)3胶体区别于FeCl3溶液最本质的特征 |
| B.阳光穿透清晨的树林时形成的光柱,是胶体的丁达尔效应的体现 |
| C.鸡蛋清溶液分类上属于悬浊液 |
| D.向FeCl3溶液中加入NaOH溶液,会出现红褐色Fe(OH)3胶体 |
| A.胶体、溶液、浊液的分类依据是分散质微粒直径大小 |
| B.“卤水点豆腐”、“不同牌子的墨水不能混用”都与胶体的聚沉有关 |
| C.从颜色上无法区别氯化铁溶液和氢氧化铁胶体 |
| D.可以用丁达尔现象区别硫酸铜溶液和氢氧化铁胶体 |
| A.所含溶质为NaHSO4的溶液:加入K+、CO32-、NO3-、Na+ |
| B.滴加酚酞变红的溶液:加入SO42-、Cu2+、K+、Cl - |
| C.常温下,加入铁粉能生成H2的溶液:加入Na+、Ca2+、Cl -、HCO3 - |
| D.含有大量SO42-的溶液:加入K+、Cu2+、Cl-、NO3- |
【知识点】 限定条件下的离子共存解读
| A.K+、OH-、Na+ | B.K+、N03- 、Cu2+ |
| C.Ba2+、SO42-、Na+ | D.Ca2+、 CO32-、Na+ |
| A.KHSO4=K++H++SO42- | B.NaHCO3=Na++H++CO32- |
| C.Mg(NO3)2=Mg2++(NO3)22- | D.KClO3=K++Cl5﹣+3O2﹣ |
【知识点】 电解质
①NaOH ②BaSO4 ③Cu ④蔗糖 ⑤CO2
| A.①② | B.①②⑤ | C.③④ | D.①③⑤ |
【知识点】 电解质
| A.2NaOH+Cl2==NaCl+NaClO+H2O;Cl2+2OH- ==Cl-+ClO-+H2O |
| B.CaCO3+2HCl==CaCl2+CO2↑+H2O;CO32-+2H+ == CO2↑+H2O |
| C.Al2(SO4)3+6NH3•H2O==2Al(OH)3↓+3(NH4)2SO4; Al3++3OH-==Al(OH)3↓ |
| D.Ba(OH)2+H2SO4==BaSO4↓+2H2O;2H++2OH- ==2H2O |
【知识点】 离子反应的发生及书写 离子方程式的书写解读 离子方程式的正误判断解读
| A.液态HCl不导电,所以HCl是非电解质 |
| B.NH3的水溶液能导电,所以NH3是电解质 |
| C.铜、石墨均能导电,所以它们都是电解质 |
| D.蔗糖在水溶液中和熔融时都不导电,所以是非电解质 |
【知识点】 电解质、非电解质概念解读 非电解质、电解质物质类别判断解读
五、填空题 添加题型下试题
【知识点】 化学计量
 物质的量浓度是
物质的量浓度是(1)混合气体中二氧化碳与一氧化碳的物质的量CO2
(2)混合气体缓慢通过足量的氢氧化钠溶液后,剩余的气体是
【知识点】 化学计量
六、计算题 添加题型下试题
七、解答题 添加题型下试题
(1)98 %的浓硫酸的物质的量浓度为
(2)现有下列几种规格的量筒,应选用
①5 mL量筒 ②10 mL量筒 ③50 mL量筒 ④100 mL量筒
(3)实验需要以下步骤:①定容②量取③摇匀④洗涤⑤转移⑥冷却⑦计算⑧装瓶⑨稀释进行顺序为
A. ⑦②④⑨⑥③⑤①⑧ B.⑦②⑥⑨⑤④③①⑧
C.⑦②⑨⑥⑤④①③⑧ D. ⑦②⑨⑥④⑤③①⑧
(4)下列操作使所配溶液的物质的量浓度偏高的是
A.往容量瓶中转移溶液时有少量液体溅出
B.未洗涤稀释浓H2SO4的小烧杯
C.定容时俯视刻度线
D.洗净容量瓶未干燥即用来配制溶液
E.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
(1)据此,可判断出固体中肯定有
(2)写出②中反应的离子方程式
试卷分析
试卷题型(共 47题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、未知 | |||
| 1 | 0.85 | 物质的量浓度的计算 | 未知 |
| 19 | 0.85 | 物质分离、提纯的常见物理方法 萃取和分液 过滤 海带中碘的提取及检验 | 未知 |
| 二、单选题 | |||
| 2 | 0.65 | 物质的量浓度计算-溶液混合的有关计算 | |
| 3 | 0.65 | 硫酸根离子的检验 离子的检验 常见阴离子的检验 | |
| 4 | 0.85 | 离子的检验 无机物的检验 | |
| 5 | 0.85 | 硫酸根离子的检验 离子的检验 | |
| 6 | 0.65 | 仪器使用与实验安全 | |
| 7 | 0.85 | 仪器使用与实验安全 常用仪器及使用 化学实验基础操作 实验安全 | |
| 8 | 0.4 | 常见阴离子的检验 | |
| 9 | 0.85 | 物质分离、提纯的常见化学方法 物质分离、提纯综合应用 | |
| 10 | 0.85 | 化学实验基础操作 蒸发与结晶 | |
| 11 | 0.85 | 物质的分离、提纯 物质分离、提纯的常见物理方法 物质分离、提纯综合应用 蒸发与结晶 | |
| 12 | 0.85 | 物质分离、提纯综合应用 过滤 | |
| 13 | 0.65 | 常见气体的制备与收集 实验方案设计的基本要求 | |
| 14 | 0.65 | 电解质与非电解质 电解质的电离 电解质、非电解质概念 | |
| 15 | 0.65 | 离子反应的发生及书写 离子方程式的书写 | |
| 16 | 0.94 | 蒸馏与分馏 | |
| 17 | 0.65 | 物质的分离、提纯 物质分离、提纯的常见物理方法 物质分离、提纯的常见化学方法 | |
| 18 | 0.65 | 蒸发与结晶 过滤 | |
| 20 | 0.85 | 蒸发与结晶 蒸馏与分馏 萃取和分液 | |
| 21 | 0.4 | 物质的量及单位——摩尔 阿伏加德罗常数 摩尔质量 气体摩尔体积 | |
| 22 | 0.85 | 阿伏加德罗常数的求算 结合物质结构基础知识与NA相关推算 | |
| 23 | 0.94 | 阿伏加德罗定律 阿伏加德罗定律及其推论 阿伏加德罗定律的应用 | |
| 24 | 0.85 | 阿伏加德罗定律及其推论 阿伏加德罗定律的应用 | |
| 25 | 0.85 | 阿伏加德罗定律 | |
| 26 | 0.94 | 一定物质的量浓度的溶液的配制 配制一定物质的量浓度的溶液的步骤、操作 配制一定物质的量浓度的溶液实验的误差分析 | |
| 27 | 0.94 | 物质的量浓度的基础计算 配制一定物质的量浓度的溶液实验的仪器 | |
| 28 | 0.85 | 物质的量浓度概念、含义 某溶液与物质的量浓度相关的物理量的判断 物质的量浓度的计算 依据物质的量浓度公式的基础计算 | |
| 29 | 0.65 | 物质的量浓度 | |
| 30 | 0.85 | 物质的量浓度计算-溶液混合的有关计算 | |
| 31 | 0.94 | 物质的量浓度的计算 物质的量浓度的基础计算 物质的量浓度与溶液稀释的计算 | |
| 32 | 0.94 | 分散系概念及其分类 胶体的性质和应用 | |
| 33 | 0.85 | 分散系概念及其分类 胶体的定义及分类 胶体的性质和应用 胶体的制备 | |
| 34 | 0.85 | 分散系概念及其分类 胶体的定义及分类 胶体的性质和应用 | |
| 35 | 0.65 | 限定条件下的离子共存 | |
| 36 | 0.4 | 离子反应概念 离子反应的发生条件 限定条件下的离子共存 | |
| 37 | 0.64 | 电解质 | |
| 38 | 0.64 | 电解质 | |
| 39 | 0.65 | 离子反应的发生及书写 离子方程式的书写 离子方程式的正误判断 | |
| 40 | 0.85 | 电解质、非电解质概念 非电解质、电解质物质类别判断 | |
| 三、填空题 | |||
| 41 | 0.64 | 化学计量 | |
| 42 | 0.85 | 物质的量浓度 物质的量浓度的计算 物质的量浓度计算-溶液稀释的有关计算 | |
| 43 | 0.85 | 根据n=N/NA进行相关计算 结合物质结构基础知识与NA相关推算 以N=m·NA/M为中心的有关基本粒子的推算 | |
| 44 | 0.64 | 化学计量 | |
| 四、计算题 | |||
| 45 | 0.85 | 物质的量有关计算 根据n=m/M进行相关计算 化学方程式计算中物质的量的运用 | |
| 五、解答题 | |||
| 46 | 0.65 | 配制一定物质的量浓度的溶液的步骤、操作 配制一定物质的量浓度的溶液实验的误差分析 配制一定物质的量浓度的溶液实验的仪器 配制一定物质的量浓度溶液的综合考查 | 实验探究题 |
| 47 | 0.65 | 离子反应在化合物组成的分析、鉴定的应用 硫酸根离子的检验 离子的检验 无机物的检验 | 无机推断题 |