河北省高阳中学2017-2018学年高一1月月考化学试题
河北
高一
阶段练习
2018-11-15
357次
整体难度:
适中
考查范围:
认识化学科学、物质结构与性质、化学实验基础、常见无机物及其应用
一、单选题 添加题型下试题
| A.氧化物、化合物 | B.化合物、盐 | C.溶液、 胶体 | D.溶液、 分散系 |
| A.133 | B.78 | C.55 | D.23 |
| A.CH4的摩尔质量为16g mol-1 |
| B.从1L 2mol/L的H2SO4溶液中取出5mL,则所取溶液中氢离子的浓度为4mol/L |
| C.加入稀盐酸产生能使澄清石灰水变浑浊的无色气体,说明原溶液一定含有CO32- |
| D.可用焰色反应可区分KCl和NaCl |
【知识点】 化学计量
| A.所含分子数目相同 |
| B.所含氢原子的物质的量之比为3:4 |
| C.质量之比为16:17 |
| D.密度之比为17:16 |
| A.溶解 过滤 蒸发结晶 | B.加热 溶解 过滤 |
| C.溶解 过滤 蒸馏 | D.溶解 过滤 分液 |
【知识点】 化学实验基础
二、未知 添加题型下试题
三、单选题 添加题型下试题
四、未知 添加题型下试题
五、单选题 添加题型下试题
| A.称取12.5 g CuSO 4 •5H 2 O,灼烧去结晶水后,再配成500 mL溶液 |
| B.称取12 g胆矾配成480 mL溶液 |
| C.称取12.5 g胆矾配成500 mL溶液 |
| D.称取8 g CuSO 4 溶于500 mL水中 |
【知识点】 配制一定物质的量浓度的溶液的步骤、操作解读
| A.0.75 mol·L-1 | B.0.5 mol·L-1 | C.1 mol·L-1 | D.0.25 mol·L-1 |
【知识点】 物质的量浓度
| A.用托盘天平称取3.23g NaCl固体 |
| B.用10mL量筒量取7.50mL稀盐酸 |
| C.分液以后下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 |
| D.稀释浓硫酸时,把浓硫酸沿器壁慢慢注入水里,并不断搅拌 |
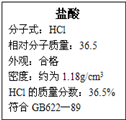
| A.3 mol/L | B.8.4 mol/L | C.11.8 mol/L | D.0.5 mol/L |
①标准状况下,2.24 L水中含有0.1 NA个水分子
②常温常压下,32g SO2 含有的分子数约为3.01×1023
③2 mol NaOH的摩尔质量为80g/mol
④H2的气体摩尔体积约为22.4L/mol
⑤标况下,22.4L由N2和N2O组成的混合气体中,所含有的氮原子的物质的量为2mol
⑥2mol/L的CaCl2溶液中Cl-的数目为4NA
⑦常温常压下,1mol氦气含有的原子数为NA
⑧11.2 L氯气中含有 NA个氯原子
| A.①③④⑥⑧ | B.①④⑤⑥⑧ | C.①②④⑥⑧ | D.②③④⑤⑦ |
【知识点】 化学计量
| A.固体氯化钠不导电,所以氯化钠不是电解质 |
| B.氯化氢水溶液能导电,所以氯化氢是电解质 |
| C.SO2溶于水能导电,所以SO2是电解质 |
| D.氨水能导电,所以氨水是电解质 |
【知识点】 非电解质、电解质物质类别判断解读
| A.0.5mol/L | B.0.6mol/L | C.1mol/L | D.2mol/L |
【知识点】 物质的量浓度计算-溶液混合的有关计算解读
A.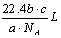 | B.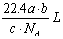 | C.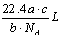 | D.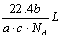 |
【知识点】 阿伏加德罗定律
| A.甲的分子数比乙的分子数多 | B.甲的物质的量比乙的物质的量少 |
| C.甲的摩尔体积比乙的摩尔体积小 | D.甲的相对分子质量比乙的相对分子质量小 |
【知识点】 阿伏加德罗定律
 Se和
Se和 Se的说法正确的是
Se的说法正确的是A. Se 和 Se 和 Se含有的电子数分别为78和80 Se含有的电子数分别为78和80 |
B. Se和 Se和 Se互为同位素 Se互为同位素 |
C. Se和 Se和 Se 分别含有44和46个质子 Se 分别含有44和46个质子 |
D. Se和 Se和 Se都含有34个中子 Se都含有34个中子 |
【知识点】 元素周期表 元素周期律
| A.BaCl2 | B.HCl | C.NaOH | D.Ba(OH)2 |
| 纯净物 | 混合物 | 电解质 | 非电解质 | |
| A | 冰水混合物 | 明矾 | 液态 | 蔗糖 |
| B | CaO | 海水 | 铜 | 乙醇 |
| C | 胆矾 | 镁合金 | AgCl |  |
| D | 氢氧化钠 | 空气 |  溶液 溶液 | 食醋 |
| A.A | B.B | C.C | D.D |
【知识点】 无机物质的分类 非电解质、电解质物质类别判断解读
| A.蒸发 | B.萃取 | C.过滤 | D.蒸馏 |
| A.在任意条件下,若两种分子保持原组成,则其相对分子质量之比为m:n |
| B.相同状况下,同体积的气体A与B的质量之比为m:n |
| C.同质量的A、B在非标准状况下,其分子数之比为n:m |
| D.25℃、1.25×105Pa时,两气体的密度之比为n:m |
A. mol·L-1 mol·L-1 | B. mol·L-1 mol·L-1 |
C. mol·L-1 mol·L-1 | D. mol·L-1 mol·L-1 |
【知识点】 物质的量浓度的计算 依据物质的量浓度公式的基础计算解读
| A.体积:④<①<②<③ |
| B.密度:①<④<③<② |
| C.质量:④<①<③<② |
| D.氢原子数:②<④<③<① |
| A.1:2:3 | B.1:1:1 | C.2:3:6 | D.6:3:2 |
【知识点】 物质的量浓度的计算
| A.质子数 | B.密度 | C.质量 | D.原子数 |
【知识点】 阿伏加德罗定律的应用解读 原子的基本构成解读
六、解答题 添加题型下试题
(1)将混合物溶于水,得无色澄清溶液;
(2)向此溶液中滴加BaCl2溶液,有白色沉淀产生;
(3)过滤后,在白色沉淀中加足量稀HNO3,沉淀溶解。
此推断:混合物中肯定有
【知识点】 离子反应在化合物组成的分析、鉴定的应用解读 离子的检验 无机物的检验

(1)从氯化钾溶液中得到氯化钾固体,选择装置
(2)从油水混合物中分离出植物油,选择装置
(3)装置A中①的名称是
(4)海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如下流程的实验:




 ―→
―→
粗盐中含Ca2+、Mg2+、Fe3+、
 等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:
等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:①加入过量的Na2CO3溶液 ②加入过量的BaCl2溶液 ③加入过量的NaOH溶液 ④调节溶液的pH等于7 ⑤溶解 ⑥过滤 ⑦蒸发
正确的操作顺序是
a.⑤②③①⑥④⑦ b.⑤①②③⑥④⑦
c.⑤②①③④⑥⑦ d.⑤③②①⑥④⑦
【知识点】 物质分离、提纯的常见物理方法
(1)需要使用的主要仪器有量筒、烧杯、玻璃棒、
(2)其操作步骤可分解为以下几步:
A.用量筒量取
B.用适量蒸馏水分三次洗涤烧杯和玻璃棒,将每次的洗液都移入容量瓶里。
C.将稀释后的硫酸小心地用玻璃棒引流容量瓶里。
D.检查容量瓶是否漏水。
E.将蒸馏水直接加入容量瓶,至液面接近刻度线1-2cm处。
F.盖紧瓶塞,反复颠倒振荡,摇匀溶液。
G.用胶头滴管向容量瓶里逐滴加入蒸馏水,到液面最低点恰好与刻线相切。
请据此填写:
①完成上述步骤中的空白处。
②补充完成正确的操作顺序(用字母填写):
( D )→( A )→( )→( )→( )→( )→( F )。
③将浓硫酸在烧杯中稀释后移入容量瓶时,必须
(3)试分析下列操作对所配溶液的浓度有何影响:
①量取浓硫酸时眼睛俯视刻度线,会导致所配溶液浓度会
②定容时,眼睛俯视刻度线,所配溶液浓度会
③定容后,加盖倒转摇匀后,发现溶面低于刻度线,又滴加蒸馏水至刻度。所配溶液浓度会
试卷分析
试卷题型(共 30题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.4 | 分类方法的应用 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系 胶体 | |
| 2 | 0.65 | 原子中相关数值及其之间的相互关系 元素、核素、同位素 | |
| 3 | 0.94 | 化学计量 | |
| 4 | 0.94 | 气体摩尔体积 阿伏加德罗定律 | |
| 5 | 0.94 | 化学实验基础 | |
| 7 | 0.65 | 物质的量浓度 物质的量浓度的计算 | |
| 9 | 0.65 | 配制一定物质的量浓度的溶液的步骤、操作 | |
| 10 | 0.65 | 物质的量浓度 | |
| 11 | 0.4 | 常用仪器及使用 配制一定物质的量浓度的溶液的步骤、操作 萃取和分液 | |
| 12 | 0.65 | 物质的量浓度计算-溶液配制有关计算 一定物质的量浓度的溶液的配制 | |
| 13 | 0.15 | 化学计量 | |
| 14 | 0.65 | 离子共存 离子反应的实际应用 离子反应在混合物分离、除杂中的应用 离子反应在化合物组成的分析、鉴定的应用 | |
| 15 | 0.65 | 非电解质、电解质物质类别判断 | |
| 16 | 0.94 | 物质的量浓度计算-溶液混合的有关计算 | |
| 17 | 0.94 | 阿伏加德罗定律 | |
| 18 | 0.85 | 阿伏加德罗定律 | |
| 19 | 0.64 | 元素周期表 元素周期律 | |
| 20 | 0.65 | 无机物的检验 物质检验和鉴别的基本方法选择及应用 物质检验和鉴别的实验方案设计 | |
| 21 | 0.85 | 无机物质的分类 非电解质、电解质物质类别判断 | |
| 22 | 0.4 | 常用仪器及使用 蒸发与结晶 蒸馏与分馏 过滤 | |
| 23 | 0.85 | 阿伏加德罗定律的应用 化学方程式计算中物质的量的运用 | |
| 24 | 0.65 | 物质的量浓度的计算 依据物质的量浓度公式的基础计算 | |
| 25 | 0.65 | 阿伏加德罗定律及其推论 阿伏加德罗定律的应用 根据n=N/NA的相关计算 根据N=m·NA/M的相关推算 | |
| 26 | 0.65 | 物质的量浓度的计算 | |
| 27 | 0.65 | 阿伏加德罗定律的应用 原子的基本构成 | |
| 二、未知 | |||
| 6 | 0.85 | 铵根离子的检验 硫酸根离子的检验 离子的检验 常见阳离子的检验 | 未知 |
| 8 | 0.65 | 摩尔质量 物质的量有关计算 | 未知 |
| 三、解答题 | |||
| 28 | 0.65 | 离子反应在化合物组成的分析、鉴定的应用 离子的检验 无机物的检验 | 实验探究题 |
| 29 | 0.65 | 物质分离、提纯的常见物理方法 | 实验探究题 |
| 30 | 0.65 | 配制一定物质的量浓度的溶液的步骤、操作 配制一定物质的量浓度的溶液实验的误差分析 配制一定物质的量浓度的溶液实验的仪器 配制一定物质的量浓度溶液的综合考查 | 实验探究题 |



 、OH-三种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来。下列实验操作的操作顺序中,正确的是
、OH-三种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来。下列实验操作的操作顺序中,正确的是

