2014-2015内蒙古赤峰市宁城县高一上学期期末考试化学试卷
内蒙古
高一
期末
2017-07-26
511次
整体难度:
适中
考查范围:
认识化学科学、化学实验基础、常见无机物及其应用、物质结构与性质
一、单选题 添加题型下试题
| A.光是一种胶体 |
| B.雾是一种胶体 |
| C.薄雾中的小水滴颗粒大小约为10-9 m~10-7 m |
| D.发生丁达尔效应 |
A.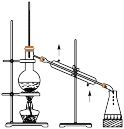 | B. | C. | D. |
| A.分别放在炒锅中加热,观察是否有残留物 |
| B.分别用干净铁丝蘸取样品在煤气炉的火焰上灼烧,观察火焰颜色 |
| C.将样品溶解,分别加入澄清石灰水,观察是否有白色沉淀 |
| D.在水杯中各盛相同质量的样品,分别加入等体积的白醋,观察反应的剧烈程度 |
【知识点】 碳酸钠与碳酸氢钠鉴别的实验解读
| A.质子数 | B.密度 | C.质量 | D.原子数 |
【知识点】 阿伏加德罗定律的应用解读 原子的基本构成解读
 ,将粗盐溶于水,然后进行下列五项操作:①过滤,②加过量的NaOH溶液,③加适量盐酸,④加过量Na2CO3溶液,⑤加过量BaCl2溶液。正确的操作顺序是
,将粗盐溶于水,然后进行下列五项操作:①过滤,②加过量的NaOH溶液,③加适量盐酸,④加过量Na2CO3溶液,⑤加过量BaCl2溶液。正确的操作顺序是| A.①④②⑤③ | B.④①②⑤③ | C.②⑤④③① | D.⑤②④①③ |
【知识点】 卤素在自然界的存在解读 物质分离、提纯的常见化学方法解读
| A.硫元素的质量比为5:4 | B.分子数之比为1:1 |
| C.原子总数之比为4:3 | D.质量之比为1:1 |
①SiO2
 Na2SiO3 ②CuSO4
Na2SiO3 ②CuSO4 CuCl2 ③SiO2
CuCl2 ③SiO2 H2SiO3④CuO
H2SiO3④CuO Cu(OH)2
Cu(OH)2⑤Na2O2
 Na2SO4
Na2SO4| A.①② | B.③④ |
| C.②③④ | D.②③④⑤ |
【知识点】 物质的转化
| A.H+、K+、Fe2+、NO3- | B.OH-、Cl-、Na+、NH4+ |
| C.Cu2+、NO3-、OH-、Cl- | D.Mg2+、K+、Cl-、NO3- |
【知识点】 离子共存
| A.向氯化亚铁溶液中通入氯气:Fe2++Cl2=Fe3++2Cl- |
| B.将氯气通入冷的氢氧化钠溶液中:Cl2+2OH-=Cl-+ClO-+H2O |
| C.铝片与氢氧化钠溶液反应:Al+2OH-=AlO2-+H2↑ |
| D.金属铝溶于盐酸中:Al+2H+=Al3++H2↑ |
【知识点】 离子反应的发生及书写 离子方程式的书写解读 离子方程式的正误判断解读
| A.实验②证明Fe2+既有氧化性又有还原性 |
| B.上述实验中,有一个氧化还原反应 |
| C.实验①生成的气体不能使湿润的淀粉KI试纸变蓝 |
| D.上述实验证明氧化性:MnO4->Cl2>Fe3+ |
【知识点】 氧化还原反应基本概念 氧化性、还原性强弱的比较解读
| A.2.3 g钠由原子变为离子时失去的电子数为NA |
| B.在常温常压下,1 mol氩气含有的原子数为2NA |
| C.标准状况下2.24 L氨气所含电子总数为0.1NA |
| D.在常温常压下,62 g Na2O中含有O2-离子数为NA |
【知识点】 化学计量
 2K2S+K2SO3+3H2O,则反应中氧化剂和还原剂的质量比是
2K2S+K2SO3+3H2O,则反应中氧化剂和还原剂的质量比是 | A.3∶1 | B.1∶3 | C.2∶1 | D.1∶2 |
| A.①⑤④③ | B.②③④③ | C.②③⑤③ | D.①⑤③ |
| A.0.1mol | B.0.3mol | C.0.5mol | D.0.15mol |
【知识点】 物质的量有关计算

| A.1.75 mol∙L−1 | B.3.50 mol∙L−1 | C.0.85 mol∙L−1 | D.无法确定 |
 6NH3+3CO2+C3H6N6,对C3H6N6说法正确的是
6NH3+3CO2+C3H6N6,对C3H6N6说法正确的是| A.摩尔质量为126 |
| B.式量为126g·mol-1 |
| C.每个C3H6N6分子含3个N2分子 |
| D.0.1molC3H6N6含碳原子数为1.806×1023 |
【知识点】 化学计量
二、填空题 添加题型下试题
(1)能导电的是(填字母,下同)
(2)属于电解质的是
(3)属于非电解质的是
【知识点】 电解质
(2)将新制的氯水分成三份:
①向其中第一份中滴入
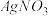 溶液,离子方程式是
溶液,离子方程式是②向第二份中滴入
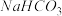 溶液,离子方程式是
溶液,离子方程式是③向第三份中滴入紫色石蕊试液,现象是先
(3)工业上制取漂白粉的化学方程式是
 反应,生成具有漂白性的物质,其化学方程式是
反应,生成具有漂白性的物质,其化学方程式是(1)取样品,加热至高温,产生一种能使澄清石灰水变浑浊的无色气体。
(2)往冷却后的固体残渣中加入足量的稀盐酸,固体残渣全部溶解,同时产生一种可燃性气体。根据以上实验推断:该固体一定含有
【知识点】 化学实验基础
三、解答题 添加题型下试题

(1)写出该反应的化学方程式
(2)玻璃管中石棉绒的作用是
(3)圆底烧瓶中盛装的水,该装置受热后的主要作用是
(4)该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中固体物质的成分是
(5)该同学按上述实验方案进行了实验,结果溶液未变红色,原因是
(6)该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出与上述现象相关的反应的化学方程式

(7)一段时间后,该同学发现(4)中未变红的溶液变成红色,说明Fe2+ 具有
【知识点】 常见无机物及其应用
四、计算题 添加题型下试题
(1)混合液中Fe3+的物质的量浓度
(2)混合液中SO
 的物质的量浓度
的物质的量浓度(3)向溶液中加入足量铁粉,经足够长时间后,铁粉有剩余,求此时溶液中FeSO4的物质的量浓度
试卷分析
试卷题型(共 21题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 分散系概念及其分类 | |
| 2 | 0.94 | 胶体的性质和应用 配制一定物质的量浓度的溶液实验的仪器 物质分离、提纯的常见物理方法 | |
| 3 | 0.85 | 碳酸钠与碳酸氢钠鉴别的实验 | |
| 4 | 0.65 | 阿伏加德罗定律的应用 原子的基本构成 | |
| 5 | 0.65 | 卤素在自然界的存在 物质分离、提纯的常见化学方法 | |
| 6 | 0.65 | 物质的量有关计算 根据n=m/M进行相关计算 以N=m·NA/M为中心的有关基本粒子的推算 | |
| 7 | 0.85 | 物质的转化 | |
| 8 | 0.64 | 离子共存 | |
| 9 | 0.85 | 离子反应的发生及书写 离子方程式的书写 离子方程式的正误判断 | |
| 10 | 0.65 | 氧化还原反应基本概念 氧化性、还原性强弱的比较 | |
| 11 | 0.64 | 化学计量 | |
| 12 | 0.65 | 氧化还原反应有关计算 与氧化剂、还原剂有关的计算 基于氧化还原反应守恒规律的计算 | |
| 13 | 0.65 | 铝与强碱溶液反应 偏铝酸钠与二氧化碳的反应 物质分离、提纯综合应用 | |
| 14 | 0.65 | 物质的量有关计算 | |
| 15 | 0.85 | 化学方程式计算中物质的量的运用 氢氧化铝与强碱反应 铝盐与强碱溶液反应 氢氧化铁的制备 | |
| 16 | 0.64 | 化学计量 | |
| 二、填空题 | |||
| 17 | 0.64 | 电解质 | |
| 18 | 0.64 | 化学实验基础 卤素及其化合物 | |
| 19 | 0.4 | 化学实验基础 | |
| 三、解答题 | |||
| 20 | 0.64 | 常见无机物及其应用 | 实验探究题 |
| 四、计算题 | |||
| 21 | 0.85 | 化学方程式计算中物质的量的运用 物质的量浓度计算-溶液稀释的有关计算 物质的量浓度计算-溶液混合的有关计算 | |



