浙江省诸暨市第二高级中学2020-2021学年高二下学期期中考试化学试题
浙江
高二
期中
2021-08-26
642次
整体难度:
适中
考查范围:
有机化学基础、化学实验基础、常见无机物及其应用、化学反应原理、认识化学科学
一、单选题 添加题型下试题
| A.日常生活中不能用粥汤检验碘盐中是否含有KIO3 |
| B.将铁屑、浓溴水、苯混合可制得溴苯 |
| C.用蒸馏方法除去乙醇中的水 |
| D.洗涤沉淀时,应用玻璃棒轻轻搅拌,使得沉淀表面上的杂质溶于水中 |
| A.纸层析法适用于分离和检验化学性质十分相近的分子或离子 |
| B.用纸层析法可以检验氯化铁溶液中是否混有少量氯化铜 |
| C.纸层析法是利用试样中各种离子随展开剂在滤纸上展开的速率不同而形成不同位置的色斑 |
| D.为了看到色斑,只有有色离子的检验才可以用纸层析法 |
| A.NaNO3和NaCl | B.CuO和木炭粉 |
| C.MnO2和KCl | D.BaSO4和AgCl |
| A.油污 | B.铁锈 | C.锌 | D.硫化物 |
| A.往新配制的可溶性淀粉溶液中滴加碘水,溶液显蓝色,用CCl4不能从中萃取出碘 |
| B.当锌完全溶解后,铁与酸反应产生氢气的速率会显著减慢,此现象可作为判断镀锌铁皮中锌镀层是否完全被反应掉的依据 |
| C.镀锌铁皮发生电化学腐蚀时,锌发生氧化反应 |
| D.食醋的总酸含量是指食醋中醋酸的总物质的量浓度 |
【知识点】 金属的电化学腐蚀与防护 乙酸具有酸的通性解读
| A.在“镀锌铁皮的镀层厚度的测定”实验中,将镀锌铁皮放入稀硫酸,待产生氢气的速率突然减小,可以判断锌镀层已反应完全。 |
| B.在“火柴头中氯元素的检验”实验中,摘下几根未燃过的火柴头,将其浸于水中,稍后取少量溶液于试管中,滴加硝酸银溶液和稀硝酸后,即可判断氯元素的存在。 |
| C.在“硫酸亚铁铵的制备”实验中,为了得到硫酸亚铁铵晶体,应小火加热蒸发皿,直到有大量晶体析出时停止加热。 |
| D.受强酸或强碱腐蚀致伤时,应先用大量水冲洗,再用2%醋酸溶液或饱和硼酸溶液洗,最后用水冲洗,并视情况作进一步处理 |
【知识点】 氯离子的检验解读 仪器使用与实验安全 化学实验方案的设计与评价
A.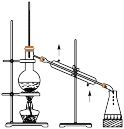 | B. | C. | D. |

| A.分子数 | B.质量 | C.颜色 | D.平均相对分子质量 |
【知识点】 温度对化学平衡移动的影响解读
a.将0.2mol·L-1A溶液和0.2mol·L-1B溶液各20mL混合
b.将0.5mol·L-1A溶液和0.5mol·L-1B溶液各50mL混合
c.将1mol·L-1A溶液和1mol·L-1B溶液各10mL混合,同时倒入30mL蒸馏水
d.将1mol·L-1A溶液20mL和1.2mol·L-1B溶液60mL混合
反应开始时,反应速率由大到小的顺序是
| A.d>b>c>a | B.b>d>a>c |
| C.d>c>b>a | D.b>c>d>a |
【知识点】 浓度对化学反应速率的影响解读
| A.1:1 | B.2:1 | C.3:1 | D.1:3 |
| A.溶液呈中性,可选用甲基橙或酚酞作指示剂 |
| B.溶液呈中性,只能选用石蕊作指示剂 |
| C.溶液呈碱性,可选用甲基橙或酚酞作指示剂 |
| D.溶液呈碱性,只能选用酚酞作指示剂 |
【知识点】 酸碱中和滴定指示剂选择解读


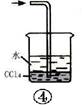
| A.装置①可用于由工业酒精制取无水酒精 |
| B.装置②可用于干燥、收集氨气,并吸收多余的氨气 |
| C.装置③可用于排空气法收集NO气体 |
| D.装置④中下层物质若为四氯化碳,则可用于吸收氯化氢 |
【知识点】 一氧化氮的化学性质解读 物质分离、提纯的常见物理方法
A.硫酸铝溶液中加入过量的氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH |
B.铁片放入过量的稀硝酸中:3Fe+8H++2NO =3Fe2++2NO2↑+4H2O =3Fe2++2NO2↑+4H2O |
C.将铝片放入过量NaOH溶液中:2Al+2OH-+6H2O=2Al(OH) +3H2↑ +3H2↑ |
D.四羟基合铝酸盐与过量盐酸反应:Al(OH) +4H+=Al3++4H2O +4H+=Al3++4H2O |
【知识点】 离子方程式的正误判断解读

| A.它是苯酚的同系物 |
| B.1mol该物质能与溴水反应消耗2molBr2,发生取代反应 |
| C.1mol该有机物能与足量金属钠反应生成0.5 mol H2 |
| D.1mol该有机物能与2 mol NaOH反应 |
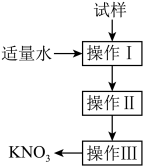
| A.操作Ⅰ是过滤,将固体分离除去 | B.操作Ⅱ是加热浓缩、趁热过滤,除去杂质氯化钠 |
| C.操作Ⅲ是过滤、洗涤,将硝酸钾晶体从溶液中分离出来 | D.操作Ⅰ~Ⅲ总共需两次过滤 |
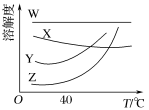
| A.W | B.X | C.Y | D.Z |
【知识点】 有机物重结晶解读 物质分离、提纯的常见物理方法

| A.大于10.00 mL | B.小于10.00 mL |
| C.等于10.00 mL | D.等于11.00 mL |
| A.用量筒量取一定体积液体时,俯视读出的读数 |
| B.用标准盐酸滴定未知浓度的NaOH溶液,酸式滴定管未用标准盐酸润洗,所测出的碱液的浓度值 |
| C.同一滴定实验,一般做三次,取三次实验的平均值进行计算,但某同学只做了一次 |
| D.达到滴定终点时,俯视读数标准液滴定未知物质的量浓度的HCl溶液 |
【知识点】 酸碱中和滴定的误差分析解读
| A.V1>V2 | B.V1<V2 | C.V1=V2 | D.V1≤V2 |
 和1,8—二硝基萘
和1,8—二硝基萘 的混合物。后者可溶于质量分数大于98%的硫酸,而前者不能。利用这一性质可以将这两种异构体分离。将上述硝化产物加入适量的98%硫酸,充分搅拌,用耐酸漏斗过滤,欲从滤液中得到固体1,8—二硝基萘,应采用的方法是
的混合物。后者可溶于质量分数大于98%的硫酸,而前者不能。利用这一性质可以将这两种异构体分离。将上述硝化产物加入适量的98%硫酸,充分搅拌,用耐酸漏斗过滤,欲从滤液中得到固体1,8—二硝基萘,应采用的方法是| A.蒸发浓缩结晶 | B.向滤液中加水后过滤 |
| C.用碳酸钠溶液处理滤液 | D.将滤液缓缓加入水中 |
 和
和 ,②
,② 和
和 ,③
,③ 和
和 。将3支试管均倒置于盛水的水槽中,充分反应后,试管中剩余气体的体积分别为
。将3支试管均倒置于盛水的水槽中,充分反应后,试管中剩余气体的体积分别为 、
、 、
、 ,则下列的关系正确的是
,则下列的关系正确的是A.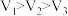 | B.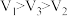 |
C.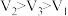 | D.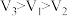 |
【知识点】 氮氧化物溶解于水的相关计算解读 二氧化氮与水反应解读
| A.0mol | B.0.67mol | C.1mol | D.1.33 mol |
 的物质的量浓度是(单位:mol·L—1)
的物质的量浓度是(单位:mol·L—1) A.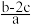 | B.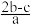 | C. | D.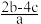 |
【知识点】 物质的量浓度的计算 化学方程式中物质的量的运用解读
 、Fe2+、Al3+、CO
、Fe2+、Al3+、CO 、SO
、SO 、SO
、SO 、Cl-中的若干种,某同学为了确认其成分,取X溶液进行连续实验,实验过程及产物如图:
、Cl-中的若干种,某同学为了确认其成分,取X溶液进行连续实验,实验过程及产物如图: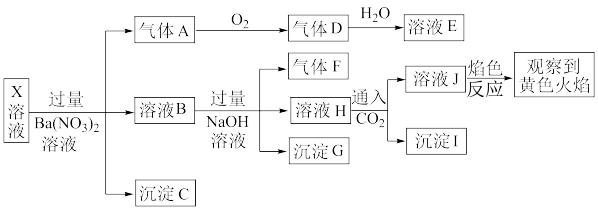
下列结论正确的是( )
A.X中肯定存在Na+、Fe2+、Al3+、NH 、SO 、SO |
| B.X中不能确定的离子是Al3+、Na+、K+和Cl- |
| C.沉淀C一定是BaSO4、沉淀G一定是Fe(OH)3、沉淀I一定是Al(OH)3 |
| D.气体F经催化氧化可直接生成气体D |
【知识点】 离子反应在化合物组成的分析、鉴定的应用解读
| A.混合气体中含二氧化氮1.12L |
| B.消耗氧气的体积为1.68L |
| C.此反应过程中转移的电子为0.3mol |
| D.参加反应的硝酸是0.4mol |
二、填空题 添加题型下试题
(1)除去氯化钠溶液中的石灰石:
(2)除去碘中混有的碘化钠固体:
(3)除去乙醇中溶解的少量食盐:
(4)除去Fe(OH)3胶体中混有的Cl-:
三、解答题 添加题型下试题

已知:①反应方程式为
 +(CH3CO)2O
+(CH3CO)2O
 +CH3COOH
+CH3COOH②抽滤的实验装置如图所示。

请回答有关问题:
(1)仪器A的名称是
(2)在步骤②中,若冷却结晶时未出现结晶,可以
(3)实验时,当仪器B中液面高度快达到支管口位置时,应进行的操作是
(4)仪器C中两玻璃导管的位置是否正确?答:
(5)在步骤④中,用饱和NaHCO3溶液可以将阿司匹林和副产物等分离,其化学原理是
(6)步骤⑤中,搅拌使反应充分进行至
(7)若实验得到2.70g纯净的阿司匹林,则产品的产率为
【知识点】 物质分离、提纯综合应用解读 常见有机物的制备解读
Ⅰ.摩擦剂中氢氧化铝的定性检验
取适量牙膏样品,加水充足搅拌、过滤。
(1)往滤渣中加入过量 NaOH溶液,过滤。氢氧化铝与NaOH溶液反应的离子方程式是
(2)往(1)所得滤液中先通入过量二氧化碳,再加入过量稀盐酸。观察的现象是
Ⅱ.牙膏样品中碳酸钙的定量测定
利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO
 沉淀质量,以确定碳酸钙的质量分数。
沉淀质量,以确定碳酸钙的质量分数。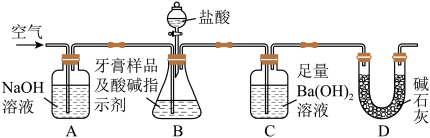
依据实验过程回答下列问题:
(3)实验过程中需持续缓缓通入空气。其作用除了可搅拌B、C中的反应物外,还有:
(4)C中反应生成BaCO3的化学方程式是
(5)下列各项措施中,不能提高测定准确度的是
a.在加入盐酸之前,应排净装置内的CO2气体
b.滴加盐酸不宜过快
c.在A-B之间增添盛有浓硫酸的洗气装置
d.在B-C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(6)实验中准确称取8.00 g样品三份,进行三次测定,测得BaCO3平均质量为3.94 g。则样品中碳酸钙的质量分数为
(7)有人认为不必测定C中生成的BaCO3质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,原因是
【知识点】 探究物质组成或测量物质的含量解读 物质性质的探究解读
四、填空题 添加题型下试题
 NaNO2+
NaNO2+ KI+
KI+ →
→ NO↑+
NO↑+ I2+
I2+ K2SO4+
K2SO4+ Na2SO4+
Na2SO4+
(1)请完成并配平该化学方程式
(2)在上述反应中,若要生成25.4gI2,则电子转移了
(3)用上述反应来处理NaNO2并不是最佳方法,其原因是
(4)亚硝酸钠可以与酸反应生成亚硝酸,亚硝酸是不稳定的弱酸,它只存在于冷的稀溶液中,易发生分解反应:3HNO2=2NO↑+HNO3+H2O。请从浓醋酸、氨水、纯碱、稀盐酸、碘化钾溶液、淀粉溶液中选择适当的物质,设计两个简单的实验鉴别NaNO2和NaCl。
方案1:所加试剂是
方案2:所加试剂是
【知识点】 氧化还原反应有关计算 氧化还原反应方程式的配平解读 电子转移计算
五、解答题 添加题型下试题
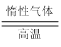 Li2FeSiO4+Li2SO4+SiO2
Li2FeSiO4+Li2SO4+SiO2某学习小组按如下实验流程制备Li2FeSiO4并测定所得产品中Li2FeSiO4的含量。
实验(一)制备流程:
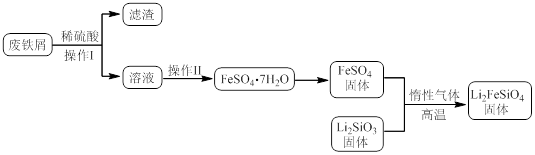
实验(二) Li2FeSiO4含量测定:
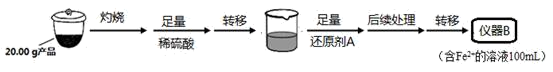
从仪器B中取20.00 mL溶液至锥形瓶中,另取0.2000 mol·Lˉ1的酸性KMnO4标准溶液装入仪器C中,用氧化还原滴定法测定Fe2+含量。相关反应为:MnO4- +5Fe2++8H+=Mn2++5Fe3++4H2O,杂质不与酸性KMnO4标准溶液反应。经4次滴定,每次消耗KMnO4溶液的体积如下:
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗KMnO4溶液体积 | 20.00 mL | 19.98mL | 21.38mL | 20.02mL |
(2)制备Li2FeSiO4时必须在惰性气体氛围中进行,其原因是
(3)操作Ⅱ的步骤
(4)还原剂A可用SO2,写出该反应的离子方程式
(5)滴定终点时现象为
六、填空题 添加题型下试题

请回答:
(1)H2SO4溶液的物质的量浓度为
(2)a=2,用于沉淀铁离子,消耗NaOH的体积是
试卷分析
试卷题型(共 31题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 苯的取代反应 化学实验基础操作 过滤 | |
| 2 | 0.65 | 纸上层析 | |
| 3 | 0.94 | 物质的分离、提纯 蒸发与结晶 过滤 | |
| 4 | 0.65 | 铁与非氧化性酸的反应 几种铁的氧化物的化学性质 物质分离、提纯综合应用 | |
| 5 | 0.65 | 金属的电化学腐蚀与防护 乙酸具有酸的通性 | |
| 6 | 0.65 | 氯离子的检验 仪器使用与实验安全 化学实验方案的设计与评价 | |
| 7 | 0.94 | 胶体的性质和应用 配制一定物质的量浓度的溶液实验的仪器 物质分离、提纯的常见物理方法 | |
| 8 | 0.65 | 温度对化学平衡移动的影响 | |
| 9 | 0.65 | 浓度对化学反应速率的影响 | |
| 10 | 0.94 | 物质的量有关计算 化学方程式中物质的量的运用 铝与酸溶液反应 铝与强碱溶液反应 | |
| 11 | 0.65 | 酸碱中和滴定指示剂选择 | |
| 12 | 0.65 | 一氧化氮的化学性质 物质分离、提纯的常见物理方法 | |
| 13 | 0.65 | 离子方程式的正误判断 | |
| 14 | 0.4 | 有机官能团的性质及结构 同系物的判断 醇与活泼金属反应的相关计算 含有酚羟基的物质性质的推断 | |
| 15 | 0.65 | 物质的分离、提纯 物质分离、提纯的常见物理方法 蒸发与结晶 过滤 | |
| 16 | 0.85 | 有机物重结晶 物质分离、提纯的常见物理方法 | |
| 17 | 0.85 | 酸碱中和滴定实验基本操作及步骤 酸碱中和滴定实验相关仪器 酸碱中和滴定的误差分析 | |
| 18 | 0.65 | 酸碱中和滴定的误差分析 | |
| 19 | 0.65 | 酸碱混合时的定性判断及计算 一元强酸与一元弱酸的比较 | |
| 20 | 0.65 | 有机物分离提纯操作的综合考查 物质分离、提纯的常见物理方法 | |
| 21 | 0.65 | 氮氧化物溶解于水的相关计算 二氧化氮与水反应 | |
| 22 | 0.65 | 明矾与氢氧化钡溶液反应的离子方程式 铝盐与强碱溶液反应 | |
| 23 | 0.65 | 物质的量浓度的计算 化学方程式中物质的量的运用 | |
| 24 | 0.65 | 离子反应在化合物组成的分析、鉴定的应用 | |
| 25 | 0.4 | 基于氧化还原反应守恒规律的计算 铜与强氧化性酸的反应 电子转移计算 | |
| 二、填空题 | |||
| 26 | 0.65 | 胶体的性质和应用 物质分离、提纯的常见物理方法 过滤 渗析 | |
| 29 | 0.85 | 氧化还原反应有关计算 氧化还原反应方程式的配平 电子转移计算 | |
| 31 | 0.65 | 化学方程式计算中物质的量的运用 含氧化铝的混合物的提纯 氢氧化铝与强碱反应 铁的氧化物 | |
| 三、解答题 | |||
| 27 | 0.65 | 物质分离、提纯综合应用 常见有机物的制备 | 实验探究题 |
| 28 | 0.65 | 探究物质组成或测量物质的含量 物质性质的探究 | 实验探究题 |
| 30 | 0.4 | 物质含量的测定 中和滴定 物质制备的探究 | 实验探究题 |



