辽宁省丹东市2017-2018学年高二下学期期末质量监测化学试题
辽宁
高二
期末
2020-04-30
99次
整体难度:
容易
考查范围:
有机化学基础、化学与STSE、化学实验基础、认识化学科学、常见无机物及其应用、物质结构与性质、化学反应原理
一、单选题 添加题型下试题
①硝基苯 ②甲苯 ③溴苯 ④植物油 ⑤蚁酸 ⑥乙酸乙酯 ⑦硬脂酸甘油酯
| A.①②③ | B.④⑥⑦ | C.①②④⑤ | D.②④⑥⑦ |
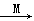 乙酸乙酯,下列说法错误的是( )
乙酸乙酯,下列说法错误的是( )| A.X可用新制的氢氧化铜检验 |
| B.Y可发生加成反应 |
| C.由Y生成乙酸乙酯的反应属于取代反应 |
| D.可用碘的四氯化碳溶液检验淀粉是否水解完全 |
【知识点】 葡萄糖与新制氢氧化铜溶液的反应 淀粉、纤维素的水解 淀粉与碘的反应
| A.乙醇、乙酸和乙酸乙酯能用饱和Na2CO3溶液鉴别 |
| B.除去乙烷中少量的乙烯,可在光照条件下通入Cl2,再气液分离 |
| C.乙烯和聚乙烯都能使溴的四氯化碳溶液褪色 |
| D.蛋白质、葡萄糖、油脂均能发生水解反应 |
| A.苯不能使酸性高锰酸钾溶液褪色,所以苯不能发生氧化反应 |
| B.石油的主要成分是烃,煤经过分馏可制得焦炭、煤焦油等产品 |
| C.丙烯分子中所有原子不可能在同一平面上 |
| D.淀粉、纤维素都是天然高分子有机物,其链节中都含有葡萄糖 |
| A.甲苯的硝化、油脂的皂化均可看作取代反应 |
| B.蛋白质水解生成葡萄糖放出热量,提供生命活动的能量 |
| C.石油裂解的目的是为了提高轻质液体燃料的产量和质量 |
| D.棉花和合成纤维的主要成分是纤维素 |

| A.它的一氯代物有6种 |
| B.它的分子中所有的碳原子一定在同一平面上 |
C.它和丁基苯(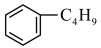 )互为同分异构体 )互为同分异构体 |
| D.一定条件下,它分别可以发生加成、取代、氧化、还原等反应 |
【知识点】 有机官能团的性质及结构 多官能团有机物的结构与性质解读
| A.相对分子质量相同的几种化合物,互为同分异构体 |
| B.分子组成相差一个或几个CH2原子团的物质,互为同系物 |
| C.C5H11Cl的同分异构体(不考虑立体异构)共有8种 |
| D.淀粉与纤维素是化学式为(C6H10O5)n的同分异构体 |
| A.标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为7/22.4NA |
| B.1 mol甲基(—CH3)所含的电子总数为9NA |
| C.0.5 mol 1,3-丁二烯分子中含有C=C双键数为NA |
| D.1 mol碳正离子(CH3+)所含的电子总数为8NA |
【知识点】 阿伏加德罗常数的求算解读

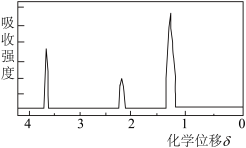
| A.含有碳碳双键、羟基、羰基、羧基 | B.含有苯环、羟基、羰基、羧基 | C.含有羟基、羰基、羧基、酯基 | D.含有碳碳双键、苯环、羟基、羰基 |
【知识点】 常见官能团名称、组成及结构解读
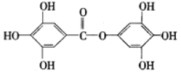 ,lmol A与足量的NaOH溶液混合共热,充分反应后最多消耗NaOH的物质的量为
,lmol A与足量的NaOH溶液混合共热,充分反应后最多消耗NaOH的物质的量为| A.6mol | B.7mol | C.8mol | D.9mol |
| A.CH4和C4H10 | B.乙酸和甲酸甲酯 |
C.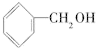 和 和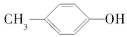 | D.苯甲酸和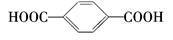 |
【知识点】 同系物的判断解读 简单有机物同分异构体书写及辨识解读
| A.戊烷有2种同分异构体 |
| B.C8H10中只有3种属于芳香烃的同分异构体 |
| C.甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有6种 |
| D.CH3CH2CH2CH3光照下与氯气反应,只生成1种一氯代烃 |
【知识点】 同分异构体的数目的确定解读
| A.10种 | B.12种 | C.11种 | D.13种 |
| A.3种 | B.4种 | C.5种 | D.6种 |
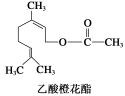
①属于芳香族化合物;②不能发生银镜反应;③分子式为C12H20O2;④它的同分异构体中可能有酚类;⑤1mol该有机物水解时只能消耗1molNaOH
| A.②③④ | B.①④⑤ | C.①②③ | D.②③⑤ |
| A.2mL | B.4 mL | C.8 mL | D.无法求解 |
【知识点】 烃燃烧产物的量和烃的组成关系解读
| A.在标况下,11.2LNO与11.2LO2混合后所含分子数为0.75NA |
| B.铝跟氢氧化钠溶液反应生成1mol氢气时,转移的电子数为NA |
| C.0.1molNa2O2晶体中含有0.4NA个离子 |
| D.常温常压下,16gO3所含的电子数为8NA |
| A.NaNO3和NaCl | B.CuO和木炭粉 |
| C.MnO2和KCl | D.BaSO4和AgCl |
| A.用SO2水溶液吸收Br2:SO2+Br2+2H2O=4H++SO42-+2Br- |
| B.酸性高锰酸钾和过氧化氢制取少量氧气:4MnO4-+4H2O2+12H+=4Mn2++7O2↑+10H2O |
| C.用稀硫酸除去铜绿:4H++Cu2(OH)2CO3=2Cu2++CO2↑+3H2O |
| D.少量Ba(HCO3)2溶液与NaOH溶液反应:Ba2++2HCO3-+2OH-=BaCO3↓+2H2O+CO32- |
【知识点】 离子方程式的书写解读 离子方程式的正误判断解读
| A.无法确定 | B.等于40% |
| C.小于40% | D.大于40% |
【知识点】 物质的量浓度的基础计算解读
| A.Cu2S既是氧化产物又是还原产物 |
| B.5molFeS2发生反应,有21mole—转移 |
| C.CuSO4和FeS2是氧化剂,FeS2是还原剂 |
| D.产物中的SO42—有一部分是氧化产物 |
【知识点】 氧化还原反应基本概念 氧化还原反应有关计算 氧化还原反应的规律解读
| A.19.7g | B.22.3g | C.30.7g | D.39.2g |
【知识点】 氧化还原反应有关计算 物质含量的测定
| A.x≤a,2I−+Cl2=I2+2Cl− |
| B.x=1.2a,10Fe2++14I−+12Cl2=10Fe3++7I2+24Cl− |
| C.x=1.4a,4Fe2++10I−+7Cl2=4Fe3++5I2+14Cl− |
| D.x≥1.5a,2Fe2++4I−+3Cl2=2Fe3++2I2+6Cl− |
【知识点】 离子方程式的书写解读 氧化性、还原性强弱的比较解读
| A.肯定有Na+、Al3+、Mg2+、SO42- | B.肯定有Na+、Mg2+、Al3+、Cl- |
| C.肯定没有K+、HCO3-、MnO4- | D.肯定没有K+、NH4+、Cl- |
【知识点】 离子反应在化合物组成的分析、鉴定的应用解读 离子的检验
| A.从性质的角度分类,SO2和NO2都属于酸性氧化物 |
| B.从在水中是否发生电离的角度,SO2和NO2都属于电解质 |
| C.从元素化合价的角度分类,SO2和NO2都既可作氧化剂又可作还原剂 |
| D.从对大气及环境影响和颜色的角度,SO2和NO2都是大气污染物,都是有色气体 |