北京市朝阳区中国人民大学附属中学朝阳学校2019-2020学年高一上学期10月月考化学试卷
北京
高一
阶段练习
2021-10-11
527次
整体难度:
适中
考查范围:
认识化学科学、有机化学基础、物质结构与性质、常见无机物及其应用、化学实验基础
一、单选题 添加题型下试题
 |  |  |  |
| A.甲醇低温所制氢气用于新能源汽车 | B.氘、氚用作“人造太阳”核聚变燃料 | C.偏二甲肼用作发射“天宫二号”的火箭燃料 | D.开采可燃冰,将其作为能源使用 |
| A.A | B.B | C.C | D.D |
| A.Cl2 | B.HCl | C.MgCl2 | D.Mg(OH)2 |
| A.光是一种胶体 |
| B.雾是一种胶体 |
| C.薄雾中的小水滴颗粒大小约为10-9 m~10-7 m |
| D.发生丁达尔效应 |
A.H2SO4=2H++SO | B.NaHSO4=Na++H++SO |
| C.KOH=K++OH- | D.CO2=C4++2O2- |
【知识点】 电解质、非电解质概念解读 电离方程式解读
| A.酸在水溶液中电离产生的阳离子全部是氢离子 |
| B.碱在水溶液中电离产生的阴离子全部是氢氧根离子 |
| C.盐在水溶液中电离一定有金属阳离子产生 |
| D.酸和盐在水溶液中电离都可能有含氧酸根离子产生 |
【知识点】 酸、碱、盐、氧化物的概念及其相互联系解读 电解质的电离
| A.氧化物:CO2 NO SO2 H2O |
| B.碱:NaOH KOH Ba(OH)2 Na2CO3 |
| C.铵盐:NH4Cl NH4NO3 (NH4)2SO4 NH3•H2O |
| D.碱性氧化物:Na2O CaO Mn2O7 MgO |
| A.铜铸塑像上出现铜绿[Cu2(OH)2CO3] | B.充有氢气的气球遇明火爆炸 |
| C.大理石雕像被酸雨腐蚀毁坏 | D.铁质菜刀生锈 |
【知识点】 氧化还原反应基本概念
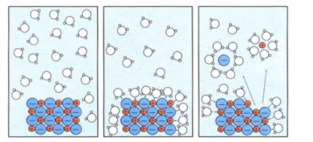
| A.氯化钠是由钠离子和氯离子组成的 |
| B.氯化钠在水中形成能自由移动的水合钠离子和水合氯离子 |
| C.氯化钠的电离方程式为:NaCl=Na++Cl- |
| D.氯化钠的电离过程需要通电才能完成 |
| A.Fe是氧化剂 | B.CuSO4是还原剂 |
| C.Fe被氧化 | D.CuSO4发生氧化反应 |
【知识点】 氧化还原反应基本概念
| A.Cl2O | B.ClO2 | C.Cl2O7 | D.Cl2O5 |
【知识点】 酸、碱、盐、氧化物的概念及其相互联系解读 其他含卤化合物
| A.硝酸钾溶液能导电,所以硝酸钾溶液是电解质 |
| B.石墨有较好的导电性,所以石墨属于电解质 |
| C.液态氯化氢、固态氯化钠均不能导电,所以氯化氢、氯化钠均不是电解质 |
| D.蔗糖在水溶液中和熔融状态下均不能导电,所以蔗糖是非电解质 |
【知识点】 电解质与非电解质
| A.2Cl2+2Ca(OH)2=CaCl2 +Ca(ClO)2+2H2O |
| B.SO2+Cl2+2H2O=H2SO4+2HCl |
| C.CaCO3+2HCl=CaCl2+CO2↑+H2O |
D.2KClO3 2KCl+3O2↑ 2KCl+3O2↑ |
【知识点】 氧化还原反应的几组概念解读 常见氧化剂与还原剂解读
A.H+、K+、Cu2+、SO | B.Mg2+、NO 、Na+、Cl- 、Na+、Cl- |
C.NO 、Cl-、Na+、Ag+ 、Cl-、Na+、Ag+ | D.Na+、K+、Cl-、HCO |
【知识点】 限定条件下的离子共存解读
| A.Ca(HCO3)2+2NaOH=CaCO3↓+Na2CO3+2H2O |
| B.Ca(OH)2+K2CO3=CaCO3↓+2KOH |
| C.2KHCO3+Ca(OH)2=CaCO3↓+K2CO3+2H2O |
| D.Ca(OH)2+CO2=CaCO3↓+H2O |
【知识点】 离子反应的发生及书写 离子方程式的书写解读
 及泥沙,得到纯净的KCl,可将固体溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序
及泥沙,得到纯净的KCl,可将固体溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序①过滤;②加过量KOH溶液;③加适量盐酸;④加过量K2CO3溶液⑤加过量BaCl2溶液
| A.②①⑤④③ | B.④①②⑤③ | C.②⑤④①③ | D.①④②⑤③ |
【知识点】 物质的分离、提纯 物质分离、提纯的常见化学方法解读
| A.金属铁与硫酸反应有气泡产生:Fe+2H+=Fe3++H2↑ |
B.向NaOH溶液中通入少量的CO2气体:CO2+2OH-=H2O+CO |
C.稀硫酸与Ba(OH)2溶液反应:SO +Ba2++OH-+H+=BaSO4↓+H2O +Ba2++OH-+H+=BaSO4↓+H2O |
| D.硫酸铜溶液与NaOH溶液反应:OH-+Cu2+=CuOH↓ |
【知识点】 离子反应的发生及书写 离子方程式的书写解读 离子方程式的正误判断解读
| A.NaOH,FeCl3 | B.Ba(OH)2、Fe2(SO4)3 |
| C.Ba(OH)2、CuSO4 | D.NaOH、CuCl2 |
【知识点】 离子反应概念解读 离子反应的发生及书写 离子反应的发生条件解读
| A.CaH2既是氧化剂,又是还原剂 |
| B.H2既是氧化产物,又是还原产物 |
| C.CaH2是还原剂,H2O是氧化剂 |
| D.氧化产物与还原产物的质量比为1∶1 |
二、 添加题型下试题
| A.Cu+2Fe3+=Cu2++2Fe2+ | B.10Cl-+2MnO +16H+=2Mn2++5Cl2↑+8H2O +16H+=2Mn2++5Cl2↑+8H2O |
| C.2Fe2++Cl2=2Fe3++2Cl- | D.5Pb2++2MnO +2H2O=5PbO2+2Mn2++4H+ +2H2O=5PbO2+2Mn2++4H+ |
三、填空题 添加题型下试题
A.CaO、Na2O、CO2、CuO
B.H2、O2、S、Cu
C.O2、Fe、Cu、Zn
D.H3PO4、H2O、H2SO4、HNO3
(1)以上四组物质中与其他类别不同的物质依次是(填化学式)A
(2)A、B、C、D这四种物质共同作用可生成一种碱式盐,该反应属于四大基本反应类型中的
(1)选择适宜的物质完成下列反应,并写出有关反应的化学方程式:
①
 +2H+=CO2↑+H2O
+2H+=CO2↑+H2O②Ag++Cl-=AgCl↓
(2)写出下列反应的离子方程式:
①盐酸溶解氢氧化铜沉淀
②硫酸氢钠溶液中加入少量碳酸钠溶液:
③碳酸氢钠溶液中加入少量氢氧化钠溶液:
四、解答题 添加题型下试题

(1)联合制碱所制得的碱是指
(2)①~③所涉及的操作方法中,包含过滤的是
(3)NaHCO3溶于水发生的电离方程式是:
(4)根据图,将上述化学方程式补充完整:
NH3+CO2+__________+__________=NaHCO3↓+NH4Cl
(5)②是煅烧NaHCO3固体,分解产物有三种,分别是碳酸钠、CO2、
五、填空题 添加题型下试题
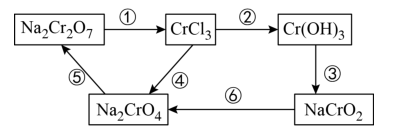
(1)在上述有编号的步骤中,需用还原剂的是
(2)在Na2Cr2O7+6KI+14HCl=2CrCl3+2NaCl+3I2+7H2O反应中
①
②用双线桥标明电子转移方向与数目:
(1)取少量Fe2O3粉末(红棕色)加入适量盐酸,所发生的离子方程式为
(2)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴
(3)取另一小烧杯也加入20mL蒸馏水,向烧杯中加入1mLFeCl3溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到
(4)取乙烧杯中少量Fe(OH)3胶体置于试管中,向试管中滴加一定量稀盐酸,边滴边振荡,可以看到溶液红褐色逐渐变浅,最终得到澄清的FeCl3溶液,发生此变化的化学方程式为
(5)已知Al(OH)3胶体能够净水,则Fe(OH)3胶体
六、解答题 添加题型下试题
①将固体混合物溶于水,搅拌后得到无色透明溶液;
②在①所得的溶液中滴加Ba(NO3)2溶液,有白色沉淀生成;
③过滤,然后在所得白色沉淀中加入过量稀硝酸,沉淀部分溶解。
由此判断:
(1)原混合物中肯定有
(2)写出上述实验过程中可能发生反应的离子方程式:
(3)对可能含有的物质采用的检验方法是
【知识点】 离子反应在化合物组成的分析、鉴定的应用解读 离子的检验
一氧化碳与氧化铁反应生成的黑色物质真的是铁粉吗?于是他们进行了以下探究:
【查阅资料】
资料一:铁粉和四氧化三铁粉末能被磁铁吸引而氧化亚铁(黑色)不能;
资料二:四氧化三铁中铁元素有+2、+3两种化合价,其化学式可用FeO·Fe2O3的形式表示;
【提出猜想】黑色物质可能是四氧化三铁、氧化铁和铁粉中的一种或几种。
【进行实验】兴趣小组收集了一氧化碳与氧化铁反应生成的黑色物质进行了下列实验:
| 实验方案 | 实验现象 | |
| 甲 | 取少量黑色物质用磁铁吸引 | 黑色物质全部被磁铁吸引 |
| 乙 | 取少量黑色物质加入30%热的HCl中 | 无气泡、溶液颜色变成黄绿色 |
| 丙 | 取少量黑色物质加入CuSO4溶液中 | 无任何现象 |
①甲实验现象说明黑色物质中没有
生成的黑色物质应为四氧化三铁。
②写出黑色粉末和热的盐酸反应的化学方程式
(2)【拓展探究】
同学们对四氧化三铁产生了兴趣,从参考资料中找到了氧化沉淀法生产复印用高档四氧化三铁粉的工艺流程简图。

【生产流程】
【查阅资料】
资料一:硫酸亚铁在不同温度下的溶解度如表所示:
| 温度/℃ | 0 | 10 | 30 | 50 | 60 | 70 | 80 | 90 |
| 溶解度 | 14.0 | 17.0 | 25.0 | 33.0 | 35.3 | 33.0 | 30.5 | 27.0 |
资料三:获得四氧化三铁的反应原理为:Fe(OH)2+2Fe(OH)3
 Fe3O4+4H2O
Fe3O4+4H2O【问题讨论】
①溶解时,用50℃至80℃的热水目的是
②写出加入适量氢氧化钠溶液时发生反应的化学方程式
③上述过程中,要控制“通一定量空气”的目的是
④要使四氧化三铁的产率最高,则上述流程中产生的氢氧化亚铁和氢氧化铁的最佳质量比为
⑤副产品P是硫酸钠,由溶液N获得该副产品的操作顺序是b→
a.过滤 b.加热浓缩
c.冷却结晶 d.晶体加热至完全失去结晶水
试卷分析
试卷题型(共 29题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 物理变化与化学变化 甲烷的存在及用途 生活中常见的几种醇 核素 | |
| 2 | 0.65 | 化学物质的分类方法 酸、碱、盐、氧化物的概念及其相互联系 | |
| 3 | 0.85 | 分散系概念及其分类 | |
| 4 | 0.94 | 电解质、非电解质概念 电离方程式 | |
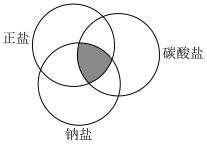
| 5 | 0.65 | 交叉分类法 酸、碱、盐、氧化物 碳酸钠 碳酸氢钠 | |
| 6 | 0.65 | 酸、碱、盐、氧化物的概念及其相互联系 电解质的电离 | |
| 7 | 0.65 | 交叉分类法 树状分类法 酸、碱、盐、氧化物的概念及其相互联系 | |
| 8 | 0.94 | 氧化还原反应基本概念 | |
| 9 | 0.85 | 电离的定义 电离方程式 | |
| 10 | 0.65 | 氧化还原反应基本概念 | |
| 11 | 0.85 | 酸、碱、盐、氧化物的概念及其相互联系 其他含卤化合物 | |
| 12 | 0.85 | 电解质与非电解质 | |
| 13 | 0.85 | 氧化还原反应的几组概念 常见氧化剂与还原剂 | |
| 14 | 0.85 | 限定条件下的离子共存 | |
| 15 | 0.94 | 胶体 渗析 | |
| 16 | 0.65 | 离子反应的发生及书写 离子方程式的书写 | |
| 17 | 0.85 | 物质的分离、提纯 物质分离、提纯的常见化学方法 | |
| 18 | 0.85 | 离子反应的发生及书写 离子方程式的书写 离子方程式的正误判断 | |
| 19 | 0.65 | 离子反应概念 离子反应的发生及书写 离子反应的发生条件 | |
| 20 | 0.85 | 氧化还原反应基本概念 氧化还原反应的应用 氧化还原反应在生活、生产中的应用 氧化还原反应的规律 | |
| 二、 | |||
| 21 | 0.85 | 离子方程式的正误判断 氧化性、还原性强弱的比较 氧化还原反应的规律 | |
| 三、填空题 | |||
| 22 | 0.85 | 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系 四种基本反应类型 | |
| 23 | 0.65 | 离子反应概念 离子反应的发生及书写 离子反应的发生条件 离子方程式的书写 | |
| 24 | 0.94 | 氧化还原反应在生活、生产中的应用 氧化还原反应的规律 | |
| 26 | 0.85 | 氧化还原反应的几组概念 单线桥、双线桥分析氧化还原反应 氧化还原反应在生活、生产中的应用 | |
| 27 | 0.85 | 胶体的性质和应用 胶体的制备 四种基本反应类型 | |
| 四、解答题 | |||
| 25 | 0.65 | 氨的碱性 碳酸氢钠 碳酸钠与碳酸氢钠的相互转化 物质分离、提纯综合应用 | 工业流程题 |
| 28 | 0.65 | 离子反应在化合物组成的分析、鉴定的应用 离子的检验 | 实验探究题 |
| 29 | 0.65 | 几种铁的氧化物的化学性质 有关铁及其化合物转化的流程题型 铁及铁的氧化物混合物反应的相关计算 常见无机物的制备 | 实验探究题 |