云南省玉溪市华宁一中2020-2021学年高一下学期期中考试化学试题
云南
高一
期中
2021-06-15
306次
整体难度:
适中
考查范围:
认识化学科学、有机化学基础、常见无机物及其应用、化学实验基础、化学与STSE、物质结构与性质、化学反应原理
一、单选题 添加题型下试题
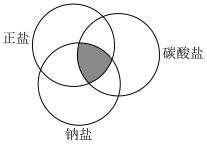
| A.分子式相同 |
| B.分子中各元素的质量分数分别相同 |
| C.相同质量燃烧时,产生二氧化碳的物质的量相同 |
| D.相同质量燃烧时,消耗氧气的物质的量相同 |
| A.2Na+2H2O=2NaOH+H2↑ |
| B.CaO+H2O=Ca(OH)2 |
| C.3NO2+H2O=2HNO3+NO |
| D.2F2+2H2O=4HF+O2 |
【知识点】 氧化还原反应基本概念 常见氧化剂与还原剂解读
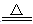 MnCl2+Cl2↑+2H2O,当生成7.1gCl2时,被氧化的HCl的质量是
MnCl2+Cl2↑+2H2O,当生成7.1gCl2时,被氧化的HCl的质量是| A.3.65g | B.7.3g | C.10.95g | D.14.6g |
【知识点】 氧化还原反应有关计算 与氧化剂、还原剂有关的计算解读

下列叙述中正确的是( )
| A.偏二甲肼的摩尔质量为60g |
| B.6.02×1023个偏二甲肼分子的质量为60g |
| C.1mol偏二甲肼的质量为60g•mol-1 |
| D.6g偏二甲肼含有NA个偏二甲肼分子 |
| A.二氧化硫、氮氧化物、一氧化碳、可吸入颗粒物 |
| B.二氧化硫、氮氧化物、二氧化碳、可吸入颗粒物 |
| C.稀有气体、氮氧化物、一氧化碳、可吸入颗粒物 |
| D.稀有气体、氮氢化物、一氧化碳、可吸入颗粒物 |
| A.Fe2O3 | B.Fe3O4 | C.Fe4O5 | D.Fe5O7 |

| A.铝球表面有气泡产生,且有白色沉淀生成,杠杆不平衡 |
| B.铝球表面有气泡产生,溶液澄清;铁球表面有红色物质析出,溶液蓝色变浅,杠杆右边下沉 |
| C.反应后去掉两烧杯,杠杆仍平衡 |
| D.右边球上出现红色,左边溶液的碱性增强 |
| A.CaCO3 | B.P2O5 | C.CuO | D.KMnO4 |
| A.第三周期ⅠA族 | B.第三周期ⅡA族 |
| C.第四周期ⅠA族 | D.第四周期ⅡA族 |
【知识点】 元素周期表提供的元素信息解读
| A.单宁作还原剂 | B.单宁作氧化剂 |
| C.单宁被还原 | D.单宁中某元素化合价降低 |
【知识点】 氧化还原反应基本概念 氧化还原反应的应用
| A.Na | B.Cu | C.H2 | D.Fe |
【知识点】 氯气与非金属单质的反应解读 氯气与金属单质的反应解读
| A.b+n+2 | B.b+n-2 |
| C.b-n-2 | D.b-n+2 |
| A.CO2和Na2CO3 | B.CO和CO2 |
| C.CO和H2CO3 | D.CH4和CO2 |
【知识点】 有关粒子结构的化学用语
| A.Na2CO3和盐酸 | B.AlCl3和NaOH |
| C.NaAlO2和硫酸 | D.Na2CO3和BaCl2 |
| (1)a和b混合 | 气体变红棕色 |
| (2)c和d混合 | 产生白烟 |
| (3)c和e分别通入少量溴水中 | 溴水都变成无色透明的液体 |
| (4)b和e分别通入氢硫酸中 | 都产生淡黄色浑浊 |
| A.O2、NO、HCl、NH3、CO2 | B.O2、NO、NH3、HCl、SO3 |
| C.NO、O2、NH3、HCl、SO2 | D.HCl、CO2、NH3、H2S、CH4 |
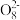 +H2O→Mn
+H2O→Mn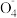 +S
+S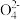 +H+。下列说法正确的是
+H+。下列说法正确的是| A.该反应中起氧化作用的是Mn2+ |
| B.反应后溶液的酸性增强 |
| C.反应中有1个还原剂参加反应,则转移4个电子 |
| D.该反应常用于检验溶液中Mn2+的存在,现象是溶液紫红色消失 |
| A.合金的密度比各成分金属小 |
| B.合金的抗腐蚀性能都很好 |
| C.合金的导电性比各成分金属强 |
| D.合金的种类和性能与成分有关 |
【知识点】 金属材料的性质及利用 金属与合金性能比较解读
| A.2:1 | B.2:3 | C.1:1 | D.1:2 |
【知识点】 利用烃完全燃烧耗氧量的规律进行的计算解读
| A.构成原电池正极和负极的材料必须是两种金属 |
| B.由铜、锌作电极与稀硫酸溶液组成的原电池中铜是负极 |
| C.电子通过稀硫酸溶液由锌流向铜,通过溶液时被氢离子得到而放出氢气 |
| D.铜锌原电池工作时,溶液的酸性降低 |
| A.33 g | B.24 g | C.29 g | D.22 g |
【知识点】 化学方程式计算中物质的量的运用解读 硫与金属单质的反应解读
二、解答题 添加题型下试题
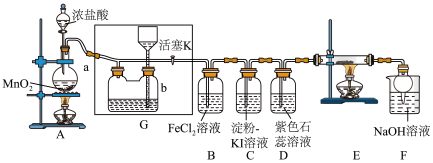
(1)A中发生反应的化学方程式为
(2)实验开始时,先打开分液漏斗旋塞和活塞K,点燃A处酒精灯,让氯气充满整个装置,再点燃E处酒精灯。回答下列问题:
①在装置D中能看到的实验现象是
②在装置E的硬质玻璃管内盛有炭粉,发生氧化还原反应,产物为CO2和HCl,则E中发生反应的化学方程式为
③装置F中球形干燥管的作用是
(3)储气瓶b内盛放的试剂是
(4)装置B中FeCl2被Cl2氧化,反应的化学方程式为

(1)如图装置,在干燥管中装入Na2O2后,打开活塞加入稀硫酸,生成CO2。打开K1,关闭K2,加热铜丝,目的是
(2)若打开K2,关闭K1,出现
(3)根据以上的实验结论,写出生成CO2、O2反应的化学方程式:
【知识点】 过氧化钠和二氧化碳反应解读 物质性质的探究解读
三、填空题 添加题型下试题
(1)物质C的名称为
(2)单质A在单质B中燃烧的化学方程式为
(3)单质B与水反应的化学方程式为
(4)化合物D与水反应的化学方程式为
四、解答题 添加题型下试题
| 阳离子 | Na+、H+、Ba2+ |
| 阴离子 | OH-、CO 、SO 、SO |
(2)乙溶液与丙溶液反应可生成气体M,则M的化学式为
(3)乙、丙溶液与甲溶液反应可分别生成白色沉淀A和B,其中B可溶于稀硝酸。
①乙的化学式为
②B溶于稀硝酸的离子方程式为
五、填空题 添加题型下试题
(1)除去氯化钙加入的试剂是
(2)除去氯化镁加入的试剂是
(3)除去硫酸钠加入的试剂是
六、解答题 添加题型下试题
(1)实验过程:在一支试管中加入5 mL 5%的H2O2溶液,然后滴入适量的FeCl3溶液,把带火星的木条伸入试管。
实验现象:
实验结论:FeCl3溶液可以催化分解H2O2。
(2)已知FeCl3在水中可解离出Fe3+和Cl-,同学们提出以下猜想:
甲同学的猜想:真正催化分解H2O2的是FeCl3溶液中的H2O;
乙同学的猜想:真正催化分解H2O2的是FeCl3溶液中的Fe3+;
丙同学的猜想:真正催化分解H2O2的是FeCl3溶液中的Cl-。
你认为最不可能的是
(3)同学们对余下的两个猜想,用实验进行了探究,请你仔细分析后填表:
| 实验过程 | 实验现象 | 结论 |
【知识点】 催化剂对化学反应速率的影响解读 化学实验探究
试卷分析
试卷题型(共 31题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 有机物的结构式、结构简式、比例模型、球棍模型、最简式 烃燃烧相关计算 利用等效变形思想解答有机物燃烧问题 | |
| 2 | 0.65 | 交叉分类法 酸、碱、盐、氧化物 碳酸钠 碳酸氢钠 | |
| 3 | 0.65 | 氧化还原反应基本概念 常见氧化剂与还原剂 | |
| 4 | 0.85 | 硅的物理性质与用途 | |
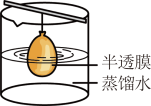
| 5 | 0.65 | 分散系概念及其分类 胶体的性质和应用 萃取和分液 渗析 | |
| 6 | 0.85 | 氧化还原反应有关计算 与氧化剂、还原剂有关的计算 | |
| 7 | 0.65 | 摩尔质量与相对原子质量区别与联系 根据n=m/M进行相关计算 以N=m·NA/M为中心的有关基本粒子的推算 | |
| 8 | 0.94 | 大气污染 大气污染来源及危害 | |
| 9 | 0.65 | 物质的量有关计算 氧化还原反应的规律 氯气与还原性化合物的反应 铁的氧化物 | |
| 10 | 0.85 | 铝与强碱溶液反应 铁 | |
| 11 | 0.94 | 化学物质的分类方法 分类方法的应用 无机物质的分类 | |
| 12 | 0.65 | 元素周期表提供的元素信息 | |
| 13 | 0.85 | 氧化还原反应基本概念 氧化还原反应的应用 | |
| 14 | 0.85 | 氯气与非金属单质的反应 氯气与金属单质的反应 | |
| 15 | 0.94 | 原子的基本构成 原子中相关数值及其之间的相互关系 具有相同结构的多种离子的性质相关分析及判断 | |
| 16 | 0.94 | 有关粒子结构的化学用语 | |
| 17 | 0.85 | 同系物的概念 同系物的判断 | |
| 18 | 0.65 | 碳酸钠与盐酸的反应 铝盐与强碱溶液反应 偏铝酸钠与盐酸的反应 | |
| 19 | 0.65 | 一氧化氮的化学性质 二氧化硫的弱氧化性 常见气体的检验 | |
| 20 | 0.94 | 铁 铁的物理性质 | |
| 21 | 0.65 | 氧化还原反应有关计算 氧化还原反应方程式的配平 氧化还原反应的规律 | |
| 22 | 0.85 | 金属材料的性质及利用 金属与合金性能比较 | |
| 23 | 0.4 | 利用烃完全燃烧耗氧量的规律进行的计算 | |
| 24 | 0.65 | 原电池原理理解 原电池电子流向判断及应用 原电池正负极判断 | |
| 25 | 0.85 | 化学方程式计算中物质的量的运用 硫与金属单质的反应 | |
| 二、解答题 | |||
| 26 | 0.65 | 氯气的实验室制法 氯气与还原性化合物的反应 综合实验设计与评价 | 实验探究题 |
| 27 | 0.65 | 过氧化钠和二氧化碳反应 物质性质的探究 | 实验探究题 |
| 29 | 0.85 | 离子方程式的书写 离子反应在化合物组成的分析、鉴定的应用 硫酸根离子的检验 | 无机推断题 |
| 31 | 0.94 | 催化剂对化学反应速率的影响 化学实验探究 | 实验探究题 |
| 三、填空题 | |||
| 28 | 0.65 | 氯气与水的反应 过氧化钠与水的反应 | |
| 30 | 0.94 | 离子反应在混合物分离、除杂中的应用 物质分离、提纯的常见化学方法 | |