云南省通海三中2019-2020学年高一上学期期末考试化学试题
云南
高一
期末
2020-01-12
285次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、物质结构与性质、化学实验基础
一、单选题 添加题型下试题
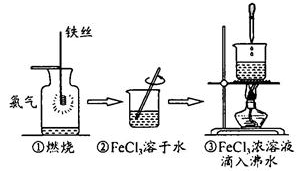
| A.实验①、③反应制得的物质均为纯净物 |
| B.实验②、③均未发生氧化还原反应 |
| C.实验②、③均为放热反应 |
| D.实验①、②所涉及的物质均为电解质 |
| A.原子最外层电子数由多到少的顺序:Y、X、W、Z |
| B.原子半径由大到小的顺序:W、Z、Y、X |
| C.元素非金属性由强到弱的顺序:Z、W、X |
| D.简单气态氢化物的稳定性由强到弱的顺序:X、Y、W |
A.新制氯水含有 、 、 、 、 、 、 分子 分子 |
B. 溶液滴入新制氯水中,有无色气泡产生 溶液滴入新制氯水中,有无色气泡产生 |
| C.氯水和液氯都能使干燥的有色布条褪色 |
| D.新制氯水的pH要比久置氯水的pH小 |
| A.ⅥA | B.ⅣB | C.ⅢB | D.ⅣA |
【知识点】 元素周期表结构
A.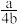 mol-1 mol-1 | B.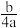 mol-1 mol-1 | C. mol-1 mol-1 | D. mol-1 mol-1 |
| A.粒子大小相同 | B.粒子质量相同 |
| C.粒子间距离相同 | D.粒子间作用力相同 |
【知识点】 决定物质体积大小的微观因素解读 阿伏加德罗定律及其推论解读
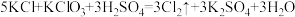 ,下列说法不正确的是
,下列说法不正确的是A. 是氧化剂 是氧化剂 |
| B.被氧化与被还原的氯元素的质量比为5∶1 |
C. 既不是氧化剂又不是还原剂 既不是氧化剂又不是还原剂 |
D. 参加反应时有10mol电子转移 参加反应时有10mol电子转移 |
【知识点】 氧化还原反应的几组概念解读 氧化还原反应有关计算 电子转移计算
| A.A>B>C | B.B>A>C | C.C>A>B | D.C>B>A |
| A.过氧化钠——漂白剂 |
| B.次氯酸钠——消毒剂 |
| C.纯碱——治疗胃酸过多 |
| D.小苏打——制作馒头和面包的膨松剂 |
| A.H2SO4→SO2 | B.H2S→SO2 |
| C.S→SO2 | D.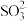 →SO2 →SO2 |
【知识点】 氧化还原反应基本概念 氧化还原反应的规律解读
| A.磷酸钠 | B.硫酸铝 | C.氯化钡 | D.硫酸钾 |
【知识点】 化学物质的分类方法
| A.Na2O2是淡黄色固体,久置于空气中变成Na2O |
| B.Na2O2与水的反应中,Na2O2只作氧化剂 |
| C.用Na2O2漂白过的织物、麦秆等日久又渐渐变成黄色 |
| D.Na2O2放入饱和NaOH溶液中,放出大量的O2,并有白色固体析出 |
【知识点】 过氧化钠的物理性质、组成、结构及用途解读
| A.赤铁矿的主要成分是Fe3O4 |
| B.赤铁矿的主要成分与铁锈的主要成分不相同 |
| C.磁铁矿粉末溶于盐酸后,加入KSCN溶液,溶液变红色 |
| D.Fe3O4俗称铁红 |
| A.都能电离出金属离子 | B.都能与酸反应生成盐和水 |
| C.都能使无色酚酞溶液变成红色 | D.溶液中都含有OH- |
【知识点】 无机物质的分类
| A.Fe2O3 | B.Fe3O4 | C.Fe4O5 | D.Fe5O7 |
| A.OH-、F-、Ne、O2- |
| B.H2O、CH4、NH3、Ne |
| C.H3O+、Na+、NH4+、Mg2+ |
| D.O2-、F-、Mg2+、Al3+ |
| A.化合物 | B.盐 | C.钠盐 | D.碱 |
【知识点】 无机物质的分类
| A.最外层有7个电子 | B.原子半径比碘大 |
| C.易失去电子 | D.得到电子能力比碘弱 |
| A.容量瓶用蒸馏水洗涤后未干燥即用来配制溶液 |
| B.定容时,观察液面俯视刻度线 |
| C.摇匀后,液面低于刻度线,没有再加蒸馏水 |
| D.用蒸馏水洗涤烧杯和玻璃棒,并将洗涤液转移入容量瓶中 |
【知识点】 配制一定物质的量浓度的溶液实验的误差分析解读
| A.分散系是否有丁达尔现象 |
| B.分散质粒子是否带电荷 |
| C.分散系是否稳定 |
| D.分散质粒子直径的大小 |
【知识点】 分散系概念
| A.7d | B.5d | C.2.5d | D.2d |
【知识点】 摩尔质量的概念解读 阿伏加德罗定律及其推论解读
| A.是碳元素的一种同素异形体 | B.是碳元素的一种同位素原子 |
| C.全部由12C组成 | D.能溶于水 |
【知识点】 无机物质的分类 物质结构与性质综合考查解读
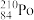 的说法正确的是( )
的说法正确的是( )| A.钋原子的核外电子数是126 |
| B.钋原子核内中子数与质子数之差是42 |
| C.钋原子核内中子数是84 |
| D.钋元素的相对原子质量是210 |
| A.Na+、NO3-、K+、OH- | B.MnO4-、K+、SO42-、Na+ |
| C.K+、SO42-、HCO3-、Na+ | D.NH4+、NO3-、Mg2+、Cl- |
【知识点】 限定条件下的离子共存解读
| A.电解质不一定能导电,能导电的物质不一定是电解质 |
| B.非电解质不导电,不导电的物质一定是非电解质 |
| C.溶于水或熔融状态下能导电的物质一定是电解质 |
| D.酸、碱、盐都是电解质,氧化物都是非电解质 |
【知识点】 电解质与非电解质
| A.Na+、Ca2+、SO42-、Cl- | B.H+、Mg2+、CO32-、S2- |
| C.K+、Mg2+、SO42-、NO3- | D.K+、Na+、NO3-、SO42- |
【知识点】 限定条件下的离子共存解读

| A.X为氢氧化钠,Y为氯化铝 |
| B.X为氯化铝,Y为氢氧化钠 |
| C.X为盐酸,Y为偏铝酸钠 |
| D.X为偏铝酸钠,Y为盐酸 |
【知识点】 铝盐与强碱溶液反应解读 偏铝酸钠与盐酸的反应解读
| A.漂白粉是化合物 | B.水玻璃是纯净物 |
| C.盐酸是电解质 | D.纯碱不属于碱 |
| A.1 g CaCO3 | B.0.8 mol H2SO4 | C.10 mL H2O | D.54 g Al |
【知识点】 摩尔质量的概念解读 摩尔质量与相对原子质量区别与联系解读
二、填空题 添加题型下试题

一个体重50 kg的健康人含铁2 g,这2g铁在人体中以Fe2+和Fe3+的形式存在。以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是
A.Fe B.Fe2+ C.Fe3+
(2)亚硝酸钠有毒,有传言说亚硝酸钠是致癌物质,但事实上亚硝酸钠并不是致癌物质,致癌的是亚硝酸钠在一定条件下生成的亚硝胺。工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有
A.Cl2 B.O2 C.FeCl3 D.KMnO4(H+)
(3)在Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了
三、解答题 添加题型下试题
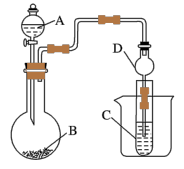
(1)仪器A的名称为
(2)已知在常温下,高锰酸钾和浓盐酸反应能生成氯气。实验室中现有药品Na2S溶液、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫的;装置A、B、C中所装药品分别为
(3)若要证明非金属性:S>C>Si,则A中加

请回答该实验中的问题。
(1)实验前必须对整套装置进行气密性的检查,操作方法是
(2)圆底烧瓶中盛装的是水,该装置受热后的主要作用是
(3)酒精灯和酒精喷灯点燃的顺序是
(4)干燥管中盛装的物质可以是
(5)如果要在A处玻璃管口处点燃该气体,则必须对该气体进行
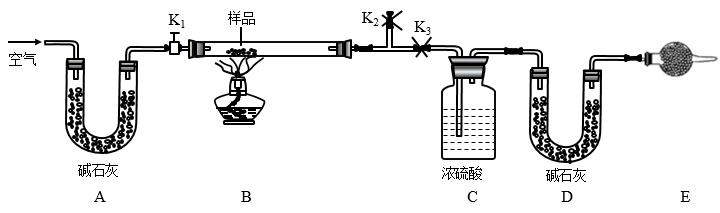
(1)实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是
②称取样品,并将其放入硬质玻璃管中,称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟,其目的是
④关闭活塞K1、K2,打开K3,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学方程式为
⑤打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U形管D的质量。
(2)关于该实验方案,请回答下列问题。
①若加热反应后不鼓入空气,对NaCl质量测定结果的影响是
②E处干燥管中盛放的药品是碱石灰,其作用是
③若样品质量为w g,反应后C、D装置增加的质量分别为m1g、m2g,则混合物中Na2CO3·10H2O的质量分数为
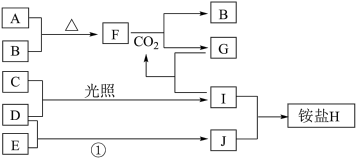
请回答下列问题:
(1)E和J的化学式分别是
(2)写出F和CO2反应的化学方程式并用单线桥法表示电子转移的情况:
(3)将少量单质C通入盛有淀粉碘化钾溶液的试管中,溶液变蓝色,该反应的离子方程式为
(4)标况下3.36 L气体B与A完全反应,转移电子的数目为
【知识点】 无机综合推断 根据物质性质进行元素种类推断解读
试卷分析
试卷题型(共 35题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 胶体的制备 电解质、非电解质概念 铁与非金属单质反应 | |
| 2 | 0.85 | 元素金属性与非金属性递变规律的理解及应用 元素非金属性强弱的比较方法 微粒半径大小的比较方法 根据物质性质进行元素种类推断 | |
| 3 | 0.65 | 溴、碘的性质 萃取和分液 | |
| 4 | 0.85 | 氯水 氯水的成分及检验 氯水的性质 新制氯水与久置氯水的区别 | |
| 5 | 0.85 | 元素周期表结构 | |
| 6 | 0.65 | 阿伏加德罗常数的求算 根据n=N/NA的相关计算 根据N=m·NA/M的相关推算 | |
| 7 | 0.65 | 决定物质体积大小的微观因素 阿伏加德罗定律及其推论 | |
| 8 | 0.65 | 氧化还原反应的几组概念 氧化还原反应有关计算 电子转移计算 | |
| 9 | 0.65 | 元素周期律、元素周期表的推断 根据原子结构进行元素种类推断 具有相同结构的多种离子的性质相关分析及判断 | |
| 10 | 0.85 | 漂白粉和漂粉精 过氧化钠的物理性质、组成、结构及用途 碳酸钠的俗称、物理性质及用途 碳酸氢钠的俗称、物理性质及用途 | |
| 11 | 0.94 | 氧化还原反应基本概念 氧化还原反应的规律 | |
| 12 | 0.85 | 化学物质的分类方法 | |
| 13 | 0.65 | 过氧化钠的物理性质、组成、结构及用途 | |
| 14 | 0.85 | 几种铁的氧化物的物理性质及用途 几种铁的氧化物的化学性质 铁盐的检验 | |
| 15 | 0.65 | 无机物质的分类 | |
| 16 | 0.65 | 物质的量有关计算 氧化还原反应的规律 氯气与还原性化合物的反应 铁的氧化物 | |
| 17 | 0.85 | 原子相关微粒的数值与元素性质的关系 原子中相关数值及其之间的相互关系 | |
| 18 | 0.85 | 无机物质的分类 | |
| 19 | 0.65 | 同主族元素性质递变规律理解及应用 原子序数与元素在周期表中的位置的关系分析及利用 | |
| 20 | 0.85 | 配制一定物质的量浓度的溶液实验的误差分析 | |
| 21 | 0.65 | 分散系概念 | |
| 22 | 0.4 | 摩尔质量的概念 阿伏加德罗定律及其推论 | |
| 23 | 0.65 | 无机物质的分类 物质结构与性质综合考查 | |
| 24 | 0.65 | 原子中相关数值及其之间的相互关系 元素、核素、同位素 | |
| 25 | 0.65 | 限定条件下的离子共存 | |
| 26 | 0.65 | 电解质与非电解质 | |
| 27 | 0.65 | 限定条件下的离子共存 | |
| 28 | 0.65 | 铝盐与强碱溶液反应 偏铝酸钠与盐酸的反应 | |
| 29 | 0.94 | 树状分类法 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系 非电解质、电解质物质类别判断 | |
| 30 | 0.85 | 摩尔质量的概念 摩尔质量与相对原子质量区别与联系 | |
| 二、填空题 | |||
| 31 | 0.65 | 氧化还原反应在生活、生产中的应用 基于氧化还原反应守恒规律的计算 亚铁盐 | |
| 三、解答题 | |||
| 32 | 0.65 | 元素金属性、非金属性强弱探究实验 常用仪器及使用 化学实验基础操作 | 实验探究题 |
| 33 | 0.65 | 铁与水蒸气的反应 物质性质的探究 综合实验设计与评价 | 实验探究题 |
| 34 | 0.4 | 碳酸氢钠的不稳定性 碳酸钠、碳酸氢钠混合物的有关求算 探究物质组成或测量物质的含量 | 实验探究题 |
| 35 | 0.65 | 无机综合推断 根据物质性质进行元素种类推断 | 无机推断题 |



