黑龙江省肇东市第四中学2022-2023学年高一上学期期末考试化学试题
黑龙江
高一
期末
2023-01-06
143次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、化学反应原理、物质结构与性质、初中衔接知识点、化学实验基础
一、单选题 添加题型下试题
| A.烧碱、纯碱均属于碱 |
| B.漂白粉与漂白液均为混合物 |
| C.H2SO4、NaOH、BaSO4均属于强电解质 |
| D.HClO、HNO3均具有氧化性,都是氧化性酸 |
 。下列说法正确的是
。下列说法正确的是| A.14C和14N互为同位素 |
| B.1mol14N2的中子数为14NA |
| C.14C与C60互为同素异形体 |
D.当14g核素14N完全被轰击时,吸收中子(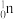 )的质量约为6.02 )的质量约为6.02 1023g 1023g |
A.在加入 粉能产生 粉能产生 的溶液中: 的溶液中: 、 、 、 、 、 、 |
B.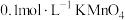 溶液: 溶液: 、 、 、 、 、 、 |
C.某无色透明溶液: 、 、 、 、 、 、 |
D.在碱性溶液中: 、 、 、 、 、 、 |
【知识点】 限定条件下的离子共存解读
| A.Zn→ZnSO4 | B.CuO→CuCl2 |
| C.CaCO3→CO2 | D.NaOH→Na2SO4 |
【知识点】 酸、碱、盐、氧化物的概念及其相互联系解读
A. 、Cl﹣ 、Cl﹣ | B. 、Cl﹣ 、Cl﹣ | C. 、 、 | D.OH﹣、 |
【知识点】 离子共存
| A.标准状况下22.4LCO和CO2的混合气体中含碳原子数为NA |
| B.1 L 1 mol·L-1HCl溶液中含有HCl分子为NA个 |
| C.标准状况下,2.24 L水中约含有NA个氧原子 |
| D.28 g N2和CO的混合气体,所占的体积为22.4 L |
 气体,另一个盛有
气体,另一个盛有 和CO的混合气体。在同温同压下,两容器内的气体一定相同的物理量有几项:
和CO的混合气体。在同温同压下,两容器内的气体一定相同的物理量有几项:(1)分子数 (2)原子数 (3)质量 (4)中子数 (5)密度 (6)气体摩尔体积
| A.4项 | B.5项 | C.6项 | D.3项 |
【知识点】 阿伏加德罗定律及其推论解读 阿伏加德罗定律的应用解读
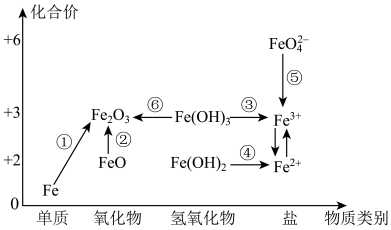
| A.铁与高温水蒸气的反应可实现上述①转化 |
| B.加热Fe(OH)3发生转化⑥,Fe2O3加水溶解可转化为Fe(OH)3 |
| C.维生素C能将Fe3+转化为Fe2+,该过程中维生素C作还原剂 |
| D.FeO是一种黑色粉末,不稳定,在空气中受热,迅速被氧化成Fe2O3 |
【知识点】 铁 铁与水蒸气的反应解读 与“铁三角”有关的推断解读
A.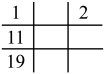 | B. | C.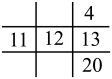 | D.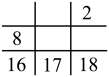 |
【知识点】 元素周期表结构分析解读 元素周期表提供的元素信息解读
| A.温度相同、体积相同的O2(g)和N2(g)分子数相同 |
| B.同温等压下,SO2气体与CO2气体的密度之比等于16∶11 |
| C.温度和容积相同的两气罐中分别盛有5 mol O2(g)和2 mol N2(g),两容器中的压强之比等于5∶2 |
| D.同温等压条件下,5 mol O2(g)和2 mol H2(g)的体积之比等于5∶2 |
【知识点】 阿伏加德罗定律 阿伏加德罗定律及其推论解读 阿伏加德罗定律的应用解读
A.3Fe+4H2O(g) Fe3O4+4H2 Fe3O4+4H2 | B.2H2O 2H2↑+O2↑ 2H2↑+O2↑ |
| C.2Na2O2+2H2O═4NaOH+O2↑ | D.2F2+2H2O═4HF+O2 |
【知识点】 氧化还原反应的几组概念解读
| A.1 mol任何气体所占的体积都约是22.4 L |
| B.1 mol气体在非标准状况下的体积不可能是22.4 L |
| C.气体摩尔体积不仅适用于纯气体,也适用于混合气体 |
| D.0.3 mol氢气与0.7 mol 氧气的混合气体的体积约是22.4 L |
A.Fe2O3 Fe Fe FeCl3 FeCl3 | B.H2O2 H2 H2 H2O H2O |
C.CaCl2溶液 CaCO3 CaCO3 CO2 CO2 | D.CuSO4溶液 Cu Cu CuO CuO |
 ]可用于治疗高磷酸盐血症,其制备的化学方程式为
]可用于治疗高磷酸盐血症,其制备的化学方程式为 。下列表示相关微粒的化学用语正确的是
。下列表示相关微粒的化学用语正确的是| A.镧(57La)为第VIIA族元素 |
B.CO2的球棍模型为 |
C.NaCl的形成过程: |
D.Cl-的结构示意图: |
| A.质子数 | B.核电荷数 | C.核外电子数 | D.离子所带的电荷数 |
A.碳酸钙溶于稀盐酸中: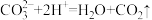 |
B.氧化镁与稀硝酸反应: |
C.硫酸镁溶液与氢氯化钡溶液混合: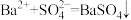 |
D.澄清的石灰水与盐酸的反应: |
【知识点】 离子方程式的正误判断解读
A.在反应 中, 中, 作还原剂,在其他反应中,反应物中的 作还原剂,在其他反应中,反应物中的 一定也作还原剂 一定也作还原剂 |
B.在反应 中,氧化性: 中,氧化性: |
| C.金属活动性顺序中,排在前面的金属阳离子的氧化性强于排在后面的金属阳离子的氧化性 |
D. 中硫元素的化合价是 中硫元素的化合价是 价,处于硫的最高价,因此 价,处于硫的最高价,因此 的氧化性一定很强 的氧化性一定很强 |
【知识点】 氧化性、还原性强弱的比较解读 氧化还原反应的规律解读
①过滤 ②蒸发 ③溶解 ④向容量瓶中转移液体
| A.①和② | B.①和③ | C.③和④ | D.①和④ |
| A.漂白粉是化合物 | B.水玻璃是纯净物 |
| C.盐酸是电解质 | D.纯碱不属于碱 |
| A.Cu |
| B.H2 |
| C.Mg |
| D.不能确定 |

| A.最简单气态氢化物的热稳定性:R>Q | B.最高价氧化物对应水化物的酸性:W<Q |
| C.原子半径:T>Q>R | D.T的最高价氧化物水化物具有两性 |
| A.在已知碱金属元素中具有最大的原子半径 |
| B.在空气中燃烧时生成氧化物Fr2O |
| C.最高价氧化物对应的水化物是强碱 |
| D.其单质的熔点比金属钠的熔点低 |
【知识点】 同主族元素性质递变规律
| A.1 mol二氧化碳中含有1 mol碳和2 mol氧 |
| B.0.012 kg12C中含有的碳原子数约为6.02×1023 |
| C.1 mol甲烷的质量为16 g·mol-1 |
| D.2 g氢气所含的原子数目为NA |
【知识点】 结合物质结构基础知识与NA相关推算解读
二、解答题 添加题型下试题

(1)甲的化学式为
(2)写出甲和D反应的化学方程式
(3)为检验化合物甲中元素的化合价,需要用到的药品有___________。
| A.稀硫酸 | B.盐酸 | C.硫氰化钾溶液 | D.高锰酸钾溶液 |
(4)为测定A和乙高温反应后所得固体中化合物甲的质量分数。取反应后所得固体并设计以下实验:

化合物甲的质量分数为
【知识点】 无机综合推断 物质含量的测定 探究物质组成或测量物质的含量解读
a.稀H2SO4b.盐酸 c.CO2d.氨水 e.NaOH
(2)已知X是某金属单质,X、A、B、C含同一种元素,可发生如下转化:
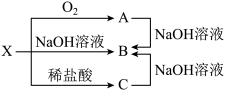
①写出下列物质的化学式:X:
②写出以下反应的离子方程式:A→B:
试卷分析
试卷题型(共 27题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系 硝酸的强氧化性 强电解质和弱电解质的判断 | |
| 2 | 0.65 | 原子的基本构成 原子中相关数值及其之间的相互关系 元素、核素、同位素 几组常见同素异形体 | |
| 3 | 0.65 | 限定条件下的离子共存 | |
| 4 | 0.65 | 酸、碱、盐、氧化物的概念及其相互联系 | |
| 5 | 0.85 | 离子共存 | |
| 6 | 0.85 | 阿伏加德罗常数的求算 阿伏加德罗常数的应用 结合气体物质与NA相关推算 结合物质结构基础知识与NA相关推算 | |
| 7 | 0.65 | 阿伏加德罗定律及其推论 阿伏加德罗定律的应用 | |
| 8 | 0.65 | 铁 铁与水蒸气的反应 与“铁三角”有关的推断 | |
| 9 | 0.94 | 电解质的电离 电离的定义 | |
| 10 | 0.65 | 元素周期表结构分析 元素周期表提供的元素信息 | |
| 11 | 0.65 | 阿伏加德罗定律 阿伏加德罗定律及其推论 阿伏加德罗定律的应用 | |
| 12 | 0.85 | 氧化还原反应的几组概念 | |
| 13 | 0.85 | 阿伏加德罗定律 22.4L/mol适用条件 阿伏加德罗定律及其推论 | |
| 14 | 0.65 | 物质的转化 身边的化学物质 | |
| 15 | 0.65 | 原子结构示意图、离子结构示意图 有机物的结构式、结构简式、比例模型、球棍模型、最简式 共价型分子结构式、电子式 | |
| 16 | 0.94 | 原子相关微粒的数值与元素性质的关系 原子的基本构成 原子中相关数值及其之间的相互关系 | |
| 17 | 0.85 | 离子方程式的正误判断 | |
| 18 | 0.65 | 氧化性、还原性强弱的比较 氧化还原反应的规律 | |
| 19 | 0.94 | 仪器使用与实验安全 常用仪器及使用 化学实验基础操作 配制一定物质的量浓度的溶液实验的仪器 | |
| 20 | 0.94 | 树状分类法 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系 非电解质、电解质物质类别判断 | |
| 21 | 0.65 | 离子反应在混合物分离、除杂中的应用 氧化性、还原性强弱的比较 氧化还原反应的规律 | |
| 22 | 0.65 | 金属与非金属在周期表中位置及其性质递变的规律 结合物质计算的元素周期律、元素周期表相关推断 | |
| 23 | 0.85 | 碳酸氢钠与酸反应 碳酸氢钠与碱反应 | |
| 24 | 0.65 | 同主族元素性质递变规律 | |
| 25 | 0.65 | 结合物质结构基础知识与NA相关推算 | |
| 二、解答题 | |||
| 26 | 0.65 | 无机综合推断 物质含量的测定 探究物质组成或测量物质的含量 | 无机推断题 |
| 27 | 0.85 | 无机综合推断 氢氧化铝 铝与强碱溶液反应 氧化铝与碱溶液反应 | 无机推断题 |



