山西省陵川县平城中学2021-2022学年高一上学期第一次月考化学试题
山西
高一
阶段练习
2021-10-28
182次
整体难度:
适中
考查范围:
认识化学科学、初中衔接知识点、化学实验基础、化学与STSE、常见无机物及其应用
一、单选题 添加题型下试题
A.Fe2O3 Fe Fe FeCl3 FeCl3 | B.H2O2 H2 H2 H2O H2O |
C.CaCl2溶液 CaCO3 CaCO3 CO2 CO2 | D.CuSO4溶液 Cu Cu CuO CuO |
| A.月波成露露成霜,借与南枝作淡妆 |
| B.春蚕到死丝方尽,蜡炬成灰泪始干 |
| C.宝剑锋从磨砺出,梅花香自苦寒来 |
| D.莫道雪融便无迹,雪融成水水成冰 |
【知识点】 物质的转化
①金属氧化物也可以是酸性氧化物;②非金属氧化物一定是酸性氧化物;③碱性氧化物一定是金属氧化物;④能与酸反应生成盐和水的氧化物一定是碱性氧化物;⑤能与碱反应生成盐和水的氧化物一定是酸性氧化物
| A.③④⑤ | B.①②③ | C.②④⑤ | D.①②③④⑤ |
| A.利用丁达尔效应可以区分溶液和胶体 |
| B.胶体的分散质粒子直径大于 1 nm 小于 100 nm,能通过滤纸 |
| C.PM2.5 是指大气中直径接近于 2.5×10-6 m(1 m=109 nm)的颗粒物,也称可吸入颗粒物, 这些细颗粒物分散在空气中形成的分散系是胶体 |
| D.溶液的分散质粒子直径小于 1 nm,能通过滤纸 |
| A.淀粉胶体中含有少量的氯化钠,可用适量硝酸银溶液除去 |
| B.纳米材料粒子直径一般从几纳米到几十纳米(1 nm=10-9m),但是纳米材料不属于胶体 |
| C.氢氧化铁胶体中逐滴加入过量的稀硫酸溶液,开始产生红褐色沉淀 ,最后沉淀溶解 |
| D.水泥厂,冶金厂用高压电除去烟尘,是因为烟尘微粒带电荷 |
【知识点】 分散系概念 胶体的性质和应用解读 物质分离、提纯的常见化学方法解读


| A.掐丝:粘铜丝→烧焊→硫酸煮→清水洗 | B.点蓝:将铅丹、硼酸盐等化合熔制后填色 |
| C.烧蓝:高温焙烧、三填三烧 | D.打磨:用金刚砂、磨刀石、椴木炭三次水磨 |
二、未知 添加题型下试题
三、单选题 添加题型下试题
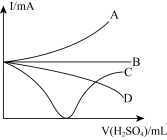
| A.A | B.B | C.C | D.D |
| 纯净物 | 混合物 | 电解质 | 非电解质 | |
| A | 浓盐酸 | 天然气 | 硫酸 | 干冰 |
| B | 氢氧化钡 | 蔗糖溶液 | 硫酸钡 | 三氧化硫 |
| C | 胆矾 | 石灰水 | KOH | 碳酸钙 |
| D | 硫酸 | 铝合金 | 氯化钠 | 氢气 |
| A.A | B.B | C.C | D.D |
四、多选题 添加题型下试题
A.强碱性溶液中:K+、Mg2+、Cl-、 |
B.室温下,能使紫色石蕊溶液变红的溶液中:Na+、Fe3+、 、 、 |
C.有Ca2+的溶液中:Na+、K+、 、Cl- 、Cl- |
D.在无色透明的溶液中:K+、Cu2+、 、 、 、 、 |
【知识点】 离子反应的发生条件解读 限定条件下的离子共存解读
五、单选题 添加题型下试题
| A.氢氧化钡溶液与硫酸的反应:OH-+H+=H2O |
| B.澄清的石灰水与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H2O |
| C.铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag |
| D.碳酸钙溶于稀盐酸中:CaCO3+2H+=Ca2++H2O+CO2↑ |
【知识点】 离子反应的发生及书写 离子方程式的正误判断解读
A.向某溶液中加入稀盐酸产生无色气体,将气体通入澄清石灰水中,澄清石灰水变浑浊,则原溶液中一定有CO |
| B.向某溶液中加入氯化钡溶液有白色沉淀产生,再加足量稀硝酸,沉淀不消失,则原溶液中一定有 Ag+ |
C.向某溶液中先加入足量盐酸,没有明显现象,再加入BaCl2溶液;产生白色沉淀,则原溶液中一定有SO |
| D.向某溶液中加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,则原溶液一定有Ba2+ |
| A.野火烧不尽,春风吹又生 |
| B.春蚕到死丝方尽,蜡炬成灰泪始干 |
| C.明月松间照,清泉石上流 |
| D.爆竹声中一岁除,春风送暖入屠苏 |
【知识点】 氧化还原反应基本概念
| A.Zn+2HCl=ZnCl2+H2↑ | B.2H2S+SO2=3S↓+2H2O |
C.H2+CuO Cu+H2O Cu+H2O | D.2H2O 2H2↑+O2↑ 2H2↑+O2↑ |
【知识点】 氧化还原反应的几组概念解读
| A.BaCl2溶液中滴加稀硫酸 | B.盐酸和氧化铁反应 |
| C.铁片放入CuSO4溶液中 | D.氢气还原CuO |
【知识点】 离子反应概念解读 氧化还原反应基本概念
A. | B.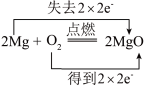 |
C. | D.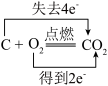 |

| A.1 个 | B.2 个 | C.3 个 | D.4 个 |
【知识点】 氧化还原反应基本概念 含硫化合物之间的转化解读
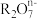 与S2-能在酸性溶液中发生反应:
与S2-能在酸性溶液中发生反应: 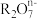 +3S2-+14H+=2R3++3S↓+7H2O,则
+3S2-+14H+=2R3++3S↓+7H2O,则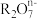 中R化合价为
中R化合价为| A.+4 | B.+5 | C.+6 | D.+7 |
【知识点】 氧化还原反应的规律解读 基于氧化还原反应守恒规律的计算解读
 K2MnO4+MnO2+O2↑,有关该反应,下列说法错误的是( )
K2MnO4+MnO2+O2↑,有关该反应,下列说法错误的是( )| A.氧化剂和还原剂都是KMnO4 |
| B.该反应的还原产物只有MnO2 |
| C.该反应的氧化产物是O2 |
| D.KMnO4中Mn表现氧化性,O表现还原性 |
【知识点】 氧化还原反应的几组概念解读
Ce4++Fe2+=Fe3++Ce3+
Sn2++2Fe3+=2Fe2++Sn4+
由此可以确定Fe2+、Ce3+、Sn2+三种离子的还原性由强到弱的顺序
| A.Sn2+、Fe2+、Ce3+ | B.Sn2+、Ce3+、Fe2+ |
| C.Ce3+、Fe2+、Sn2+ | D.Fe2+、Sn2+、Ce3+ |
【知识点】 氧化性、还原性强弱的比较解读
六、填空题 添加题型下试题
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将
的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将 还原为 N2,其化学方程式为 10Al+6NaNO3+ 4NaOH=10NaAlO2+3N2↑+2H2O。
还原为 N2,其化学方程式为 10Al+6NaNO3+ 4NaOH=10NaAlO2+3N2↑+2H2O。请回答下列问题:
(1)上述反应中,
(2)用双线桥法表示反应中电子转移的方向和数目:
(1)在汽车尾气系统中装置催化转化器,可有效降低 NOx 的排放,当尾气中空气不足时,NOx在催化转化器中被还原成 N2 排出。 写出 NO 被 CO 还原的化学方程式:
(2)实验室里迅速制备少量氯气可利用以下反应:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。
①用双线桥法表示出电子转移情况:
②用单线桥法表示出电子转移情况:
③该反应中氧化剂是
七、解答题 添加题型下试题
A、用pH试纸检验溶液,发现溶液呈强酸性;
B、取部分溶液逐滴加入NaOH溶液,使溶液由酸性变为碱性,无沉淀产生;
C、取少量B中的碱性溶液,滴加Na2CO3溶液,有白色沉淀产生。
①根据上述事实确定:该溶液中肯定存在的离子有
②写出C中发生反应的离子方程式
(Ⅱ)按要求写出下列物质间反应的离子反应方程式:
(1)硫酸氢钠与碳酸氢钠溶液混和
(2)氢氧化镁固体溶于足量盐酸溶液:
【知识点】 离子反应的发生及书写 离子反应的实际应用
八、填空题 添加题型下试题

(1)Ba(OH)2 在水中以离子形式存在的实验证据
(2)A~B 段发生的离子反应是
(3)B 点恰好完全反应,此时溶液中存在的微粒有 H2O、
(4)下列化学反应的实质与 Ba(OH)2 溶液和稀盐酸反应的实质相同的是
A.Ba(OH)2 和H2SO4 B.NaOH 和H2SO4 C.Ba(OH)2 与HNO3
试卷分析
试卷题型(共 24题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 物质的转化 身边的化学物质 | |
| 2 | 0.94 | 物质的转化 | |
| 3 | 0.85 | 化学物质的分类方法 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系 | |
| 4 | 0.94 | 溶液 分散系概念及其分类 胶体的性质和应用 | |
| 5 | 0.94 | 分散系概念 胶体的性质和应用 物质分离、提纯的常见化学方法 | |
| 6 | 0.65 | 物理变化与化学变化 化学科学对人类文明发展的意义 大气污染来源及危害 | |
| 8 | 0.65 | 物质水溶液的导电性 离子反应的实际应用 | |
| 9 | 0.85 | 分类方法的应用 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系 电解质与非电解质 | |
| 11 | 0.85 | 离子反应的发生及书写 离子方程式的正误判断 | |
| 12 | 0.85 | 硫酸根离子的检验 常见阳离子的检验 常见阴离子的检验 | |
| 13 | 0.85 | 氧化还原反应基本概念 | |
| 14 | 0.65 | 氧化还原反应的几组概念 | |
| 15 | 0.85 | 离子反应概念 氧化还原反应基本概念 | |
| 16 | 0.65 | 氧化还原反应定义、本质及特征 单线桥、双线桥分析氧化还原反应 氧化还原反应有关计算 氧化还原反应的规律 | |
| 17 | 0.94 | 氧化还原反应基本概念 含硫化合物之间的转化 | |
| 18 | 0.85 | 氧化还原反应的规律 基于氧化还原反应守恒规律的计算 | |
| 19 | 0.65 | 氧化还原反应的几组概念 | |
| 20 | 0.85 | 氧化性、还原性强弱的比较 | |
| 二、未知 | |||
| 7 | 0.85 | 物质的转化 | 未知 |
| 三、多选题 | |||
| 10 | 0.65 | 离子反应的发生条件 限定条件下的离子共存 | |
| 四、填空题 | |||
| 21 | 0.85 | 氧化还原反应的几组概念 氧化还原反应定义、本质及特征 单线桥、双线桥分析氧化还原反应 | |
| 22 | 0.85 | 氧化还原反应定义、本质及特征 单线桥、双线桥分析氧化还原反应 氧化还原反应方程式的配平 | |
| 24 | 0.85 | 电解质的电离 物质水溶液的导电性 离子方程式的书写 | |
| 五、解答题 | |||
| 23 | 0.65 | 离子反应的发生及书写 离子反应的实际应用 | 无机推断题 |




