2015-2016学年福建省福州八中高一上学期期末化学试卷
福建
高一
期末
2017-07-27
393次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、化学与STSE、物质结构与性质、化学实验基础
一、单选题 添加题型下试题
| A.混合物:空气、矿泉水、水银 |
| B.酸性氧化物:、CO2、SO2、CO |
| C.盐:醋酸钠、氯化铵、纯碱 |
| D.弱电解质:CH3COOH、H2O、NH3 |
| A.由于电流的作用,酸、碱、盐溶于水发生电离 |
| B.胶体的分散质粒子直径小于l00nm但大于1nm |
| C.存在自由移动的离子是电解质溶液导电的原因 |
| D.醋酸溶液中存在H+、CH3COOH、CH3COO﹣等微粒,故醋酸是弱电解质 |
【知识点】 电解质
| A.焰色反应呈黄色,加硝酸酸化的AgNO3溶液有白色沉淀 |
| B.焰色反应呈紫色,加盐酸酸化的AgNO3溶液有白色沉淀 |
| C.焰色反应呈黄色,加盐酸酸化的AgNO3溶液有白色沉淀 |
| D.焰色反应呈紫色,加硝酸酸化的AgNO3溶液有白色沉淀 |
| A.H2在Cl2中燃烧会产生苍白色火焰 |
| B.氯水用于漂白表现了HClO的强氧化性 |
| C.漂白粉是混合物,其有效成分是氯化钙 |
| D.漂白粉应密封保存 |
【知识点】 卤素及其化合物
| A.13C与15N有相同的中子数 | B.13C与12C是同一种核素 |
| C.15N与14N互为同位素 | D.15N的相对原子质量为15 |
【知识点】 元素周期表 元素周期律
| A.Fe2+、Fe3+ | B.Fe2+、Cu2+ |
| C.Fe3+、Cu2+ | D.Cu+、Cu2+ |
【知识点】 Fe、Cu及相关离子的反应解读
①Cl2-制消毒剂 ②AgBr-制胶卷,感光纸 ③AgI-人工降雨 ④碘-预防甲状腺肿大 ⑤淀粉-检验I2的存在 ⑥NaClO-漂白纺织物
| A.②③④⑤⑥ | B.①②③④⑤ | C.②③④⑤ | D.全部 |
| A.K+、CH3COO﹣、Na+、Cl﹣ |
| B.Na+、NO3﹣、NH4+、SO42﹣ |
| C.Fe2+、NO3﹣、Na+、SO42﹣ |
| D.Na+、HCO3﹣、Cl﹣、SO42﹣ |
【知识点】 离子共存
| A.都有H2O生成 |
| B.都有H2生成 |
| C.反应后铝元素主要以AlO2-的形式存在 |
| D.反应后铝元素主要以Al3+的形式存在 |
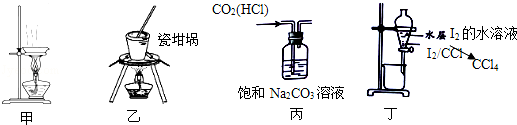
| A.甲用装置所示仪器可以蒸发、结晶制取粗盐 |
| B.用装置乙加热分离碘单质和氯化钠的混合固体 |
| C.用装置丙除去CO2中的少量HCl |
| D.用装置丁进行萃取、分液 |
【知识点】 化学实验基础
| A.氯气与水反应:Cl2+H2O═Cl﹣+ClO﹣+2H+ |
| B.铁与盐酸反应:2Fe+6H+═3H2↑+2Fe3+ |
| C.硫酸与氢氧化钡混合:2H++SO42﹣+Ba2++2OH¯═Ba SO4↓+2 H2O |
| D.向AlCl3溶液中滴入过量NaOH溶液:Al3++3OH﹣=Al(OH)3↓ |
【知识点】 离子反应的发生及书写
| A.硝酸和碳酸氢钠溶液的反应 | B.稀硫酸和碳酸钾溶液的反应 |
| C.醋酸和碳酸钠溶液的反应 | D.盐酸和碳酸钡溶液的反应 |
【知识点】 离子反应的发生及书写
| 选项 | 待提纯的物质 | 选用的试剂 | 操作方法 |
| A | NaOH(Na2CO3) | 盐酸 | ﹣ |
| B | Na2CO3粉末(NaHCO3) | ﹣ | 加热 |
| C | Fe (Al) | 稀硫酸 | 过滤 |
| D | NaHCO3溶液(Na2CO3) | CaCl2溶液 | 过滤 |
| A.A | B.B | C.C | D.D |
【知识点】 化学实验基础
| A.⑤ | B.④ | C.③ | D.② |
【知识点】 碳酸钠与碳酸氢钠的相互转化解读 镁的结构与化学性质解读
| A.NaOH是氧化产物 |
| B.当1molNaH发生反应时,该反应转移电子的物质的量为2mol |
| C.NaH为还原剂 |
| D.H2O既是还原剂又是氧化剂 |
【知识点】 氧化还原反应基本概念
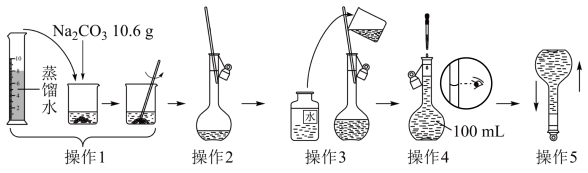
| A.所配制的Na2CO3溶液的物质的量浓度为1.0 mol · L-1 |
| B.操作2是将溶解并放置至室温的Na2CO3溶液转移到容量瓶中 |
| C.操作4如果仰视,会使配得溶液的浓度偏低 |
| D.操作5中,定容摇匀后发现液面低于刻度线,继续加水至液面与刻度线相切 |
| 离子 | Na+ | Al3+ | Cl﹣ | X |
| 个数 | 2a | a | a | b |
| A.NO3﹣、2a | B.SO42﹣、2a | C.OH﹣、2a | D.SO42﹣、4a |
【知识点】 离子共存
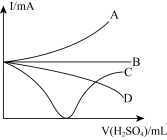
| A.A | B.B | C.C | D.D |
二、填空题 添加题型下试题
(1)医疗上,用碳酸氢钠治疗胃酸过多的原理(用离子方程式表示)
(2)氯碱工业的反应原理(又为氯气的工业制法)(用化学方程式表示):
(3)用过氧化钠作为呼吸面具的供氧剂与二氧化碳反应的原理(用化学方程式表示)
(4)写出用铜与氯化铁反应印刷电路板的原理(用离子方程式表示)
该反应中
(5)配平下列反应的方程式,并标出电子转移的方向和数目
【知识点】 氧化还原反应有关计算 钠及其化合物
三、解答题 添加题型下试题
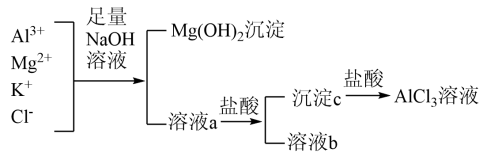
(1)写出混合物中加入足量氢氧化钠溶液时,溶液中发生反应的离子方程式:
(2)氢氧化钠溶液能否用氨水代替,为什么?
(3)在溶液a中加入盐酸时需控制盐酸的量,为什么?
【知识点】 含氧化铝的混合物的提纯解读 物质分离、提纯综合应用解读
四、单选题 添加题型下试题
①(NH4)2CO3 ②Al(OH)3 ③NaHCO3 ④Al2O3 ⑤Fe(NO3)2
| A.①②③④ | B.②③④ | C.②④⑤ | D.全部 |
| A.+1 | B.+2 |
| C.+4 | D.+5 |
| A.10.0 mol/L | B.15 mol/L | C.1.2 mol/L | D.0.9 mol/L |
【知识点】 钠及其化合物
| A.Cl2 | B.KMnO4 | C.FeCl3 | D.HCl |
【知识点】 氧化性、还原性强弱的比较解读 氧化还原反应的规律解读
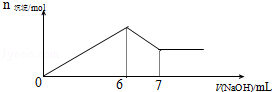
| A.2:1 | B.2:3 | C.6:1 | D.3: 1 |
【知识点】 化学计量
五、解答题 添加题型下试题
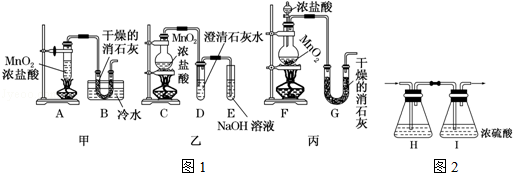
(1)请对上述丙装置的缺点进行评价:
(2)请从甲、乙、丙各套装置中选取合理的部分,按气体从左至右的流向组成一套较合理的装置
(3)部分学生认为上述组装装置仍存在缺点,他们指出在前两个仪器之间应增加如图2所示装置,你认为H洗气瓶中所盛液体是
已知:3Fe+4H2O
 Fe3O4+4H2↑
Fe3O4+4H2↑Fe3O4+8H+═2Fe3++Fe2++4H2O
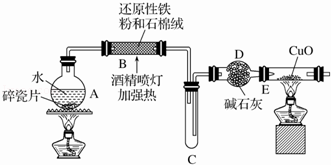
探究一 设计如图所示装置进行“铁与水反应”的实验,
(1)反应前A中投放碎瓷片的目的是
(2)装置E中发生反应的方程式为
探究二 设计如下实验方案确定反应后硬质玻璃管中黑色固体的成分,
待硬质玻璃管B冷却后,取少许其中的固体物质溶于盐酸后,将所得溶液分成两份,
(3)一份滴加几滴KSCN溶液,若溶液变血红色,推断硬质玻璃管B中固体物质的成分为
①一定有Fe3O4,可能有单质铁 ②一定有Fe
③只有Fe3O4 ④只有Fe
(4)另一份加入
探究三 设计如下流程测定反应后硬质玻璃管B中固体含铁元素的质量分数,
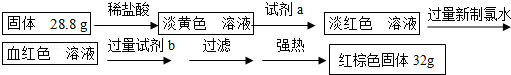
(5)写出加入过量氯水时反应的离子方程式:
(6)试剂b的化学式是
(7)计算反应后B装置中铁元素的质量分数为
试卷分析
试卷题型(共 29题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 分类方法的应用 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系 | |
| 2 | 0.64 | 电解质 | |
| 3 | 0.85 | 氯离子的检验 焰色试验 | |
| 4 | 0.64 | 卤素及其化合物 | |
| 5 | 0.94 | 铁 人体健康物质基础 | |
| 6 | 0.64 | 元素周期表 元素周期律 | |
| 7 | 0.65 | Fe、Cu及相关离子的反应 | |
| 8 | 0.85 | 氯气的用途 氯气与碱溶液反应 其他含卤化合物 碘与淀粉的显色反应 | |
| 9 | 0.64 | 离子共存 | |
| 10 | 0.85 | 铝 氧化铝 | |
| 11 | 0.85 | 氯水的成分及检验 氯水的性质 | |
| 12 | 0.64 | 化学实验基础 | |
| 13 | 0.64 | 离子反应的发生及书写 | |
| 14 | 0.64 | 离子反应的发生及书写 | |
| 15 | 0.64 | 化学实验基础 | |
| 16 | 0.65 | 碳酸钠与碳酸氢钠的相互转化 镁的结构与化学性质 | |
| 17 | 0.64 | 氧化还原反应基本概念 | |
| 18 | 0.85 | 一定物质的量浓度的溶液的配制 配制一定物质的量浓度的溶液的步骤、操作 配制一定物质的量浓度的溶液实验的误差分析 配制一定物质的量浓度的溶液实验的仪器 | |
| 19 | 0.4 | 离子共存 | |
| 20 | 0.65 | 物质水溶液的导电性 离子反应的实际应用 | |
| 23 | 0.65 | 碳酸氢钠 氧化铝 氢氧化铝 | |
| 24 | 0.85 | 氧化还原反应有关计算 与氧化剂、还原剂有关的计算 基于氧化还原反应守恒规律的计算 | |
| 25 | 0.4 | 钠及其化合物 | |
| 26 | 0.65 | 氧化性、还原性强弱的比较 氧化还原反应的规律 | |
| 27 | 0.64 | 化学计量 | |
| 二、填空题 | |||
| 21 | 0.64 | 氧化还原反应有关计算 钠及其化合物 | |
| 三、解答题 | |||
| 22 | 0.65 | 含氧化铝的混合物的提纯 物质分离、提纯综合应用 | 实验探究题 |
| 28 | 0.4 | 化学实验基础 卤素及其化合物 | 实验探究题 |
| 29 | 0.4 | Fe2+的鉴别及其应用 铁盐的检验 探究物质组成或测量物质的含量 化学实验探究 | 实验探究题 |