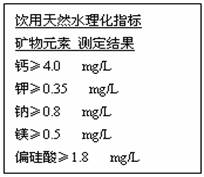
2014-2015福建省闽清高中等四校高一上学期期中联考化学试卷
福建
高一
期中
2017-07-26
393次
整体难度:
适中
考查范围:
化学与STSE、初中衔接知识点、认识化学科学、物质结构与性质、常见无机物及其应用、化学实验基础
一、单选题 添加题型下试题
| A.生石灰、白磷、熟石灰 | B.空气、氮气、胆矾 |
| C.干冰、铁、氯化氢 | D.烧碱、水银、碘酒 |
【知识点】 物质的分类
| A.分散质粒子直径的大小 | B.是否有丁达尔效应 |
| C.是否均一、稳定、透明 | D.能否透过滤纸 |
【知识点】 分散系
| A.H2、D2、T2互为同位素 |
| B.金属氧化物均为碱性氧化物 |
| C.质量数为131,中子数为78的碘原子常用于核反应堆的燃料棒。其核外电子数为53 |
D.S2-的结构示意图: |
【知识点】 原子的构成
| A.因为NH3的水溶液可以导电,所以NH3是电解质 |
| B.因为Cl2可以使湿润的有色布条褪色,所以Cl2具有漂白性 |
| C.因为液态HCl不导电,所以HCl是非电解质 |
| D.因为氢氧化铁胶体具有吸附性,所以常用于净水 |
| A.分子数 | B.电子数 | C.原子数 | D.中子数 |
【知识点】 化学计量
| A.萃取 | B.蒸馏 | C.蒸发 | D.溶解 |
【知识点】 化学实验基础
| A.18g D2O中含有的氧原子数为NA |
| B.实验室用2mol的浓HCl在加热条件下与足量的MnO2反应,转移的电子数为NA |
| C.22.4L氯化氢溶于水可电离出1molCl- |
| D.由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA |
【知识点】 化学计量
| A.A | B.B | C.C | D.D |
| A.含氧原子个数比为2:3 | B.含硫元素质量比为4:5 |
| C.含氧元素质量比为5:6 | D.含硫原子个数比为1:1 |
| A.“氯碱工业”通过电解饱和食盐水生产氯气和烧碱。 |
| B.通常状况下,干燥的氯气能和Fe反应 |
| C.纯净的H2在Cl2中安静地燃烧,发出苍白色火焰,集气瓶口呈现雾状;光照H2和Cl2的混合气体时,因迅速化合而爆炸 |
| D.新制氯水具有漂白性,久置氯水最终变为稀盐酸 |
【知识点】 卤素及其化合物
| A.石蕊溶液 | B.稀盐酸 | C.稀硫酸 | D.CaCl2溶液 |
【知识点】 化学实验基础
| A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32— |
| B.某溶液与NaOH溶液共热,产生使湿润蓝色石蕊试纸变红气体,说明原溶液中存在NH4+ |
| C.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42— |
| D.可用焰色反应实验检验溶液中是否含有K+ |
【知识点】 化学实验基础
| A.用容量瓶配制一定物质的量浓度的NaOH溶液时,溶解后的溶液要马上转移至容量瓶 |
| B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C.蒸发结晶时当蒸发到剩有少量液体时,停止加热,利用余热将液体蒸干 |
| D.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
【知识点】 化学实验基础
| A.75 mL 2 mol/L的CaCl2 | B.150 mL 3 mol/L的KCl |
| C.150 mL 1 mol/L的NaCl | D.75mL 2 mol/L的NH4Cl |
【知识点】 化学计量
①0.6mol NH3 ②标准状况下22.4L He
③4℃9mL水(ρ=1g/mL) ④19.6g H2SO4
| A.②①③④ | B.①③④② | C.①④③② | D.②③④① |
【知识点】 化学计量
| A.1molH2含有的电子数 | B.通常状况下,22.4LCO2所含的分子数 |
| C.0.012kg12C所含的原子数 | D.1L1mol·L-1的CaCl2溶液所含的Cl-数 |
【知识点】 化学计量
| A.在用托盘天平称量所需NaCl的质量时,左盘放砝码右盘放NaCl |
| B.定容时俯视刻度线 |
| C.转移时,把烧杯和玻璃棒用蒸馏水洗涤并把洗涤液也转移至容量瓶 |
| D.容量瓶中有少量水,转移溶液前将容量瓶烘干 |
【知识点】 仪器使用与实验安全
| A.该溶液的物质的量浓度为1 mol·L—1 |
| B.该溶液中含有35.5 g Na2SO4 |
| C.配制100 mL该溶液需用7.1 g Na2SO4 |
| D.量取100 mL该溶液倒入烧杯中,烧杯中Na+的物质的量为0.1 mol |
【知识点】 化学实验基础
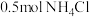 溶液、
溶液、 溶液、
溶液、 溶质作为培养液,若用
溶质作为培养液,若用 和
和 三种物质来配制
三种物质来配制 上述营养液,所需三种盐的物质的量是
上述营养液,所需三种盐的物质的量是A.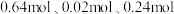 | B.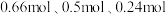 |
C.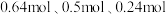 | D. |
二、填空题 添加题型下试题
A萃取分液 B升华 C结晶 D分液 E蒸馏 F过滤
(1)从溴水中提取溴
(2)从含有少量氯化钠的硝酸钾混合液中获得硝酸钾
(3)分离水和汽油的混合物
(4)分离酒精(沸点为78.1℃)和甲苯(沸点为110.6℃)两种互溶液体
【知识点】 化学实验基础
| 检测次数 | 溶液中检测出的物质 |
| 第1次 | KCl、K2SO4、Na2CO3、NaCl |
| 第2次 | KCl、BaCl2、Na2SO4、K2CO3 |
| 第3次 | Na2SO4、KCl、K2CO3、NaCl |
查阅资料:Ag2SO4、CaSO4微溶于水
(1)三次检测中,检测结果肯定不正确的是 。
(2)SO42-、CO32-和Cl-的检测最佳顺序是 。
(3)在上述检测中,若只取一次某溶液:
①检测SO42-时,所用试剂是 。
②检测CO32-时,所加试剂必须过量的原因是 。
③检测Cl-时,请写出其中的一个有关反应化学方程式是 。
三、解答题 添加题型下试题
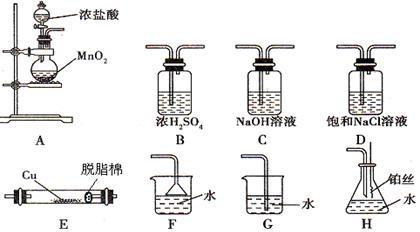
(1)若实验室制取纯净、干燥的Cl2,并进行检验其和铜的反应。所选装置的顺序依次为(从左向右)
(2)A中发生反应的化学方程式为
(3)实验过程中,先点燃
(二)化学反应的产物往往跟反应条件密切相关,下图中:

①为氯气发生装置;
②的试管里盛有15 mL 4mol/L NaOH溶液,并置于水浴中;
③的试管里盛有15 mL 0.5mol/LNaOH溶液,并置于冰水浴中;
④为尾气吸收装置。
实验结果表明②中有氯酸钠生成③中有次氯酸钠生成。
(4)比较制取氯酸钾和次氯酸钠的条件,二者的差异是
①
②
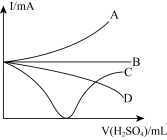
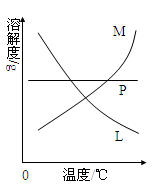
(5)反应完毕经冷却后,②的试管中有大量晶体析出。下图中符合该晶体溶解度曲线的是
(三)(6)若实验中大约需要225mL0.5mol/L的NaOH溶液,至少需要称量NaOH固体
四、计算题 添加题型下试题

(1)氯化钠的摩尔质量____________________
(2)该注射溶液的物质的量浓度为 mol/L。(保留两位有效数字)
(3)某同学配制了1000mL氯化钠注射溶液,为测定所配氯化钠注射液是否达标,取该氯化钠注射液130 mL于烧杯中,然后滴入足量的AgNO3溶液,充分反应后,过滤得到白色沉淀2.87g。请你通过计算判断该氯化钠注射液是否符合上述要求,写出计算过程。
(保留两位有效数字)
【知识点】 化学计量
试卷分析
试卷题型(共 28题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 人体健康物质基础 物质构成的奥秘 | |
| 2 | 0.94 | 四种基本反应类型与氧化还原反应的关系 | |
| 3 | 0.64 | 物质的分类 | |
| 4 | 0.85 | 分散系 | |
| 5 | 0.65 | 原子的构成 | |
| 6 | 0.65 | 次氯酸及其性质 氯气与水的反应 | |
| 7 | 0.64 | 化学计量 | |
| 8 | 0.64 | 化学实验基础 | |
| 9 | 0.64 | 化学计量 | |
| 10 | 0.65 | 物质水溶液的导电性 离子反应的实际应用 | |
| 11 | 0.85 | 物质的量有关计算 根据n=N/NA的相关计算 根据n=m/M的相关计算 根据N=m·NA/M的相关推算 | |
| 12 | 0.64 | 卤素及其化合物 | |
| 13 | 0.64 | 化学计量 阿伏加德罗定律 | |
| 14 | 0.64 | 化学实验基础 | |
| 15 | 0.64 | 化学实验基础 | |
| 16 | 0.64 | 化学实验基础 | |
| 17 | 0.64 | 化学计量 | |
| 18 | 0.64 | 化学计量 | |
| 19 | 0.64 | 化学计量 | |
| 20 | 0.64 | 化学实验基础 仪器使用与实验安全 | |
| 21 | 0.85 | 仪器使用与实验安全 | |
| 22 | 0.85 | 化学实验基础 | |
| 23 | 0.65 | 某溶液与物质的量浓度相关的物理量的判断 物质的量浓度的计算 物质的量浓度计算-与溶质成分有关的计算 | |
| 二、填空题 | |||
| 24 | 0.65 | 电解质与非电解质 电解质的电离 | |
| 25 | 0.64 | 化学实验基础 | |
| 26 | 0.64 | 化学实验基础 离子共存 | |
| 三、解答题 | |||
| 27 | 0.4 | 化学实验基础 卤素及其化合物 仪器使用与实验安全 | 实验探究题 |
| 四、计算题 | |||
| 28 | 0.64 | 化学计量 | |