广东省揭阳岐山中学2022-2023学年高一下学期4月期中考试化学试题
广东
高一
期中
2023-07-15
98次
整体难度:
适中
考查范围:
物质结构与性质、常见无机物及其应用、化学实验基础、认识化学科学、化学反应原理、化学与STSE、初中衔接知识点、有机化学基础
一、单选题 添加题型下试题
| A.硅可用作半导体材料 |
| B.氯气可用于制取漂白粉 |
| C.二氧化硅可用于制造光导纤维 |
| D.浓硫酸可以干燥NH3、H2等 |
| A.少量浓硝酸放在棕色细口瓶中 | B.少量碳酸钙固体放在广口瓶中 |
| C.少量金属钠保存在煤油中 | D.少量氢氧化钠溶液保存在带玻璃塞的试剂瓶中 |
| A.标准状况下,22.4L H2O含有的分子数为1NA |
| B.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02NA |
| C.通常状况下,1NA个CO2分子占有的体积为22.4L |
| D.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为1NA |
A.在无色溶液中:NH 、Cu2+、SO 、Cu2+、SO 、NO 、NO |
B.在含大量Ba2+溶液中:NH 、Na+、SO 、Na+、SO 、OH- 、OH- |
C.在强碱性溶液中:Na+、Ba2+、Cl-、HCO |
D.在强酸性溶液中:K+、Fe2+、Cl-、SO |
| A.Na2S | B.HCl | C.Na2SO4 | D.BaCl2 |
【知识点】 离子键 共价键 共价键与离子键的比较解读 化学键与物质类别关系的判断解读
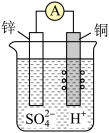
| A.铜极上有气体放出,溶液pH变大 |
| B.锌是正极,铜是负极 |
| C.导线中有电子流动,电子从锌极流到铜极 |
| D.锌极上发生了氧化反应 |
A.盐酸与石灰石反应: |
B.硫酸铜溶液中滴加氢氧化钡溶液: |
C.氢氧化镁和盐酸反应: |
D.氯化铝溶液中加入过量氨水: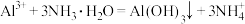 |
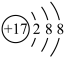 ,关于该粒子的说法正确的是
,关于该粒子的说法正确的是| A.核电荷数为18 | B.核外有3个电子层 |
| C.属于非金属元素的原子 | D.在化学反应中易得1个电子 |
| A.该过程中热能转化为化学能 |
| B.该过程中化学能转化为热能 |
| C.生成物的总能量大于反应物的总能量 |
| D.该反应放热是因为成键过程放出能量 |
| A.氢化物稳定性: HCl>H2S | B.酸性:H2CO3>H2SiO3 |
C.中子数: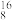 O> O> C C | D.原子半径:P>O |
| A.Fe是氧化剂 | B.CuSO4是还原剂 |
| C.Fe被氧化 | D.CuSO4发生氧化反应 |
【知识点】 氧化还原反应基本概念
A. |
B. |
C.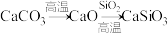 |
D. |
【知识点】 物质的转化 一氧化氮的化学性质解读 含硫化合物之间的转化解读
| A.在日常生活中广泛应用的玻璃、陶瓷、水泥的生产统称为硅酸盐工业 |
| B.废旧电池中的汞、镉、铅等重金属离子会对土壤和水源造成污染 |
| C.太阳能电池可采用硅材料制作,其应用有利于环保节能 |
| D.用福尔马林(35%~40%的甲醛溶液)作防腐剂浸泡海产品很安全 |
| A.向FeCl2溶液中滴加KSCN溶液,溶液显红色 |
| B.KAl(SO4)2·12H2O(明矾)可用于净水 |
| C.NH4Cl与Ca(OH)2混合加热可生成NH3 |
| D.Cu与FeCl3溶液反应可生成CuCl2 |
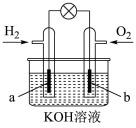
| A.a电极是该电池的正极 |
| B.O2在b电极上发生氧化反应 |
| C.电解质溶液中OH-向正极移动 |
| D.该装置实现了化学能到电能的转化 |
| A.溶液 | B.乳浊液 | C.悬浊液 | D.胶体 |
【知识点】 胶体
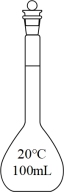
| A.实验需要用到如图所示的容量瓶 |
| B.实验需要使用托盘天平称取3.2gNaOH固体 |
| C.将NaOH固体溶解后可直接转移到容量瓶中并定容 |
| D.定容时,俯视刻度线会造成配制溶液浓度偏低 |
| A.铝块与稀盐酸的反应 | B.Ba(OH)2·8H2O与NH4Cl的反应 |
| C.灼热的炭与CO2的反应 | D.氢氧化钾与硫酸的反应 |
【知识点】 氧化还原反应定义、本质及特征解读 吸热反应和放热反应解读
| A.CH3COOH | B.CH3CH2OH | C.NH4Cl | D.KOH |
| A.品红溶液 | B.澄清石灰水 | C.紫色石蕊试液 | D.氯化钡溶液 |
【知识点】 二氧化硫与二氧化碳的性质区别解读
| A.Na | B.Mg | C.Al | D.Si |
【知识点】 同周期元素性质递变规律
| A.H2CO3 | B.H2SiO3 | C.H3PO4 | D.H2SO4 |
【知识点】 元素非金属性强弱的比较方法解读
| A.CuO → Cu | B.Fe2+ → Fe3+ | C.SO3 → H2SO4 | D.CO → CO2 |
【知识点】 氧化还原反应定义、本质及特征解读 常见氧化剂与还原剂解读
| A.它们相差一个电子层 |
| B.它们的化学性质相似 |
| C.钠原子,钠离子均为同一元素 |
| D.灼烧时,它们的焰色反应都呈黄色 |
| A.酚酞溶液 | B.氯化铁溶液 | C.硝酸银溶液 | D.氢氧化钠溶液 |
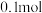 的氯化钠固体配成溶液500ml,所得溶液的物质的量浓度为
的氯化钠固体配成溶液500ml,所得溶液的物质的量浓度为

A.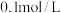 | B.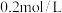 | C. | D. |
【知识点】 物质的量浓度的计算 一定物质的量浓度的溶液的配制
| A.氢 | B.碳 | C.氧 | D.氯 |
【知识点】 元素周期表提供的元素信息解读
| A.容量瓶 | B.试管 | C.烧瓶 | D.烧杯 |
| A.分解反应 | B.置换反应 |
| C.复分解反应 | D.化合反应 |
【知识点】 绿色化学与可持续发展解读 物质的化学变化
| A.氯化钠(NaCl)和碳酸钠(Na2CO3) | B.硫酸(H2SO4)和硫酸铜(CuSO4) |
| C.氢氧化钾(KOH)和硝酸钾(KNO3) | D.氢氧化钙[Ca(OH)2]和碳酸钙(CaCO3) |
【知识点】 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系解读
A. ——烧碱 ——烧碱 | B. ——小苏打 ——小苏打 |
C. ——冰醋酸 ——冰醋酸 | D. ——胆矾 ——胆矾 |
A. | B. | C. | D. |
【知识点】 物质的转化 钠与氧气等非金属的反应解读 铁与非金属单质反应解读
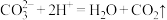 表示的是
表示的是A. 与足量稀盐酸 与足量稀盐酸 | B. 溶液与足量稀醋酸 溶液与足量稀醋酸 |
C. 溶液与足量稀硫酸 溶液与足量稀硫酸 | D. 溶液与足量稀硝酸 溶液与足量稀硝酸 |
【知识点】 离子方程式的正误判断解读
| A.使用容量瓶前应先检查它是否漏水 |
| B.容量瓶先用蒸馏水洗净,再用待配液润洗 |
| C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水,距刻度线1~2cm处时再改用胶头滴管滴加蒸馏水至刻度线 |
| D.浓硫酸稀释后立即转移到容量瓶中进行定容 |
| A.青铜是人类历史上使用最早的合金,至今已有三千多年的历史 |
| B.合金的硬度一般比它的各成分金属的小,熔点一般也比它的各成分金属的高 |
| C.世界上最常见的,用量最大的合金是钢 |
| D.合金可以由金属和非金属熔合而成 |
【知识点】 金属材料的性质及利用 金属与合金性能比较解读
 O2+H2O+2e- =2OH- ,据此判断,锌片是
O2+H2O+2e- =2OH- ,据此判断,锌片是| A.负极,被氧化 | B.正极,被氧化 | C.负极,被还原 | D.正极,被还原 |
| A.二氧化硫可用于抑制酒类中细菌生长,可在葡萄酒中微量添加 |
| B.二氧化硫能使品红褪色,加热后不恢复到红色 |
| C.二氧化硫使酸性高锰酸钾褪色,体现了二氧化硫的漂白性 |
| D.二氧化硫属于碱性氧化物,可以用NaOH溶液吸收 |

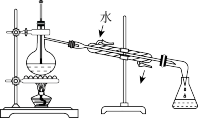
| A.装置A中粉末不变色 |
| B.装置B中溶液褪色 |
| C.装置C用于检验CO2 |
| D.装置D用于吸收尾气 |
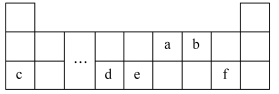
| A.原子半径:a>b |
| B.原子核外电子层数:d>a |
| C.原子的最外层电子数:c>f |
| D.元素的最高价氧化物对应水化物的碱性:c>f |
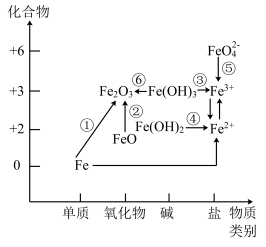
| A.铁在高温下与水蒸气反应可实现上述转化① |
| B.Fe(OH)2是在空气中容易被氧化为Fe(OH)3 |
C.由图可预测:高铁酸盐( )具有强氧化性 )具有强氧化性 |
| D.加热Fe(OH)3实现转化⑥,加硝酸可实现转化③ |
试卷分析
试卷题型(共 50题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 核素 元素、核素、同位素 | |
| 2 | 0.94 | 硫在自然界中的存在 | |
| 3 | 0.85 | 氯气的化学性质 浓硫酸的吸水性 硅的物理性质与用途 二氧化硅的用途 | |
| 4 | 0.65 | 二氧化硅的化学性质 钠单质的保存与用途 仪器使用与实验安全 实验安全 | |
| 5 | 0.85 | 阿伏加德罗常数的应用 22.4L/mol适用条件 气体物质与NA相关的推算 | |
| 6 | 0.65 | 限定条件下的离子共存 铵盐与碱反应 碳酸氢钠与碱反应 | |
| 7 | 0.85 | 离子键 共价键 共价键与离子键的比较 化学键与物质类别关系的判断 | |
| 8 | 0.65 | 原电池原理理解 原电池电子流向判断及应用 原电池正负极判断 | |
| 9 | 0.65 | 离子反应的发生及书写 离子反应的发生条件 离子方程式的书写 离子方程式的正误判断 | |
| 10 | 0.85 | 原子结构示意图、离子结构示意图 元素性质与原子结构的关系 | |
| 11 | 0.85 | 化学反应中能量变化的原因 化学键与化学反应中的能量关系 吸热反应和放热反应 | |
| 12 | 0.85 | 同周期元素性质递变规律 同主族元素性质递变规律 元素周期律的应用 同周期元素性质递变规律理解及应用 | |
| 13 | 0.65 | 氧化还原反应基本概念 | |
| 14 | 0.85 | 物质的转化 一氧化氮的化学性质 含硫化合物之间的转化 | |
| 15 | 0.65 | 硅的物理性质与用途 硅酸盐工业 废弃电池的污染及回收 食品添加剂 | |
| 16 | 0.65 | 氨气的实验室制法 明矾的净水作用及原理 铁盐的检验 印刷电路板 | |
| 17 | 0.65 | 原电池电子流向判断及应用 原电池正负极判断 氢氧燃料电池 | |
| 18 | 0.94 | 胶体 | |
| 19 | 0.85 | 配制一定物质的量浓度的溶液的步骤、操作 配制一定物质的量浓度的溶液实验的误差分析 配制一定物质的量浓度的溶液实验的仪器 | |
| 20 | 0.85 | 氧化还原反应定义、本质及特征 吸热反应和放热反应 | |
| 21 | 0.94 | 电解质与非电解质 电解质、非电解质概念 非电解质、电解质物质类别判断 | |
| 22 | 0.85 | 氯水的性质 氯水性质实验探究 | |
| 23 | 0.94 | 物理变化与化学变化 | |
| 24 | 0.94 | 原子核外电子的排布 核外电子排布规律 | |
| 25 | 0.85 | 二氧化硫与二氧化碳的性质区别 | |
| 26 | 0.94 | 同周期元素性质递变规律 | |
| 27 | 0.65 | 元素非金属性强弱的比较方法 | |
| 28 | 0.85 | 氧化还原反应定义、本质及特征 常见氧化剂与还原剂 | |
| 29 | 0.65 | 氯气 硅单质 镁 铝 | |
| 30 | 0.65 | 氧化还原反应的规律 含硫化合物之间的转化 | |
| 31 | 0.85 | 焰色试验 物质结构与性质综合考查 原子核外电子的排布 核素 | |
| 32 | 0.65 | 氯离子的检验 氯水的性质 | |
| 33 | 0.94 | 物质的量浓度的计算 一定物质的量浓度的溶液的配制 | |
| 34 | 0.94 | 元素周期表提供的元素信息 | |
| 35 | 0.65 | 仪器使用与实验安全 常用仪器及使用 配制一定物质的量浓度的溶液实验的仪器 | |
| 36 | 0.94 | 绿色化学与可持续发展 物质的化学变化 | |
| 37 | 0.85 | 化学实验基础操作 实验安全 蒸馏与分馏 | |
| 38 | 0.85 | 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系 | |
| 39 | 0.94 | 常见硫酸盐的性质 碳酸钠的俗称、物理性质及用途 碳酸氢钠的俗称、物理性质及用途 乙酸物理性质总结 | |
| 40 | 0.85 | 物质的转化 钠与氧气等非金属的反应 铁与非金属单质反应 | |
| 41 | 0.85 | Fe3+的检验 常见阳离子的检验 | |
| 42 | 0.65 | 离子方程式的正误判断 | |
| 43 | 0.85 | 常用仪器及使用 | |
| 44 | 0.65 | 铵根离子的检验 硫酸根离子的检验 离子的检验 | |
| 45 | 0.85 | 金属材料的性质及利用 金属与合金性能比较 | |
| 46 | 0.65 | 原电池原理理解 原电池正负极判断 | |
| 47 | 0.65 | 二氧化硫的化学性质 硫、氮氧化物对人体、环境的危害 酸雨 | |
| 48 | 0.85 | 二氧化硫的漂白性 二氧化硫与其他强氧化剂的反应 浓硫酸的强氧化性 物质性质的探究 | |
| 49 | 0.85 | 元素周期表提供的元素信息 元素金属性与非金属性递变规律的理解及应用 微粒半径大小的比较方法 | |
| 50 | 0.65 | 物质的转化 铁与水蒸气的反应 氢氧化铁化学性质 氢氧化亚铁的还原性 | |

 I的说法正确的是
I的说法正确的是


 、
、 、NaCl、
、NaCl、 四种溶液区别,这种试剂是
四种溶液区别,这种试剂是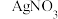 溶液
溶液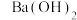 溶液
溶液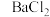 溶液
溶液

