2016-2017学年湖北省部分重点中学高一上学期期中化学试卷
湖北
高一
期中
2017-07-27
251次
整体难度:
适中
考查范围:
认识化学科学、化学实验基础、化学反应原理
一、单选题 添加题型下试题
| A.胶体发生电泳 | B.血液中发生氧化还原反应 |
| C.血液中发生复分解反应 | D.胶体发生聚沉 |
| A.汽油失火时,立即用水灭火 |
| B.实验室不小心碰翻酒精灯引起实验桌上洒落的少量酒精起火时,迅速用泡沫灭火器灭火 |
| C.浓硫酸溅到皮肤上,立即用稀 NaOH 溶液洗涤 |
| D.浓 NaOH 溶液溅到皮肤上,立即用水冲洗,然后涂上稀硼酸溶液 |
【知识点】 仪器使用与实验安全
二、未知 添加题型下试题
三、单选题 添加题型下试题
| A.③②①⑤④ | B.①②③⑤④ |
| C.②③①④⑤ | D.③⑤②①④ |
【知识点】 离子反应在混合物分离、除杂中的应用解读 物质的分离、提纯
| A.清晨,在茂密的树林,常常可以看到从枝叶间透过的一道道光柱 |
| B.一支钢笔使用两种不同牌号的蓝黑墨水,易出现堵塞 |
| C.在饱和FeCl3溶液中逐滴加入NaOH溶液,产生红褐色沉淀 |
| D.在河水与海水交界处有三角洲形成 |
A. | B. |
C.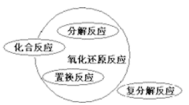 | D. |
【知识点】 四种基本反应类型解读 氧化还原反应基本概念
| A.称取7.68g硫酸铜,加入500mL水 |
| B.称取12.0g胆矾配成500mL溶液 |
| C.称取12.5g胆矾配成500mL溶液 |
| D..称取8.0g硫酸铜,加入500mL水 |
【知识点】 物质的量浓度计算-溶液配制有关计算解读
①在制取氧气中排水法收集氧气后出现倒吸现象,立即松开试管上的橡皮塞
②进行萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
③水和碘的四氯化碳溶液分液时,水从分液漏斗下口流出,碘的四氯化碳溶液从漏斗上口倒出
④进行蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
⑤酒精着火时可用湿抹布或沙子扑灭
⑥用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中
| A.①⑥ | B.②③④ | C.②④⑤ | D.③④⑤ |
| A.沸点不同的液态混合物可用蒸馏方法分离 |
| B.互不相溶的液态混合物可用分液方法分离 |
| C.互溶的液态混合物可用分液的方法分离 |
| D.可溶于水的固体与难溶于水的固体形成的混合物可用溶解、过滤、蒸发的方法分离 |
| A.氧化还原反应中,一种元素被氧化,一定是另一种元素被还原 |
| B.某元素由化合态变成游离态,此元素可能被氧化,也可能被还原 |
| C.金属单质在反应中只能作还原剂,非金属单质只能作氧化剂 |
| D.金属原子失电子越多,其还原性越强 |
【知识点】 氧化还原反应基本概念
| A.碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑ |
| B.稀H2SO4与铁粉反应:2Fe+6H+=2Fe3++3H2↑ |
| C.氢氧化钡溶液与稀H2SO4反应:Ba2++SO42-=BaSO4↓ |
| D.将氢氧化铁放入盐酸中:Fe(OH)3+3H+=Fe3++3H2O |
【知识点】 离子反应的发生及书写
| A.电解质与非电解质的本质区别,是在水溶液或熔化状态下能否电离 |
| B.强电解质与弱电解质的本质区别,是其水溶液导电性的强弱 |
| C.酸、碱和盐类都属于电解质,其他化合物都是非电解质 |
| D.常见的强酸、强碱和大部分盐都是强电解质,其他化合物都是非电解质 |
【知识点】 电解质、非电解质概念解读 强电解质与弱电解质解读
| A.3CuS+8HNO3=3Cu(NO3)2+2NO↑+3S↓+4H2O |
| B.3Cl2+6KOH=5KCl+KClO3+3H2O |
| C.3CCl4+K2Cr2O7=2CrO2C12+3COCl2+2KCl |
D.2KMnO4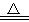 K2MnO4+MnO2+O2↑ K2MnO4+MnO2+O2↑ |
【知识点】 氧化还原反应基本概念
| A.标准状况下,22.4L H2O含有的分子数为1NA |
| B.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02NA |
| C.通常状况下,1NA个CO2分子占有的体积为22.4L |
| D.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为1NA |
| 选项 | 物质 | 杂质 | 除杂试剂或操作方法 |
| A | NaCl溶液 | Na2CO3 | 加入盐酸,蒸发 |
| B | FeSO4溶液 | CuSO4 | 加入过量铁粉并过滤 |
| C | H2 | CO2 | 依次通过盛有NaOH溶液和浓硫酸的洗气瓶 |
| D | NaNO3 | CaCO3 | 加稀盐酸溶解、过滤、蒸发、结晶 |
| A.A | B.B | C.C | D.D |
四、填空题 添加题型下试题
(2)分析氧化还原反应2P+5Br2+8H2O=2H3PO4+10HBr,用“双线桥法”表示出反应中电子转移的方向和数目为_______________________。
反应中氧化剂与还原剂的物质的量之比为____________________。
(3) 氧化还原反应3S + 6KOH = K2S + K2SO3 + 3H2O中,氧化产物是______________,还原产物是_______________。该反应的离子方程式为:___________________。
【知识点】 氧化还原反应
(1)该气体的物质的量为___________mol。
(2)该气体中所含的原子总数为______个(阿伏加德罗常数用NA表示)。
(3)该气体在标准状况下的体积为___________L。
(4)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为______________。
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为__________mol·L-l。
【知识点】 化学计量
【知识点】 离子反应的发生及书写
五、解答题 添加题型下试题
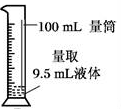
(1)所需浓硫酸的体积是 ,量取浓硫酸所用的量筒的规格是 ,
(从下列量筒的规格中选用(A10mL B20mL C50mL D100mL)
(2)第③步实验的操作是 。
(3)下列情况对所配制的稀硫酸浓度有何影响?(用偏大、偏小、无影响填写)
| A.所用的浓硫酸长时间放置在密封不好的容器中 |
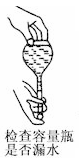
| B.容量瓶用蒸馏洗涤后残留有少量的水 |
| C.所用过的烧杯、玻璃棒未洗涤 |
| D.定容时俯视溶液的液凹面 |
六、填空题 添加题型下试题

(1)该混合溶液中,Na+的物质的量为
(2)该混合溶液中含溶质的总质量为
(3)将该混合溶液加水稀释至体积为 1 L,稀释后溶液中Cl-的物质的量浓度为
【知识点】 物质的量浓度的计算
试卷分析
试卷题型(共 21题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 胶体 胶体的性质和应用 | |
| 2 | 0.85 | 仪器使用与实验安全 | |
| 3 | 0.94 | 仪器使用与实验安全 | |
| 5 | 0.85 | 离子反应在混合物分离、除杂中的应用 物质的分离、提纯 | |
| 6 | 0.65 | 胶体的性质和应用 | |
| 7 | 0.85 | 四种基本反应类型 氧化还原反应基本概念 | |
| 8 | 0.65 | 物质的量浓度计算-溶液配制有关计算 | |
| 9 | 0.65 | 仪器使用与实验安全 化学实验基础操作 | |
| 10 | 0.85 | 蒸馏与分馏 萃取和分液 | |
| 11 | 0.64 | 氧化还原反应基本概念 | |
| 12 | 0.64 | 离子反应的发生及书写 | |
| 13 | 0.65 | 电解质、非电解质概念 强电解质与弱电解质 | |
| 14 | 0.85 | 氧化还原反应基本概念 | |
| 15 | 0.85 | 阿伏加德罗常数的应用 22.4L/mol适用条件 气体物质与NA相关的推算 | |
| 16 | 0.65 | 离子反应在混合物分离、除杂中的应用 物质分离、提纯的常见化学方法 | |
| 二、未知 | |||
| 4 | 0.65 | 离子的检验 | 未知 |
| 三、填空题 | |||
| 17 | 0.64 | 氧化还原反应 | |
| 18 | 0.4 | 化学计量 | |
| 19 | 0.64 | 离子反应的发生及书写 | |
| 21 | 0.65 | 物质的量浓度的计算 | |
| 四、解答题 | |||
| 20 | 0.64 | 化学计量 仪器使用与实验安全 | 实验探究题 |