吉林省长春市兴华中学2019-2020学年高一上学期期中考试化学试题
吉林
高一
期中
2020-02-07
371次
整体难度:
适中
考查范围:
化学实验基础、认识化学科学、化学与STSE、常见无机物及其应用、化学反应原理
一、单选题 添加题型下试题
| A.蒸馏 | B.升华 | C.过滤 | D.萃取 |
【知识点】 物质分离、提纯的常见物理方法 升华解读
| A.从碘水中提取单质碘时,不能用无水乙醇代替CCl4 |
B.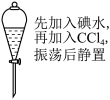 进行该图操作后,实验现象为:液体分层,下层呈紫红色 进行该图操作后,实验现象为:液体分层,下层呈紫红色 |
C. 利用该装置可以分离CCl4和水 利用该装置可以分离CCl4和水 |
| D.萃取操作时,应选择有机萃取剂,且萃取剂密度必须比水大 |
【知识点】 物质分离、提纯的常见物理方法 萃取和分液解读
| A.HCl→H2 | B.HCl→FeCl2 |
| C.H2SO4(浓) →SO2 | D.Fe→Fe2O3 |
【知识点】 氧化还原反应的几组概念解读
| A.纯碱、烧碱均属于碱 | B.凡能电离出H+的化合物均属于酸 |
| C.CuSO4·5H2O属于纯净物 | D.盐类物质一定含有金属阳离子 |
【知识点】 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系解读
| A.Ba(OH)2 | B.CH4 | C.Cl2 | D.HCl |
二、未知 添加题型下试题
三、单选题 添加题型下试题
A.2 L溶液中Ba2+、 总数为1.2NA 总数为1.2NA |
B.500 mL溶液中 浓度为0.2 mol·L-1 浓度为0.2 mol·L-1 |
| C.500 mL溶液中Ba2+浓度为0.2 mol·L-1 |
D.500 mL溶液中 物质的量为0.2 mol 物质的量为0.2 mol |
| A.常温常压下,32 g氧气的体积约为22.4L |
| B.1.8 g NH4+中含有的质子数为NA |
| C.常温常压下,48g O3含有的氧原子数为3NA |
| D.2.4 g金属镁变为镁离子时失去的电子数为0.1NA |
| A.胶体发生电泳 | B.血液中发生氧化还原反应 |
| C.血液中发生复分解反应 | D.胶体发生聚沉 |
 及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤②加过量NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液。下列操作顺序中最合适的是
及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤②加过量NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液。下列操作顺序中最合适的是| A.①④②⑤③ | B.④①②⑤③ | C.②⑤④①③ | D.⑤②④③① |
 相对应的化学方程式正确的是
相对应的化学方程式正确的是A.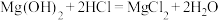 |
B.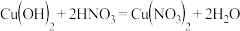 |
C.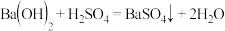 |
D. |
【知识点】 离子反应的发生及书写 离子方程式的正误判断解读
| A.加入AgNO3溶液有白色沉淀生成,证明原溶液中一定有Cl- |
B.在加入稀硝酸后的溶液中,滴加BaCl2溶液,有白色沉淀生成,证明原溶液中一定有 |
C.加入盐酸后加热,放出能使澄清石灰水变浑浊的无色气体,证明原溶液中一定含有 |
| D.加入紫色石蕊溶液,溶液显红色,证明溶液一定呈酸性 |
| A.同温同压下,相同体积的氮气和氦气所含的原子数相等 |
| B.标准状况下,5.6 L以任意比例混合的氯气和氧气所含的原子数为0.5NA |
| C.标准状况下,22.4 L SO3与水反应生成1 mol硫酸 |
| D.常温常压下,22.4 L的NO2和CO2混合气体含有2NA个O原子 |
| A.1∶6 | B.6∶1 | C.1∶5 | D.5∶1 |
【知识点】 氧化还原反应的规律解读 与氧化剂、还原剂有关的计算解读
| A.体积②>③>①>④ | B.密度 ②<③<④<① |
| C.质量②>③>④>① | D.氢原子个数 ①<③<④<② |
四、 添加题型下试题
A.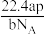 | B.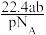 |
C.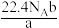 | D.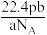 |
五、单选题 添加题型下试题
| A.金属镁与稀盐酸反应:有气体生成,Mg+2H++2Cl-=MgCl2+H2↑ |
| B.氯化钡溶液与硫酸反应:有白色沉淀生成:SO42-+Ba2+ =BaSO4↓ |
| C.碳酸钠溶液与盐酸反应:有气泡逸出:Na2CO3+2H+=2Na++CO2↑+H2O |
| D.过量铁粉与氯化铜溶液反应:溶液南蓝色变成浅绿色,同时有红色固体生成:Fe+Cu2+=Fe3++Cu |
【知识点】 离子反应的发生及书写 离子方程式的书写解读 离子方程式的正误判断解读
容量瓶容积 | 溶质质量 | 实验操作 | |
A | 480mL | 硫酸铜:7.68g | 加入500mL水 |
B | 480mL | 胆矾:12.0g | 配成500mL溶液 |
C | 500mL | 硫酸铜:8.0g | 加入500mL水 |
D | 500mL | 胆矾:12.5g | 配成500mL溶液 |
| A.A | B.B | C.C | D.D |
| A.三氧化硫与水反应:SO3+H2O=2H++SO42— |
| B.碳酸钙与盐酸:CaCO3+2H+=Ca2++CO2↑+H2O |
| C.氧化铜与稀硫酸:CuO+2H+=Cu2++H2O |
| D.碳酸氢钠溶液与氯化钡溶液反应:Ba2++CO32—=BaCO3↓ |
【知识点】 离子方程式的正误判断解读
| A.CO32- | B.NO3- | C.OH- | D.SO42- |
 2AlN+3CO。下列叙述正确的是( )
2AlN+3CO。下列叙述正确的是( )| A.AlN中氮的化合价为+3 |
| B.AlN的摩尔质量为41 g |
| C.上述反应中,N2是氧化剂,Al2O3既不是氧化剂也不是还原剂。 |
| D.上述反应中,每生成1 mol AlN需转移6 mol电子 |
| A. (b-a)/V mol·L-1 | B.(2b-a)/V mol·L-1 |
| C.2(2b-a)/V mol·L-1 | D.2(b-a)/V mol·L-1 |
六、填空题 添加题型下试题
(1) 属于电解质的是:
(2) 属于非电解质的是:
(3) 能导电的是:
(1)被氧化的元素是
(2)氧化剂与还原剂的物质的量之比是
(3)用双线桥法分析上述反应的电子转移方向和数目
七、计算题 添加题型下试题
(1)2 mol CO(NH2)2中含
(2)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为
(3)CO和CO2的混合气体18 g,在标准状况下的体积为11.2 L,则混合气体的平均摩尔质量为
八、解答题 添加题型下试题
 、
、 、
、 、
、 、
、 等混合而成,为检验它们,做了以下实验:
等混合而成,为检验它们,做了以下实验:①将固体混合物溶于水中,搅拌后得无色透明溶液;
②往此溶液中滴加硝酸钡溶液,有白色沉淀产生;
③过滤,将沉淀物置于稀硝酸中,发现沉淀全部溶解。
根据上述实验事实,回答下列问题:
(1)原固体混合物中一定含有的物质是
(2)写出步骤③中的离子方程式:
【知识点】 离子反应在化合物组成的分析、鉴定的应用解读

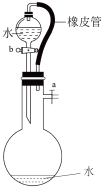
该实验的主要操作步骤如下:
①用已知浓度的浓盐酸配制100mL 1.0mol/L的盐酸溶液,需要用到的仪器有量筒、烧杯、玻璃棒、胶头滴管、______;
②用10mL量筒量取8.0mL 1.0mol/L的盐酸溶液加入锥形瓶中;
③准确称取a g已除去表面氧化膜的镁条,并系于铜丝末端,为使HCl全部参加反应,a的数值至少为______;
④往广口瓶中装入足量水,按上图连接好装置,检查装置的气密性;
⑤反应结束后待体系温度恢复到室温,忽略导管中的水,读出量筒中水的体积为VmL。
请回答下列问题。
(1)步骤①中,配制100mL 1.0mol/L的盐酸溶液时,下列哪些操作会使配制浓度偏低
A. 用量筒量取浓盐酸时,俯视量筒的刻度
B. 容量瓶未干燥即用来配制溶液
C. 未洗涤烧杯和玻璃棒
D.定容完成后,将容量瓶倒置摇匀后,发现液面低于刻度线
E.在容量瓶中定容时俯视容量瓶刻度线
(2)请填写操作步骤中的空格:步骤①
(3)实验步骤⑤中应选用
A.100mL B.200mL C.500mL
(4)读数时需要注意(至少写两点)
(5)忽略水蒸气影响,在该条件下测得气体摩尔体积为Vm=
试卷分析
试卷题型(共 30题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 物质分离、提纯的常见物理方法 升华 | |
| 2 | 0.85 | 物质分离、提纯的常见物理方法 萃取和分液 | |
| 3 | 0.94 | 氧化还原反应的几组概念 | |
| 4 | 0.85 | 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系 | |
| 5 | 0.85 | 电解质与非电解质 电解质、非电解质概念 非电解质、电解质物质类别判断 物质水溶液的导电性 | |
| 8 | 0.65 | 阿伏加德罗常数的应用 依据物质的量浓度公式的基础计算 物质的量浓度计算-与溶质成分有关的计算 | |
| 9 | 0.85 | 阿伏加德罗常数的应用 结合气体物质与NA相关推算 结合氧化还原反应知识与NA相关推算 结合物质结构基础知识与NA相关推算 | |
| 10 | 0.94 | 胶体 胶体的性质和应用 | |
| 11 | 0.85 | 离子反应在混合物分离、除杂中的应用 物质分离、提纯的常见化学方法 海水中盐的开发及利用 | |
| 12 | 0.65 | 离子反应的发生及书写 离子方程式的正误判断 | |
| 13 | 0.65 | 氯离子的检验 硫酸根离子的检验 常见阳离子的检验 常见阴离子的检验 | |
| 14 | 0.85 | 阿伏加德罗常数的求算 阿伏加德罗常数的应用 结合气体物质与NA相关推算 结合氧化还原反应知识与NA相关推算 | |
| 15 | 0.65 | 氧化还原反应的规律 与氧化剂、还原剂有关的计算 | |
| 16 | 0.65 | 阿伏加德罗定律 物质的量有关计算 根据n=N/NA进行相关计算 以N=m·NA/M为中心的有关基本粒子的推算 | |
| 18 | 0.85 | 离子反应的发生及书写 离子方程式的书写 离子方程式的正误判断 | |
| 19 | 0.94 | 物质的量浓度计算-溶液配制有关计算 一定物质的量浓度的溶液的配制 | |
| 20 | 0.85 | 离子方程式的正误判断 | |
| 21 | 0.65 | 无附加条件的离子共存 限定条件下的离子共存 离子反应在化合物组成的分析、鉴定的应用 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 | |
| 22 | 0.85 | 化学实验基础操作 | |
| 23 | 0.85 | 氧化还原反应的应用 氧化还原反应在生活、生产中的应用 氧化还原反应的规律 与氧化剂、还原剂有关的计算 | |
| 24 | 0.65 | 物质的量浓度与溶质成分有关的计算 物质的量浓度与溶液混合的计算 离子反应在化合物组成的分析、鉴定的应用 | |
| 25 | 0.65 | 物质水溶液的导电性 | |
| 二、未知 | |||
| 6 | 0.85 | 离子反应的发生条件 离子共存 物质共存 限定条件下的离子共存 | 未知 |
| 7 | 0.65 | 胶体的性质和应用 | 未知 |
| 三、 | |||
| 17 | 0.65 | 气体摩尔体积 根据n=N/NA的相关计算 气体物质与NA相关的推算 根据n=m/M的相关计算 | |
| 四、填空题 | |||
| 26 | 0.85 | 电解质、非电解质概念 非电解质、电解质物质类别判断 物质水溶液的导电性 | |
| 27 | 0.85 | 单线桥、双线桥分析氧化还原反应 氧化还原反应有关计算 与氧化剂、还原剂有关的计算 | |
| 五、计算题 | |||
| 28 | 0.65 | 物质的量有关计算 根据n=N/NA进行相关计算 根据n=m/M进行相关计算 以N=m·NA/M为中心的有关基本粒子的推算 | |
| 六、解答题 | |||
| 29 | 0.85 | 离子反应在化合物组成的分析、鉴定的应用 | 无机推断题 |
| 30 | 0.65 | 配制一定物质的量浓度的溶液实验的误差分析 配制一定物质的量浓度的溶液实验的仪器 配制一定物质的量浓度溶液的综合考查 | 实验探究题 |


 溶液中,分别滴入物质的量浓度相等的
溶液中,分别滴入物质的量浓度相等的 、
、 溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
溶液,其导电能力随滴入溶液体积变化的曲线如图所示。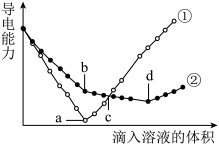
 溶液的变化曲线
溶液的变化曲线 、
、


