2015-2016学年湖南省宁远县一中高一上学期期中测试化学试卷
湖南
高一
期中
2017-07-27
336次
整体难度:
适中
考查范围:
认识化学科学、化学实验基础
一、单选题 添加题型下试题
| A.石墨 | B.烧碱 | C.蔗糖 | D.金属铝 |
【知识点】 非电解质、电解质物质类别判断解读
①根据氧化物的元素组成将氧化物分为金属氧化物和非金属氧化物;
②根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应;
③根据分散系是否有丁达尔效应来区分溶液、胶体;
④根据在水溶液里或者熔融状态下能否导电可将纯净物分为电解质和非电解质.
| A.①②④ | B.①②③ | C.②③④ | D.全部 |
【知识点】 物质的分类
| A.刻度线 | B.浓度 | C.温度 | D.容积 |
【知识点】 仪器使用与实验安全
A.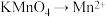 | B. |
C.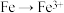 | D.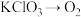 |
【知识点】 氧化还原反应基本概念 氧化还原反应的规律解读
| A.可利用过滤的方法区别溶液和胶体 |
| B.制备Fe(OH)3胶体通常是将Fe(OH)3固体溶于沸水 |
| C.直径介于1nm~100nm之间的微粒称为胶体 |
| D.电泳现象证明胶体粒子是带电的 |
【知识点】 分散系
| A.150mL 2mol•L﹣1 KClO3溶液 | B.75mL 2mol•L﹣1 CaCl2溶液 |
| C.150mL 2mol•L﹣1 KCl溶液 | D.75mL 1mol•L﹣1 AlCl3溶液 |
【知识点】 化学计量
| A.含有最高价元素的化合物不一定具有很强的氧化性 |
| B.一种元素被氧化,肯定有另一种元素被还原 |
| C.在化学反应中,得电子越多的氧化剂,其氧化性就越强 |
| D.阳离子只能得到电子被还原,阴离子只能失去电子被氧化 |
【知识点】 氧化还原反应基本概念
| A.大于50% | B.等于50% | C.小于50% | D.无法确定 |
【知识点】 物质的量浓度计算-溶液混合的有关计算解读
| A.Ag++Cl-=AgCl↓AgNO3+NaCl=AgCl↓+NaNO3 |
| B.Cu+2Ag+=Cu2++2AgCu+2AgCl=CuCl2+2Ag |
| C.Ba2++SO42-=BaSO4↓Ba(OH)2+H2SO4=BaSO4↓+2H2O |
| D.CO32-+2H+=CO2↑+H2ONaHCO3+HCl=NaCl+CO2↑+H2O |
【知识点】 离子反应的发生及书写 离子方程式的正误判断解读
| A.1∶6 | B.6∶1 | C.1∶5 | D.5∶1 |
【知识点】 氧化还原反应的规律解读 与氧化剂、还原剂有关的计算解读
| A.K+、Na+、NO3-、CO32- | B.K+、Na+、Br-、SO32- |
| C.K+、Na+、I-、SO42- | D.Na+、K+、CH3COO-、SO42- |
【知识点】 离子共存
| A.m=4,R3+是氧化产物 | B.m=2y,R3+是氧化产物 |
| C.m=2,R3+是还原产物 | D.m=y,R3+是还原产物 |
【知识点】 氧化还原反应基本概念
| A.1 L 0.1mol·L-1的NaHCO3溶液中含有阳离子的物质的量为0.2mol |
| B.4℃时9mL水和标准状况下11.2L氮气含有相同的原子数 |
| C.在25℃,1.01×105 Pa时,11.2 L氧气所含的氧原子数目为6.02×1023 |
| D.标准状况下,氧原子总数为0.2NA的SO2和O2的混合气体,其体积为2.24 L |
| A.N2 | B.N2O | C.NO | D.NO2 |
【知识点】 氧化还原反应有关计算
二、填空题 添加题型下试题
①碳酸氢钠
(2)写出下列反应的离子方程式
①氢氧化铜和稀盐酸反应
②用稀硫酸清洗铁锈(Fe2O3)
【知识点】 离子反应
(1)2KMnO4 + 16HCl(浓)=2KCl + 2MnCl2 + 5Cl2↑+ 8H2O
(2)该反应中,元素化合价升高的是
还原产物是
(3)反应中若有71克Cl2生成,转移的电子数为
【知识点】 氧化还原反应
 、OH-、HCO
、OH-、HCO
 、
、Cl-、SO42-等离子中的若干种。为了确定溶液的组成,进行了如下操作:
①向溶液中滴加酚酞试液,溶液显红色;
②取2 mL溶液,先加足量稀硝酸酸化,有气体产生,再加氯化钡溶液进行检验,没有明显现象;
(1)原溶液中一定存在的离子是
(2)经过上述操作后,还不能肯定是否存在的离子是
【知识点】 离子反应
三、解答题 添加题型下试题
(1)用10%(密度为1.00g·cm-3)的NaOH溶液配制成27.5g2%的NaOH溶液。
①计算:需
②量取:用
(2)把98%(密度为1.84g·cm-3)的浓硫酸稀释成3mol/L的稀硫酸100mL,回答下列问题:
①需要量取浓硫酸
②配制操作可分解成如下几步,正确的操作顺序是:
A.向容量瓶中注入少量蒸馏水,检查是否漏水
B.用少量蒸馏水洗涤烧杯及玻璃棒,将洗涤液注入容量瓶中,并重复操作两次
C.把已冷却的稀硫酸注入经检查不漏水的容量瓶中
D.根据计算,用量筒量取一定体积的浓硫酸
E.将浓硫酸沿烧杯壁慢慢注入盛有蒸馏水的小烧杯中,并不断用玻璃棒搅拌
F.盖上容量瓶的塞子,振荡,摇匀
G.用胶头滴管滴加蒸馏水,使液面达到刻度线
H.继续往容量瓶中加蒸馏水,使液面接近刻度线
③如果上述C操作中把未冷却的稀硫酸注入容量瓶中,所配溶液的浓度将
四、计算题 添加题型下试题
2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O(写出计算过程)
(1)所用HCl溶液的物质的量浓度是多少?
(2)15.8gKMnO4能使多少克HCl发生上述反应?有多少克HCl被氧化?
(3)若Cl2在标准状况下的密度为3.17g·L-1,则产生的Cl2在标准状况下的体积为多少?
【知识点】 化学计量 氧化还原反应有关计算
试卷分析
试卷题型(共 21题)
试卷难度
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 非电解质、电解质物质类别判断 | |
| 2 | 0.85 | 摩尔质量 气体摩尔体积 | |
| 3 | 0.85 | 物质的分类 | |
| 4 | 0.94 | 仪器使用与实验安全 | |
| 5 | 0.85 | 化学实验基础 仪器使用与实验安全 | |
| 6 | 0.65 | 氧化还原反应基本概念 氧化还原反应的规律 | |
| 7 | 0.85 | 分散系 | |
| 8 | 0.85 | 化学计量 | |
| 9 | 0.64 | 氧化还原反应基本概念 | |
| 10 | 0.65 | 物质的量浓度计算-溶液混合的有关计算 | |
| 11 | 0.85 | 离子反应的发生及书写 离子方程式的正误判断 | |
| 12 | 0.65 | 氧化还原反应的规律 与氧化剂、还原剂有关的计算 | |
| 13 | 0.64 | 离子共存 | |
| 14 | 0.65 | 氧化还原反应基本概念 | |
| 15 | 0.65 | 22.4L/mol适用条件 气体物质与NA相关的推算 | |
| 16 | 0.65 | 氧化还原反应有关计算 | |
| 二、填空题 | |||
| 17 | 0.64 | 离子反应 | |
| 18 | 0.64 | 氧化还原反应 | |
| 19 | 0.4 | 离子反应 | |
| 三、解答题 | |||
| 20 | 0.64 | 化学计量 仪器使用与实验安全 | 实验探究题 |
| 四、计算题 | |||
| 21 | 0.64 | 化学计量 氧化还原反应有关计算 | |



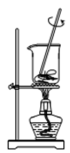 蒸发
蒸发 过滤
过滤 蒸馏
蒸馏 分液
分液

