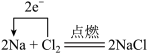贵州省贵阳市清镇养正学校2020-2021学年高一上学期期中考试化学试题
贵州
高一
期中
2021-03-01
196次
整体难度:
适中
考查范围:
认识化学科学、化学实验基础
一、单选题 添加题型下试题
| A.碱 | B.酸 | C.氧化物 | D.盐 |
【知识点】 树状分类法解读 酸、碱、盐、氧化物的概念及其相互联系解读
| A.“霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应 |
| B.“熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应 |
| C.屠呦呦提取青蒿素加入乙醚萃取,此过程属于化学变化 |
| D.“春蚕到死丝方尽,蜡炬成灰泪始干” 诗句中涉及氧化还原反应 |
①有色玻璃 ②淀粉溶液 ③硫酸钠溶液 ④云、雾 ⑤Fe(OH)3悬浊液
| A.①③ | B.②④⑤ | C.①③⑤ | D.③⑤ |
| A.稀硫酸 | B.熔融态的氯化钠 | C.NaCl晶体 | D.金属铜 |
【知识点】 非电解质、电解质物质类别判断解读
| A.NaOH→NaCl | B.H2SO4→H2 | C.HCl→Cl2 | D.CaCO3→CO2 |
【知识点】 氧化还原反应基本概念 氧化还原反应的应用
| A.用稀盐酸清洗铁锈(Fe2O3):Fe2O3+6H+===2Fe3++3H2O |
| B.铜片与硝酸银溶液反应:Cu+Ag+===Cu2++Ag |
C.硫酸铜溶液和氢氧化钡溶液混合:Ba2++ ===BaSO4↓ ===BaSO4↓ |
| D.向稀硫酸中投入铁粉:2Fe+6H+===2Fe3++3H2↑ |
【知识点】 离子方程式的正误判断解读
 的是
的是
| A.16g氧气 | B.2g氢气 |
C. 氮气 氮气 标准状况 标准状况 | D.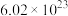 个氯气分子 个氯气分子 |
二、未知 添加题型下试题
三、单选题 添加题型下试题
| 酸 | 碱 | 盐 | 酸性氧化物 | 碱性氧化物 | |
| A | H2SO4 | Na2CO3 | Cu2SO4 | CO2 | MgO |
| B | HCl | NaOH | NaCl | CO | Na2O |
| C | CH3COOH | Cu2(OH)2CO3 | CaCO3 | SO2 | CuO |
| D | HNO3 | KOH | NaHCO3 | SO2 | CaO |
| A.A | B.B | C.C | D.D |
| A.2Na2O2+2H2O=4NaOH+O2 ↑ |
| B.NO+NO2+Na2CO3=2NaNO2+CO2↑ |
| C.Fe2O3+6HCl=2FeCl3+3H2O |
| D.N2H4+O2=N2+2H2O |
【知识点】 氧化还原反应基本概念 氧化还原反应的规律解读
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、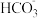 、 、 | D. 、 、 、 、 、 、 |
【知识点】 离子共存 限定条件下的离子共存解读
| A.用醋酸除去水垢:CaCO3 + 2H+ ═Ca2+ + H2O + CO2↑ |
| B.铝片插入硝酸汞溶液中: Al + Hg2+= Al3++ Hg |
| C.Ba(OH)2与稀H2SO4反应:Ba2++2OH﹣+2H++SO42﹣═BaSO4↓+2H2O |
| D.盐酸除铁锈:O2- + 2H+ ═H2O |
【知识点】 离子反应的发生及书写 离子方程式的书写解读 离子方程式的正误判断解读
| A.150mL1mol·L−1KCl 溶液 | B.100mL2mol·L−1KCl 溶液 |
| C.75mL0.5mol·L−1CaCl2 溶液 | D.75mL2mol·L−1AlCl3溶液 |
【知识点】 物质的量浓度计算-与溶质成分有关的计算解读
| A.复分解反应不一定是氧化还原反应 |
| B.置换反应有可能是非氧化还原反应 |
| C.化合反应一定是氧化还原反应 |
| D.分解反应不一定是氧化还原反应 |
| A.2F2+2H2O═4HF+O2 | B.Cl2+H2O═HCl+HClO |
| C.2Na+2H2O═2NaOH+H2↑ | D.C+H2O ═CO+H2 |
【知识点】 氧化还原反应基本概念
A.Na+ 、K+、SO 、HCO 、HCO | B.Cu2+、K+、SO 、NO 、NO |
C.Na+、 K+、Cl、 NO | D.Fe3+、K+、SO 、Cl 、Cl |
【知识点】 限定条件下的离子共存解读
四、填空题 添加题型下试题
(1)配制稀盐酸时,应选用容量为
(2)经计算需要
A.5 mL量筒 B.10 mL量筒
C.25 mL量筒 D.50 mL量筒
(3)在量取浓盐酸后,进行了下列操作:
①等稀释的盐酸的温度与室温一致后,沿玻璃棒注入选定规格的容量瓶中。
②往容量瓶中小心加蒸馏水至液面离容量瓶刻度线1~2 cm时,改用胶头滴管加蒸馏水,使溶液的液面与瓶颈的刻度线相切。
③在盛盐酸的烧杯中注入蒸馏水,并用玻璃棒搅动,使其混合均匀。
④用蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是
(4)在上述配制过程中,用刚刚洗涤洁净的量筒来量取浓盐酸,则配制的稀盐酸浓度
(1)其中能导电的有
(2)在标准状况下,4.48L的HCl气体溶于水配成500mL的溶液,其物质的量浓度为
(3)常温下,32克SO2所含有的氧原子数目为
(4)某氯化钡溶液中含有6.02×1023个Cl-,则该溶液中Ba2+的物质的量是
①醋酸与氢氧化钠反应:
②硝酸银溶液和氯化钠溶液反应:
③少量二氧化碳通入澄清石灰水中:
④铁与盐酸反应:
【知识点】 离子反应的发生及书写 离子方程式的书写解读
(2)实验室用MnO2和浓盐酸制氯气的反应为MnO2+4HCl(浓)
 MnCl2+2H2O+Cl2↑。
MnCl2+2H2O+Cl2↑。①该反应的还原产物是
②该反应中,若有0.2 mol HCl被氧化,能生成标准状况下Cl2的体积为
【知识点】 氧化还原反应的规律解读 与氧化剂、还原剂有关的计算解读 电子转移计算
试卷分析
试卷题型(共 22题)
试卷难度
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 树状分类法 酸、碱、盐、氧化物的概念及其相互联系 | |
| 2 | 0.85 | 胶体的性质和应用 物理变化与化学变化 | |
| 3 | 0.94 | 分散系概念及其分类 胶体的定义及分类 胶体的性质和应用 | |
| 4 | 0.85 | 化学实验基础 仪器使用与实验安全 | |
| 5 | 0.65 | 非电解质、电解质物质类别判断 | |
| 6 | 0.94 | 氧化还原反应基本概念 氧化还原反应的应用 | |
| 7 | 0.65 | 离子方程式的正误判断 | |
| 8 | 0.94 | 阿伏加德罗常数 气体摩尔体积 物质的量有关计算 以N=m·NA/M为中心的有关基本粒子的推算 | |
| 10 | 0.85 | 化学物质的分类方法 酸、碱、盐、氧化物的概念及其相互联系 | |
| 11 | 0.85 | 氧化还原反应基本概念 氧化还原反应的规律 | |
| 12 | 0.65 | 离子共存 限定条件下的离子共存 | |
| 13 | 0.65 | 离子反应的发生及书写 离子方程式的书写 离子方程式的正误判断 | |
| 14 | 0.85 | 物质的量浓度计算-与溶质成分有关的计算 | |
| 15 | 0.65 | 氧化还原反应定义、本质及特征 四种基本反应类型与氧化还原反应的关系 | |
| 16 | 0.65 | 电解质的电离 电解质、非电解质概念 电离的定义 电离方程式 | |
| 17 | 0.85 | 氧化还原反应基本概念 | |
| 18 | 0.85 | 限定条件下的离子共存 | |
| 二、未知 | |||
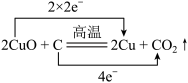
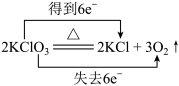
| 9 | 0.65 | 单线桥、双线桥分析氧化还原反应 | 未知 |
| 三、填空题 | |||
| 19 | 0.65 | 一定物质的量浓度的溶液的配制 配制一定物质的量浓度的溶液实验的误差分析 | |
| 20 | 0.94 | 某溶液与物质的量浓度相关的物理量的判断 物质的量有关计算 非电解质、电解质物质类别判断 物质水溶液的导电性 | |
| 21 | 0.94 | 离子反应的发生及书写 离子方程式的书写 | |
| 22 | 0.94 | 氧化还原反应的规律 与氧化剂、还原剂有关的计算 电子转移计算 | |

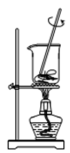 蒸发
蒸发 过滤
过滤 蒸馏
蒸馏 分液
分液