湖南省张家界市民族中学2020-2021学年高一10月月考化学试题
湖南
高一
阶段练习
2020-10-31
220次
整体难度:
适中
考查范围:
认识化学科学、物质结构与性质、常见无机物及其应用、化学实验基础、有机化学基础、化学与STSE
一、单选题 添加题型下试题
 的说法中,不正确的是
的说法中,不正确的是| A.从其阳离子看,属于钾盐 | B.从其阴离子看,属于硝酸盐 |
| C.它属于纯净物中的无机化合物 | D.因为含有氧元素,故它属于氧化物 |
【知识点】 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系解读
| A.CaCO3+2HCl===CaCl2+H2O+CO2↑ |
B.2NaHCO3 Na2CO3+H2O+CO2↑ Na2CO3+H2O+CO2↑ |
| C.Cl2+2NaOH===NaCl+NaClO+H2O |
| D.NaBr+AgNO3===AgBr↓+NaNO3 |
| A.稀硫酸 | B.熔融态的氯化钠 | C.NaCl晶体 | D.金属铜 |
【知识点】 非电解质、电解质物质类别判断解读
①有色玻璃 ②淀粉溶液 ③硫酸钠溶液 ④云、雾 ⑤Fe(OH)3悬浊液
| A.①③ | B.②④⑤ | C.①③⑤ | D.③⑤ |
二、多选题 添加题型下试题
A.MgSO4=Mg2++SO | B.Ba(OH)2=Ba2++ (OH) |
C.Al2(SO4)3=2Al3++3SO | D.KClO3=K++Cl-+3O2- |
三、未知 添加题型下试题
四、单选题 添加题型下试题
| A.Na2CO3 H2SO4 NaHCO3 | B.NaOH HCl NaCl |
| C.CH3COOH NaOH CaCl2 | D.KOH CaCO3 HNO3 |
【知识点】 化学物质的分类方法
| A.OH- | B. | C.Ag+ | D.Cu2+ |
【知识点】 离子共存 无附加条件的离子共存解读
五、未知 添加题型下试题
六、单选题 添加题型下试题
A.Ca2+、Na+、 、 、 | B.Na+、Cl-、H+、Ba2+ |
C.Na+、Fe3+、Cl-、 | D.H+、K+、 、 、 |
【知识点】 限定条件下的离子共存解读
 表示的反应是
表示的反应是| A.醋酸与氨水 | B.稀硫酸与氢氧化钡溶液 |
| C.稀盐酸与氢氧化铜 | D.稀硫酸与烧碱溶液 |
【知识点】 离子反应的发生及书写 离子方程式的书写解读 离子方程式的正误判断解读
七、未知 添加题型下试题
八、单选题 添加题型下试题
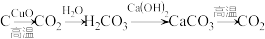
| A.化合、置换、分解、复分解 |
| B.置换、复分解、化合、分解 |
| C.置换、化合、分解、复分解 |
| D.置换、化合、复分解、分解 |
| A.用稀盐酸清洗铁锈(Fe2O3):Fe2O3+6H+===2Fe3++3H2O |
| B.铜片与硝酸银溶液反应:Cu+Ag+===Cu2++Ag |
C.硫酸铜溶液和氢氧化钡溶液混合:Ba2++ ===BaSO4↓ ===BaSO4↓ |
| D.向稀硫酸中投入铁粉:2Fe+6H+===2Fe3++3H2↑ |
【知识点】 离子方程式的正误判断解读
| A.1:1 | B.1:2 | C.1:3 | D.3:1 |
A.使石蕊变红色的溶液:Mg2+、K+、 、 、 |
B.在AgNO3溶液中:H+、K+、 、Cl- 、Cl- |
C.使酚酞变红色的溶液:Na+、Cu2+、 、 、 |
D.在Na2CO3溶液中:H+、Na+、Cl-、 |
【知识点】 限定条件下的离子共存解读
九、多选题 添加题型下试题
| A.NaOH→NaCl | B.H2SO4→H2 | C.HCl→Cl2 | D.Cu →Cu(NO3)2 |
【知识点】 氧化还原反应的几组概念解读 氧化还原反应的规律解读
十、单选题 添加题型下试题
| A.纳米铜是一种新型化合物 | B.纳米铜颗粒比普通铜更易与氧气发生反应 |
| C.纳米铜粒子大小介于1~100 nm | D.利用丁达尔现象可区别纳米铜和普通铜 |
| A.1:2 | B.2:1 | C.1:1 | D.3:2 |
【知识点】 氧化还原反应的应用 氧化还原反应有关计算
(1)将部分粉末加入水中,振荡,有白色沉淀生成;
(2)向(1)的悬浊液中加入过量稀硝酸,白色沉淀消失,并有气泡产生;
(3)取少量(2)的溶液滴入AgNO3溶液,有白色沉淀生成。下列说法正确的是
| A.步骤(1)中的白色沉淀为CaCO3和BaCO3的混合物 |
| B.步骤(2)中一定发生的离子反应为BaCO3+2H+=Ba2++CO2↑+H2O |
| C.将步骤(2)中的稀硝酸改用稀盐酸,对整个实验结果没有影响 |
| D.通过分析,该白色粉末一定含有K2CO3,可能含有Ca(NO3)2、BaCl2 |
十一、填空题 添加题型下试题
①Na2O、CO2、CuO、HNO3;
②HCl、H2O、H2SO4、H2CO3;
③NaOH、Na2CO3、KOH、Cu(OH)2
(1)三种物质依次是(填化学式):A
(2)写出物质A的电离方程式
(3)写出物质C与足量稀硫酸反应的离子方程式
【知识点】 无机物质的分类 电离方程式解读 离子反应的发生及书写
材料一:通常食醋中约含3%~5%的醋酸。醋酸在温度高于16.6℃时是一种无色液体,易溶于水。醋酸具有酸的性质。
材料二:钙是人体中的一种常量元素,人们每日必须摄入一定量钙。动物骨头中含有磷酸钙,但磷酸钙难溶于水,却能跟酸反应生成可溶性的钙盐。
(1)在10℃时,醋酸的状态是
(2)一瓶食醋为500g,则一瓶食醋中至多含醋酸
(3)已知过氧乙酸常温下能分解成醋酸和X气体:2CH3COOOH=2CH3COOH+X↑,则X的化学式为
(4)炖骨汤时人们常用食醋加入其中,主要原因是
十二、解答题 添加题型下试题

(1)写出A、B、C的化学式:A
(2)写出有关反应的化学方程式:A→B
(3)写出有关反应的离子方程式 A→Cu
十三、填空题 添加题型下试题
 MnCl2+Cl2↑+2H2O,据此回答下列问题:
MnCl2+Cl2↑+2H2O,据此回答下列问题:(1)该反应中氧化剂是
(2)用单线桥法表示电子转移的方向和数目:
MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O(3)有一种“地康法”制取氯气的反应原理如图所示:

①反应Ⅰ的离子方程式为
②反应Ⅱ属于
③工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式
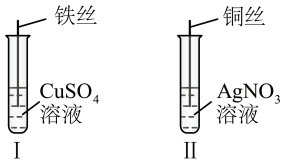
①Ⅱ中发生反应的离子方程式为
②结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为
(2)2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O中氧化性强弱顺序为
(3)反应2H2O+Cl2+SO2=H2SO4+2HCl中还原性强弱顺序为
试卷分析
试卷题型(共 27题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系 | |
| 2 | 0.65 | 氧化还原反应基本概念 氧化还原反应的定义及实质 四种基本反应类型与氧化还原反应的关系 | |
| 3 | 0.65 | 非电解质、电解质物质类别判断 | |
| 4 | 0.65 | 胶体的定义及分类 胶体的制备 | |
| 5 | 0.94 | 分散系概念及其分类 胶体的定义及分类 胶体的性质和应用 | |
| 8 | 0.94 | 化学物质的分类方法 | |
| 9 | 0.94 | 离子共存 无附加条件的离子共存 | |
| 11 | 0.65 | 限定条件下的离子共存 | |
| 12 | 0.85 | 离子反应的发生及书写 离子方程式的书写 离子方程式的正误判断 | |
| 14 | 0.85 | 四种基本反应类型 碳元素及其化合物 | |
| 15 | 0.65 | 离子方程式的正误判断 | |
| 16 | 0.85 | 氧化还原反应的应用 氧化还原反应有关计算 氧化还原反应方程式的配平 | |
| 17 | 0.65 | 限定条件下的离子共存 | |
| 19 | 0.65 | 分散系概念 胶体 胶体的性质和应用 | |
| 20 | 0.94 | 离子方程式的书写 | |
| 21 | 0.65 | 氧化还原反应的应用 氧化还原反应有关计算 | |
| 22 | 0.65 | 离子反应在化合物组成的分析、鉴定的应用 无机物的检验 常见阳离子的检验 | |
| 二、多选题 | |||
| 6 | 0.94 | 电离方程式 | |
| 18 | 0.65 | 氧化还原反应的几组概念 氧化还原反应的规律 | |
| 三、未知 | |||
| 7 | 0.85 | 氧化还原反应的几组概念 氧化还原反应的规律 | 未知 |
| 10 | 0.85 | 单质和化合物 氧化还原反应定义、本质及特征 几组常见同素异形体 | 未知 |
| 13 | 0.94 | 胶体的定义及分类 | 未知 |
| 四、填空题 | |||
| 23 | 0.65 | 无机物质的分类 电离方程式 离子反应的发生及书写 | |
| 24 | 0.85 | 乙酸的组成、结构 对人体健康具有重要意义的有机物 合理安排饮食 | |
| 26 | 0.65 | 四种基本反应类型 离子方程式的书写 氧化还原反应的几组概念 单线桥、双线桥分析氧化还原反应 | |
| 27 | 0.65 | 单线桥、双线桥分析氧化还原反应 氧化性、还原性强弱的比较 基于氧化还原反应守恒规律的计算 | |
| 五、解答题 | |||
| 25 | 0.65 | 物质的转化 铁 铜的其他化合物 | 无机推断题 |

 来表示的是
来表示的是 溶液的反应
溶液的反应

