吉林省长春市第二实验中学2020-2021学年高一上学期9月月考化学试题
吉林
高一
阶段练习
2020-10-22
419次
整体难度:
较易
考查范围:
认识化学科学、常见无机物及其应用、物质结构与性质、化学反应原理、有机化学基础、化学实验基础
一、单选题 添加题型下试题
| A.氧化剂被氧化,还原剂被还原 |
| B.氧化剂发生氧化反应,还原剂发生还原反应 |
| C.一个氧化还原反应中,氧化剂和还原剂可以是一种物质 |
| D.氧化还原反应中,金属单质只作还原剂,非金属单质只作氧化剂 |
【知识点】 氧化还原反应基本概念 氧化还原反应的规律解读
| A.溶液是电中性的,胶体是带电的 |
| B.溶液和胶体都是混合物 |
| C.溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动 |
| D.胶体与溶液的本质区别是有丁达尔效应 |
| A.液态硫酸、NH3 | B.铜、二氧化硫 |
| C.KCl固体、BaSO4 | D.熔融的KNO3、氯气 |
【知识点】 电解质与非电解质 非电解质、电解质物质类别判断解读
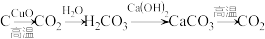
| A.化合、置换、分解、复分解 |
| B.置换、复分解、化合、分解 |
| C.置换、化合、分解、复分解 |
| D.置换、化合、复分解、分解 |
| A.化合物:干冰、冰水混合物、烧碱 |
| B.同素异形体:石墨、C60、金刚石 |
| C.非电解质:乙醇、四氯化碳、氯气 |
| D.混合物:漂白粉、纯净矿泉水、盐酸 |
| A.Fe+CuSO4=FeSO4+Cu | B.3CO+Fe2O3 2Fe+3CO2 2Fe+3CO2 |
| C.AgNO3+NaCl=AgCl↓+NaNO3 | D.2KMnO4  K2MnO4+MnO2+O2↑ K2MnO4+MnO2+O2↑ |
| A.3NO2+H2O=2HNO3+NO |
| B.CaO+H2O=2Ca(OH)2 |
| C.2F2+2H2O=4HF+O2 |
D.3Fe+4H2O(g) Fe3O4+4H2 Fe3O4+4H2 |
【知识点】 氧化还原反应基本概念
| 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
| A | Na2CO3 | H2SO4 | NaCl | Fe3O4 | SO3 |
| B | NaOH | HCl | Cu2(OH)2CO3 | Na2O | SiO2 |
| C | NaOH | NaHSO4 | CaF2 | MgO | H2O |
| D | KOH | HNO3 | NaHCO3 | Mn2O7 | CO2 |
| A.A | B.B | C.C | D.D |
【知识点】 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系解读
| A.氧化还原反应中,一种物质被氧化,另一种物质必被还原 |
| B.失电子数目越多,则还原剂的还原性就越强 |
| C.置换反应一定不属于氧化还原反应 |
| D.反应前后元素化合价没有变化的反应一定不是氧化还原反应 |
| A.根据电解质在水溶液中电离的程度,将电解质分为强电解质和弱电解质 |
| B.Na2O、MgO、Al2O3均属于碱性氧化物 |
| C.根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体 |
| D.石灰石、生石灰、熟石灰均属于碱 |
| A.同一支钢笔使用不同品牌墨水时,容易发生堵塞现象 |
| B.向氯化铁溶液中加入氢氧化钠溶液,产生红褐色沉淀 |
| C.肾功能衰竭等疾病引起的尿中毒,可利用半透膜进行血液透析 |
| D.在海水与河水交界处,易形成三角洲 |
| A.CaCO3+HCl;CaCO3+CH3COOH |
| B.BaCl2+H2SO4;Ba(OH)2+H2SO4 |
| C.NaHCO3+NaOH;Ca(HCO3)2+NaOH |
| D.NaHCO3+H2SO4;KHCO3+HCl |
 和
和 的离子数目之比为1:2时,恰好完全反应,则X元素在还原产物中的化合价为
的离子数目之比为1:2时,恰好完全反应,则X元素在还原产物中的化合价为| A.+1 | B.+2 | C.+3 | D.+4 |
【知识点】 基于氧化还原反应守恒规律的计算解读
A.Na+、Cu2+、Cl-、SO | B.Mg2+、Ba2+、NO 、Cl- 、Cl- |
C.K+、Na+、SO 、CO 、CO | D.K+、Ag+、HCO 、Br- 、Br- |
【知识点】 离子反应的发生条件解读 离子共存 限定条件下的离子共存解读
| A.碳酸钠溶液与石灰乳混合 |
| B.二氧化碳与氢氧化钠溶液反应生成碳酸钠 |
| C.氧化铁在高温下与一氧化碳反应 |
| D.铁与稀硫铜溶液反应 |
【知识点】 离子反应概念解读 氧化还原反应基本概念
| A.静电除尘与胶体的电泳有关 |
| B.当日光从窗隙射入暗室时,可观察到一束光线 |
| C.向氢氧化铁与水形成的某分散系中插入正、负电极,通直流电一段时间后,一极附近颜色变深 |
| D.向氢氧化铁胶体中加入稀硫酸溶液,胶体立即变成无色溶液 |
| A.物质所含元素处于最高价态一定具有强氧化性 |
| B.可以利用金属活动性顺序表判断金属单质的还原性 |
| C.氧化还原反应的本质是电子的得失 |
| D.金属单质可以被氧化,也可以被还原 |
【知识点】 氧化还原反应基本概念 氧化还原反应的规律解读 金属通性
| A.有机物 | B.胶体 | C.混合物 | D.酸性氧化物 |
①铝溶于稀硫酸中:Al+2H+=Al3++H2↑
②将铁粉加入稀硫酸中:2Fe+6H+=2Fe3++3H2↑
③用食醋除去水瓶中的水垢:CO
 +2CH3COOH=2CH3COO-+CO2↑+H2O
+2CH3COOH=2CH3COO-+CO2↑+H2O④氯化钙与碳酸氢钾溶液反应:Ca2++CO
 =CaCO3↓
=CaCO3↓| A.①②③ | B.②③④ | C.①③④ | D.全部 |
【知识点】 离子方程式的正误判断解读
| A.Na2O | B.SiO2 | C.CO | D.SO2 |
【知识点】 酸、碱、盐、氧化物的概念及其相互联系解读 二氧化硅
 、Al3+和M离子,经测定Fe3+、SO
、Al3+和M离子,经测定Fe3+、SO 、Al3+和M离子的数目之比为2∶4∶1∶1,则M离子可能是下列中的 ( )
、Al3+和M离子的数目之比为2∶4∶1∶1,则M离子可能是下列中的 ( )| A.Na+ | B.OH- | C.S2- | D.Cl- |
【知识点】 离子共存 离子反应的实际应用 限定条件下的离子共存解读
| A.在反应2FeCl3+Cu=2FeCl2+CuCl2 中,利用了铜的氧化性 |
| B.在反应2Cu2O+Cu2S=6Cu+SO2↑中,只有Cu2O作氧化剂 |
C.5NH4NO3 4N2↑+2HNO3+9H2O中,发生氧化反应和发生还原反应的氮原子数目之比为5∶3 4N2↑+2HNO3+9H2O中,发生氧化反应和发生还原反应的氮原子数目之比为5∶3 |
| D.因Cl2的氧化性强于I2的氧化性,所以置换反应I2+2NaClO3=2NaIO3+Cl2↑不能发生 |
【知识点】 氧化还原反应基本概念 氧化还原反应的几组概念解读 氧化还原反应的应用
| A.H2S+H2SO4(浓)=S↓+SO2↑+2H2O:2e- |
B.3Cl2+6KOH 5KCl+KClO3+3H2O:5e- 5KCl+KClO3+3H2O:5e- |
| C.2Na2O2+2H2O=4NaOH+O2↑:4e- |
| D.2H2S+SO2=3S+2H2O:4e- |
【知识点】 氧化还原反应的几组概念解读 氧化还原反应有关计算
①过滤 ②加过量的NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液
| A.②④⑤①③ | B.④②⑤①③ | C.②⑤④①③ | D.⑤②④③① |
【知识点】 离子反应的实际应用 物质分离、提纯的常见化学方法解读
 2Fe+3CO2,下列有关该反应的说法正确的是
2Fe+3CO2,下列有关该反应的说法正确的是| A.反应前后氧元素化合价发生变化 | B.CO作还原剂 |
| C.Fe2O3发生氧化反应 | D.CO被还原 |
A.NH4HCO3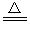 NH3↑+CO2↑+H2O NH3↑+CO2↑+H2O | B.2KMnO4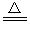 K2MnO4+MnO2+O2↑ K2MnO4+MnO2+O2↑ |
| C.Ca(OH)2+CO2=CaCO3↓+H2O | D.FeO+2HCl=H2O+FeCl2 |
【知识点】 氧化还原反应定义、本质及特征解读
| A.属于置换反应 | B.联氨是氧化剂 |
| C.联氨是还原剂 | D.氮气是氧化产物,不是还原产物 |
【知识点】 四种基本反应类型解读 氧化还原反应的几组概念解读
①H2SO3+I2+H2O=2HI+H2SO4
②2FeCl3+2HI=2FeCl2+2HCl+I2
③3FeCl2+4HNO3=2FeCl3+NO↑+2H2O+Fe(NO3)3
| A.H2SO3>HI>FeCl2>NO |
| B.NO>FeCl2>H2SO3>HI |
| C.I2>FeCl2>H2SO3>NO |
| D.FeCl2>HI>H2SO3>NO |
【知识点】 氧化性、还原性强弱的比较解读 氧化还原反应的规律解读
A.使酚酞溶液变红的溶液:Na+、Cl-、SO 、Fe3+ 、Fe3+ |
B.使紫色石蕊溶液变红的溶液:Fe2+、Mg2+、MnO 、Cl- 、Cl- |
| C.常温下pH<7的溶液:K+、Ba2+、Cl-、Br- |
D.碳酸氢钠溶液:K+、SO 、Cl-、H+ 、Cl-、H+ |
【知识点】 限定条件下的离子共存解读
 、
、 、
、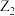 、
、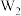 四种物质的氧化能力为
四种物质的氧化能力为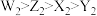 ,下列反应的化学方程式或叙述不成立的是
,下列反应的化学方程式或叙述不成立的是A.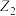 与 与 在水溶液中不能大量共存 在水溶液中不能大量共存 |
B. |
C.还原性: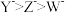 |
D.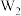 通入到 通入到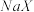 和 和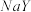 的混合溶液中: 的混合溶液中: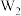 优先氧化 优先氧化 |
【知识点】 氧化性、还原性强弱的比较解读 氧化还原反应的规律解读
二、填空题 添加题型下试题
(1)上述物质中,属于纯净物的是
A.①②④ B.②④⑥ C.①②④⑤ D.全部
(2)上述干燥剂中②④⑤,其主要化学成分所属的类别依次为
A.酸 B.碱 C.盐 D.酸性氧化物 E碱性氧化物
(3)硅胶中无水氯化钴(CoCl2)呈蓝色,吸水后变为粉红色的CoCl2·6H2O,该变化过程属于
(4)为了能观察到丁达尔效应,某科学社的同学在实验室制备Fe(OH)3胶体。
①胶体与其他分散系的本质区别是:
②制备时,将
③如何设计实验验证制得的氢氧化铁是胶体:
(1)以上物质中能导电的是
(2)以上物质中属于电解质的是
(3)以上物质中属于非电解质的是
(4)写出⑤在水溶液中的电离方程式
(5)写出向⑥中加入⑨后发生反应的离子方程式
三、解答题 添加题型下试题
一个体重50 kg的健康人含铁2 g,这2 g铁在人体中以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是
A.Fe B.Fe2+ C.Fe3+
(2)工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有
A.Cl2 B.O2 C.FeCl3 D.KMnO4(H+)
(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有
(4)在Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了
【知识点】 氧化还原反应在生活、生产中的应用解读 Fe2+的还原性解读
试卷分析
试卷题型(共 38题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 电解质与非电解质 物质水溶液的导电性 | |
| 2 | 0.85 | 氧化还原反应基本概念 氧化还原反应的规律 | |
| 3 | 0.85 | 分散系概念及其分类 胶体的性质和应用 | |
| 4 | 0.85 | 电解质与非电解质 非电解质、电解质物质类别判断 | |
| 5 | 0.85 | 四种基本反应类型 碳元素及其化合物 | |
| 6 | 0.65 | 无机物质的分类 非电解质、电解质物质类别判断 几组常见同素异形体 | |
| 7 | 0.94 | 氧化还原反应定义、本质及特征 四种基本反应类型与氧化还原反应的关系 | |
| 8 | 0.85 | 氧化还原反应基本概念 | |
| 9 | 0.85 | 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系 | |
| 10 | 0.85 | 氧化还原反应基本概念 四种基本反应类型与氧化还原反应的关系 氧化性、还原性强弱的比较 氧化还原反应的规律 | |
| 11 | 0.85 | 分类方法的应用 酸、碱、盐、氧化物的概念及其相互联系 分散系概念及其分类 强电解质与弱电解质 | |
| 12 | 0.85 | 电离方程式 | |
| 13 | 0.94 | 电解质的电离 盐类水解的应用 | |
| 14 | 0.85 | 胶体的性质和应用 | |
| 15 | 0.85 | 离子方程式的书写 | |
| 16 | 0.85 | 基于氧化还原反应守恒规律的计算 | |
| 17 | 0.85 | 氧化还原反应的规律 | |
| 18 | 0.85 | 离子反应的发生条件 离子共存 限定条件下的离子共存 | |
| 19 | 0.85 | 离子反应概念 氧化还原反应基本概念 | |
| 20 | 0.85 | 氧化还原反应的应用 氧化还原反应的规律 | |
| 21 | 0.85 | 胶体的性质和应用 | |
| 22 | 0.65 | 氧化还原反应基本概念 氧化还原反应的规律 金属通性 | |
| 23 | 0.94 | 有机物通性 | |
| 24 | 0.65 | 离子方程式的正误判断 | |
| 25 | 0.85 | 酸、碱、盐、氧化物的概念及其相互联系 二氧化硅 | |
| 26 | 0.65 | 离子共存 离子反应的实际应用 限定条件下的离子共存 | |
| 27 | 0.65 | 氧化还原反应基本概念 氧化还原反应的几组概念 氧化还原反应的应用 | |
| 28 | 0.85 | 氧化还原反应的几组概念 氧化还原反应有关计算 | |
| 29 | 0.85 | 离子反应的实际应用 物质分离、提纯的常见化学方法 | |
| 30 | 0.85 | 氧化还原反应的几组概念 氧化还原反应在生活、生产中的应用 铁矿石与高炉炼铁 | |
| 31 | 0.85 | 氧化还原反应定义、本质及特征 | |
| 32 | 0.65 | 四种基本反应类型 氧化还原反应的几组概念 | |
| 33 | 0.85 | 氧化性、还原性强弱的比较 氧化还原反应的规律 | |
| 34 | 0.65 | 限定条件下的离子共存 | |
| 35 | 0.65 | 氧化性、还原性强弱的比较 氧化还原反应的规律 | |
| 二、填空题 | |||
| 36 | 0.85 | 树状分类法 胶体的定义及分类 胶体的性质和应用 胶体的制备 | |
| 37 | 0.65 | 电解质与非电解质 物质水溶液的导电性 电离方程式 | |
| 三、解答题 | |||
| 38 | 0.85 | 氧化还原反应在生活、生产中的应用 Fe2+的还原性 | 原理综合题 |







