河北省沧州市任丘市第一中学2020-2021学年高一上学期第一次阶段性测试化学试题
河北
高一
阶段练习
2020-10-24
241次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、化学实验基础、初中衔接知识点、物质结构与性质
一、单选题 添加题型下试题
| A.酸性氧化物:CO2、SiO2、SO2、CO |
| B.碱:烧碱、纯碱、苛性钾、氢氧化钡 |
| C.混合物:盐酸、水煤气、氢氧化铁胶体 |
| D.碱性氧化物:Na2O、CaO、MgO、Mn2O7 |
【知识点】 无机物质的分类
| A.Fe+CuSO4=FeSO4+Cu | B.3CO+Fe2O3 2Fe+3CO2 2Fe+3CO2 |
| C.AgNO3+NaCl=AgCl↓+NaNO3 | D.2KMnO4  K2MnO4+MnO2+O2↑ K2MnO4+MnO2+O2↑ |
 CO2
CO2 H2CO3
H2CO3 CaCO3
CaCO3 CO2其中涉及的基本反应类型依次为
CO2其中涉及的基本反应类型依次为| A.置换、化合、分解、复分解 | B.置换、化合、复分解、分解 |
| C.化合、置换、分解、复分解 | D.化合、置换、复分解、分解 |
A.H2SO4=H +SO +SO | B.Ca(OH)2=Ca2++(OH) |
| C.AlCl3=Al+3+3Cl- | D.Al2(SO4)3=2Al3++3SO |
①根据碳酸钠溶于水呈碱性,碳酸钠既属于盐,又属于碱。
②根据反应前后是否有化合价变化将化学反应分为氧化还原反应和非氧化还原反应
③根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和悬浊液
④电解质与非电解质的本质区别,是在水溶液或熔化状态下能否电离
| A.①③ | B.②④ | C.①④ | D.③④ |
| A.NaCl晶体、BaSO4 | B.液态的醋酸、酒精 |
| C.铜、二氧化硫 | D.熔融的KNO3、硫酸溶液 |
【知识点】 电解质、非电解质概念解读 非电解质、电解质物质类别判断解读
| A.氢氧化钠的摩尔质量是40 g |
| B.1 mol NaOH的质量是40 g/mol |
| C.1 g H2和1 g N2所含分子数相等 |
| D.阿伏加德罗常数个钠原子的质量是23g |
【知识点】 物质的量有关计算
A.1mol 所含质子数为10NA 所含质子数为10NA |
| B.10克氖气所含原子数约为6.02×1023 |
| C.标准状况下,22.4LSO2所含的分子数约为NA |
| D.常温常压下,32gO2和O3的混合气体所含原子数为NA |
A.1mol纯硫酸中含有NA个 离子 离子 |
| B.0.1mol硫酸钠中,含有0.2NA个Na+ |
| C.100g质量分数为46%的乙醇(C2H5OH)水溶液,含有NA个氧原子 |
| D.16.25gFeCl3溶于水形成的Fe(OH)3胶体粒子数为0.1NA |
| A.XY2 | B.X3Y2 | C.X2Y3 | D.XY |
【知识点】 阿伏加德罗定律 阿伏加德罗定律的应用解读
| A.1∶1∶1 | B.6∶4∶3 | C.4∶3∶2 | D.6∶3∶4 |
【知识点】 物质的量有关计算
| A.28V L/ mol | B.22.4 L/ mol | C.(28/V) L/ mol | D.(V/28) L/ mol |
| A.质子数之比为1∶1 | B.密度比为11∶8 |
| C.物质的量之比为8∶11 | D.原子个数比1∶1 |

| A.①是酒精,②是CCl4,③是苯 |
| B.①是酒精,②是苯,③是CCl4 |
| C.①是CCl4,②是苯,③是酒精 |
| D.①是苯,②是酒精,③是CCl4 |
| A.纳米Fe3O4磁流体分散系属于溶液 |
| B.纳米Fe3O4磁流体可以通过半透膜得到提纯 |
| C.当一束可见光通过该磁流体时会出现光亮的通路 |
| D.纳米Fe3O4磁流体比较稳定 |
①Ni+2HCl=NiCl2+H2↑ ②NiO+2HCl=NiCl2+H2O ③NiO2+4HCl=NiCl2+Cl2↑+2H2O
Ni(OH)2不溶于水。对上述反应的分析判断错误的是
| A.镍能与氯化铜溶液发生置换反应 |
| B.反应②和③都是复分解反应 |
| C.NiCl2能与NaOH溶液发生复分解反应 |
| D.反应①、③中Ni的化合价都发生了变化 |
【知识点】 物理变化与化学变化解读 四种基本反应类型解读 氧化还原反应基本概念
| A.蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 |
| B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D.萃取操作时,选择有机萃取剂,则溶质在萃取剂中的溶解度必须比原溶剂中大 |
| A.0.2mol、0.2mol、0.6mol | B.0.4mol、0.6mol、0.2mol |
| C.0.2mol、0.6mol、0.2mol | D.0.2mol、0.6mol、0.4mol |
A. | B. | C.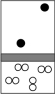 | D.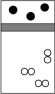 |
| 物质 | A | B | C | D |
| 反应前质量/g | 20 | 20 | 20 | 20 |
| 反应后质量/g | 20 | 28 | 22 | 10 |
| A.分解反应 | B.置换反应 | C.化合反应 | D.复分解反应 |
 2MO+4NO2↑+O2↑,加热29.6g M(NO3)2使其完全分解,在标准状况下收集11.2L的气体,那么M的摩尔质量是( )
2MO+4NO2↑+O2↑,加热29.6g M(NO3)2使其完全分解,在标准状况下收集11.2L的气体,那么M的摩尔质量是( )| A.64g/mol | B.24g/mol | C.65g/mol | D.40g/mol |
| A.1:3 | B.3:1 | C.5:6 | D.5:24 |
| 选项 | 目的 | 分离方法 | 原理 |
| A | 分离溶于水中的碘 | 乙醇萃取 | 碘在乙醇中的溶解度较大 |
| B | 分离水和乙醇 | 分液 | 水和乙醇的密度不同 |
| C | 除去KNO3固体中混杂的NaCl | 冷却结晶 | NaCl在水中的溶解度很大 |
| D | 除去丁醇中的乙醚 | 蒸馏 | 丁醇与乙醚的沸点相差较大 |
| A.A | B.B | C.C | D.D |

①4:1 ② 2:1 ③1:1 ④2:3
| A.①② | B.①④ | C.②③ | D.③④ |
【知识点】 阿伏加德罗定律及其推论解读 阿伏加德罗定律的应用解读
二、填空题 添加题型下试题
(1)下列物质中属于电解质的是
(2)上面的酸性氧化物与氢氧化钠反应的方程式
(3)将题中A物质溶于水配成饱和溶液,滴入沸水中,继续煮沸至出现红褐色可制得Fe(OH)3胶体,写出该过程的化学方程式
(4)写出下列物质的电离方程式:
KAl(SO4)2
KHSO3
NH4HSO4
Ca(OH)2
【知识点】 胶体的制备解读 电解质的电离 非电解质、电解质物质类别判断解读
三、解答题 添加题型下试题
材料一
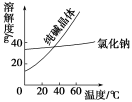
材料二
| 物质 | 熔点/℃ | 沸点/℃ | 密度/ g/cm3 | 溶解性 |
| 乙二醇(C2H6O2) | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
| 丙三醇(C3H8O3) | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
A.蒸馏法 B.萃取法
C.“溶解、结晶、过滤”的方法 D.分液法
①将纯碱从氯化钠和纯碱的混合物中分离出来,最好应用
②将乙二醇和丙三醇相互分离的最佳方法是
(2)阅读材料三
在溶解性方面,Br2(溴)与I2很相似,其稀的水溶液显黄色。在实验室里从溴水(Br2的水溶液)中提取Br2和提取I2的方法相似。
回答下列问题:
①常用的提取溴的方法是
②若观察发现提取Br2以后的水还有颜色,解决该问题的方法是
四、计算题 添加题型下试题
(2)标准状况下,将1g氦气、11g二氧化碳和4g氧气混合,该混合气体的体积约为
(3)agO2中含N个氧原子,则阿伏加 德罗常数为
(4)10gCaCO3能与含
(5)标准状况下,1.92g某气体的体积为672mL,则此气体的相对分子质量为
(6)标准状况下,某CO2和H2混合气体的密度为1.25g/L,则混合气体的平均摩尔质量为
(1)该混合气体总的物质的量为
(2)混合气体中碳原子的个数为
(3)若将该混合气体全部通过如图装置进行实验。(浓硫酸作用为除去水蒸气)

则:①气球中收集的气体质量为
②从A瓶中获得沉淀并测定其质量的操作是
③洗涤沉淀的方法为
【知识点】 物质的量有关计算 化学方程式计算中物质的量的运用解读
试卷分析
试卷题型(共 29题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 无机物质的分类 | |
| 2 | 0.94 | 氧化还原反应定义、本质及特征 四种基本反应类型与氧化还原反应的关系 | |
| 3 | 0.65 | 四种基本反应类型 | |
| 4 | 0.94 | 电离方程式 离子反应的发生条件 | |
| 5 | 0.65 | 分类方法的应用 分散系概念及其分类 电解质与非电解质 氧化还原反应基本概念 | |
| 6 | 0.85 | 电解质、非电解质概念 非电解质、电解质物质类别判断 | |
| 7 | 0.85 | 胶体的性质和应用 | |
| 8 | 0.85 | 物质的量有关计算 | |
| 9 | 0.85 | 阿伏加德罗常数的求算 结合气体物质与NA相关推算 结合物质结构基础知识与NA相关推算 | |
| 10 | 0.85 | 胶体的性质和应用 阿伏加德罗常数的求算 结合物质结构基础知识与NA相关推算 | |
| 11 | 0.85 | 阿伏加德罗定律 阿伏加德罗定律的应用 | |
| 12 | 0.94 | 物质的量有关计算 | |
| 13 | 0.85 | 气体摩尔体积 气体摩尔体积概念 物质的量有关计算 根据n=m/M进行相关计算 | |
| 14 | 0.85 | 阿伏加德罗定律及其推论 阿伏加德罗定律的应用 根据N=m·NA/M的相关推算 | |
| 15 | 0.65 | 溴、碘的性质 萃取和分液 | |
| 16 | 0.65 | 胶体的性质和应用 | |
| 17 | 0.65 | 物理变化与化学变化 四种基本反应类型 氧化还原反应基本概念 | |
| 18 | 0.85 | 化学实验基础操作 蒸发与结晶 蒸馏与分馏 萃取和分液 | |
| 19 | 0.85 | 某溶液与物质的量浓度相关的物理量的判断 物质的量有关计算 | |
| 20 | 0.65 | 阿伏加德罗定律的应用 根据n=N/NA进行相关计算 根据n=m/M进行相关计算 | |
| 21 | 0.94 | 四种基本反应类型 | |
| 22 | 0.65 | 摩尔质量的概念 22.4L/mol适用条件 根据n=m/M进行相关计算 物质的化学变化 | |
| 23 | 0.85 | 阿伏加德罗定律及其推论 原子中相关数值及其之间的相互关系 | |
| 24 | 0.65 | 物质分离、提纯的常见物理方法 蒸发与结晶 蒸馏与分馏 萃取和分液 | |
| 25 | 0.65 | 阿伏加德罗定律及其推论 阿伏加德罗定律的应用 | |
| 二、填空题 | |||
| 26 | 0.65 | 胶体的制备 电解质的电离 非电解质、电解质物质类别判断 | |
| 三、解答题 | |||
| 27 | 0.65 | 蒸馏与分馏 萃取和分液 过滤 | 实验探究题 |
| 四、计算题 | |||
| 28 | 0.65 | 气体摩尔体积 阿伏加德罗定律 根据n=N/NA进行相关计算 结合气体物质与NA相关推算 | |
| 29 | 0.85 | 物质的量有关计算 化学方程式计算中物质的量的运用 | |



