宁夏长庆高级中学2020-2021学年高一上学期期中考试化学试题1
宁夏
高一
期中
2020-12-01
227次
整体难度:
容易
考查范围:
化学实验基础、化学与STSE、常见无机物及其应用、认识化学科学、物质结构与性质、化学反应原理
一、单选题 添加题型下试题
A. | B. | C. | D. |
【知识点】 实验安全解读 工业固体废弃物的处理解读
| A.萃取 | B.渗析 | C.干馏 | D.蒸馏 |
【知识点】 物质的分离、提纯 物质分离、提纯的常见物理方法 蒸馏与分馏解读
 ,将粗盐溶于水,然后进行下列五项操作:①过滤,②加过量的NaOH溶液,③加适量盐酸,④加过量Na2CO3溶液,⑤加过量BaCl2溶液。正确的操作顺序是
,将粗盐溶于水,然后进行下列五项操作:①过滤,②加过量的NaOH溶液,③加适量盐酸,④加过量Na2CO3溶液,⑤加过量BaCl2溶液。正确的操作顺序是| A.①④②⑤③ | B.④①②⑤③ | C.②⑤④③① | D.⑤②④①③ |
【知识点】 卤素在自然界的存在解读 物质分离、提纯的常见化学方法解读
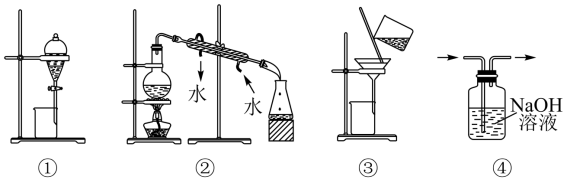
| A.分离植物油和氯化钠溶液选用① |
| B.除去氯化钠晶体中混有的氯化铵晶体选用② |
| C.分离四氯化碳中的溴单质选用③ |
| D.除去二氧化碳气体中的氯化氢气体选用④ |
| A.1 L溶液中K+浓度是0.4 mol·L−1 |
| B.500 mL溶液中含有0.1NA个K+ |
C.1 L溶液中所含K+、 总数为0.3NA 总数为0.3NA |
D.2 L溶液中 浓度是0.4 mol·L−1 浓度是0.4 mol·L−1 |
【知识点】 阿伏加德罗常数的求算解读 阿伏加德罗常数的应用解读
A. | B. | C. | D.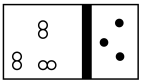 |
【知识点】 阿伏加德罗定律的应用解读 根据n=m/M的相关计算解读
| A.用蒸发皿进行结晶操作时,需垫石棉网才能加热 |
| B.洗涤沉淀的操作为边用玻璃棒搅拌边加蒸馏水冲洗漏斗内沉淀 |
| C.分液时打开旋塞,下层液体从下口放出,然后关闭旋塞,将上层液体从上口倒出 |
| D.蒸馏操作时,温度计应插入液体中以控制液体的温度 |
| A.150 mL 1 mol·L-1NaCl溶液 | B.75 mL 1 mol·L-1CaCl2溶液 |
| C.50 mL 3 mol·L-1MgCl2溶液 | D.150 mL 3 mol·L-1KCl溶液 |
A.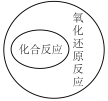 | B.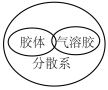 |
C.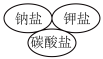 | D.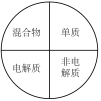 |
【知识点】 化学物质的分类方法
| A.同温同压下,相同体积的气体,其分子数一定相等,原子数也一定相等 |
| B.任何条件下,等物质的量的甲烷(CH4)和一氧化碳所含的原子数一定相等 |
| C.同温同压下的二氧化碳气体和氮气,若体积相等,则质量一定相等 |
| D.同温同压下,1L一氧化碳气体一定比1L氧气的质量小 |
| A.化合物:干冰、冰水混合物、烧碱 |
| B.同素异形体:石墨、C60、金刚石 |
| C.非电解质:乙醇、四氯化碳、氯气 |
| D.混合物:漂白粉、纯净矿泉水、盐酸 |
①将硫酸钡放入水中不能导电,所以硫酸钡是非电解质
②氨溶于水得到氨水溶液能导电,所以氨水是电解质
③固态HCl不导电,熔融态的HCl可以导电
④NaHSO4电离时生成的阳离子有氢离子,所以是酸
⑤电解质放在水中一定能导电,非电解质放在水中一定不导电
| A.仅①④ | B.仅①④⑤ |
| C.仅②③ | D.①②③④⑤ |
【知识点】 非电解质、电解质物质类别判断解读 物质水溶液的导电性解读
| A.稀盐酸滴在铜片上:Cu+2H+═Cu2++H2↑ |
| B.石灰石上滴加稀醋酸:CaCO3+2H+═Ca2++H2O+CO2↑ |
| C.氧化镁与稀盐酸混合:MgO+2H+═Mg2++H2O |
| D.铜片插入硝酸银溶液中:Cu+Ag+═Cu2++Ag |
| A.气溶胶的分散剂是气体 |
| B.根据分散质和分散剂的状态,可以将胶体分为9种 |
| C.气溶胶分散质粒子直径在1nm-100nm |
| D.胶体不能透过滤纸 |
| A.NaHSO4溶液与Ba(OH)2溶液混合 | B.NH4Cl溶液与Ca(OH)2溶液混合 |
| C.HNO3溶液与KOH溶液混合 | D.NaHCO3溶液与HCl溶液混合 |
| A.电解质与非电解质的本质区别,是在水溶液或熔化状态下能否电离 |
| B.强电解质与弱电解质的本质区别,是其水溶液导电性的强弱 |
| C.酸、碱和盐类都属于电解质,其他化合物都是非电解质 |
| D.常见的强酸、强碱和大部分盐都是强电解质,其他化合物都是非电解质 |
【知识点】 电解质、非电解质概念解读 强电解质与弱电解质解读
| A.KOH和CH3COONH4与Ba(OH)2与NH4Cl |
| B.AgNO3和HCl与Ag2CO3和HCl |
| C.BaCl2和Na2SO4与Ba(OH)2与H2SO4 |
| D.CH3COOH和Na2CO3与CH3COOH和NaHCO3 |
【知识点】 离子反应的发生及书写
| A.氧化还原反应的本质是元素化合价的升降 |
| B.氧化还原反应一定有氧元素参加 |
| C.有单质参与的反应一定是氧化还原反应 |
| D.发生氧化反应的物质也可能同时发生还原反应 |
 、Mg2+、SO
、Mg2+、SO 、Cl-、NO
、Cl-、NO 、HCO
、HCO 等离子。经检测废水呈强碱性,则可确定该厂废水中肯定不含有的离子组合是( )
等离子。经检测废水呈强碱性,则可确定该厂废水中肯定不含有的离子组合是( )A.Ag+、K+、NO 、HCO 、HCO | B.K+、NH 、NO 、NO 、SO 、SO |
C.Ag+、NH 、Mg2+、HCO 、Mg2+、HCO | D.K+、Mg2+、SO 、Cl- 、Cl- |
【知识点】 离子反应的发生条件解读 离子共存 离子反应在生活、生产中的应用解读
| A.肯定有Na2CO3,可能有CuSO4 | B.一定有NaCl,肯定没有Na2SO4 |
| C.一定有Na2CO3,可能有NaCl | D.可能有CaCl2,一定没有CuSO4 |
| A.3∶1∶1 | B.3∶2∶2 | C.1∶2∶3 | D.1∶3∶3 |
| A.Fe+CuSO4=FeSO4+Cu | B.3NaClO+NaI=NaIO3+3NaCl |
| C.Na2CO3+H2O+CO2=2NaHCO3 | D.Cl2+2FeCl2=2FeCl3 |
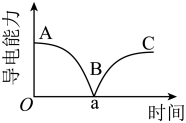
| A.AB段溶液的导电能力不断减弱,说明生成的BaSO4不是电解质 |
| B.B处溶液的导电能力约为0,说明溶液中几乎没有自由移动的离子 |
| C.BC段溶液的导电能力不断增大,主要是由于过量的H2SO4电离出的离子导电 |
| D.a时刻Ba(OH)2溶液与稀硫酸恰好完全中和 |
【知识点】 非电解质、电解质物质类别判断解读 物质水溶液的导电性解读
 、
、 、
、 、Al3+、Cu2+、Fe3+和K+中的若干种。为检验其中含有的离子,进行如下实验:取该溶液10mL,加入过量的氢氧化钡溶液并加热,产生使湿润的红色石蕊试纸变蓝色的气体,同时产生白色沉淀,过滤;向上述滤液中通入足量CO2气体,产生白色沉淀。下列关于原溶液的说法正确的是( )
、Al3+、Cu2+、Fe3+和K+中的若干种。为检验其中含有的离子,进行如下实验:取该溶液10mL,加入过量的氢氧化钡溶液并加热,产生使湿润的红色石蕊试纸变蓝色的气体,同时产生白色沉淀,过滤;向上述滤液中通入足量CO2气体,产生白色沉淀。下列关于原溶液的说法正确的是( )A.Al3+、 一定存在,Cl- 可能不存在 一定存在,Cl- 可能不存在 |
| B.至少存在4种离子 |
C. 、 、 至少含有一种 至少含有一种 |
| D.Al3+、Cu2+、Fe3+一定不存在,K+可能存在 |
二、填空题 添加题型下试题
【知识点】 非电解质、电解质物质类别判断解读 物质水溶液的导电性解读
三、解答题 添加题型下试题
下列各组混合物的分离或提纯应选用上述哪一种方法最合适?(填方法的标号)
(1)淀粉溶液中含有泥沙
(2)分离四氯化碳与水的混合物
(3)分离汽油和煤油
(4)KNO3晶体中含有少量食盐
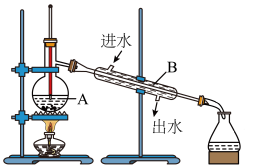
(1)改正图中的两处明显错误:
①
②
(2)写出仪器的名称:A
(3)实验时A中除加入自来水外,还需加入少量

【实验步骤】
(1)向沸水中加入几滴饱和 FeCl3溶液,继续煮沸至液体呈红褐色停止。
(2)把盛有 CuSO4溶液和 Fe(OH)3胶体的烧杯置于暗处,用红色激光笔照射两杯中的液体,观察现象。
【回答问题】
(1)Fe(OH)3胶体制备的化学方程式为:FeCl3+3H2O
 Fe(OH)3(胶体)+3HCl;该反应的离子方程式为
Fe(OH)3(胶体)+3HCl;该反应的离子方程式为(2)步骤 2 中能观察到的现象为
(3)若将实验改为向氯化铁溶液中加入氢氧化钠溶液,则会产生红褐色沉淀 Fe(OH)3,该反应的化学方程式为
| 硫酸 分子式:H2SO4 相对分子质量:98 密度:1.84g·cm-3 质量分数:98% |
(2)该学生需要量取
(3)配制时,其正确的操作顺序是(字母表示)
A.将容量瓶盖紧,颠倒摇匀
B.继续往容量瓶内小心加水,直到液面液面接近刻度线1~2cm处
C.将已冷却的硫酸沿玻璃棒注入容量瓶中
D.用少量水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.用量筒准确量取所需浓硫酸的体积,慢慢沿杯壁杯壁注入盛有少量水的烧杯中,用玻璃棒慢慢搅动,使其混合均匀
(4)若实验时遇到下列情况,将使溶液的浓度偏高的是
A.配制前容量瓶先用2 mol·L-1稀
 进行润洗;
进行润洗;B.定容时仰视刻度线;
C.容量瓶洗净后底部有蒸馏水而未作干燥处理;
D.溶液注入容量瓶前没有恢复到室温就进行定容;
E.定容、摇匀、静置后发现凹面低于刻度线又加水至刻度线
四、计算题 添加题型下试题
(1)从配制所得的溶液中取出50 mL,该50 mL的溶液中硫酸钠的物质的量浓度为:
(2)写出硫酸钠在水溶液中的电离方程式:
(3)14.2 g该固体中含有钠离子的数目是:
试卷分析
试卷题型(共 31题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 实验安全 工业固体废弃物的处理 | |
| 2 | 0.85 | 物质的分离、提纯 物质分离、提纯的常见物理方法 蒸馏与分馏 | |
| 3 | 0.65 | 卤素在自然界的存在 物质分离、提纯的常见化学方法 | |
| 4 | 0.65 | 物质分离、提纯的常见物理方法 物质分离、提纯的常见化学方法 | |
| 5 | 0.85 | 阿伏加德罗常数的求算 阿伏加德罗常数的应用 | |
| 6 | 0.85 | 阿伏加德罗定律的应用 根据n=m/M的相关计算 | |
| 7 | 0.94 | 蒸发与结晶 蒸馏与分馏 萃取和分液 过滤 | |
| 8 | 0.94 | 某溶液与物质的量浓度相关的物理量的判断 物质的量浓度计算-与溶质成分有关的计算 | |
| 9 | 0.65 | 化学物质的分类方法 | |
| 10 | 0.65 | 阿伏加德罗定律 以N=m·NA/M为中心的有关基本粒子的推算 | |
| 11 | 0.65 | 无机物质的分类 非电解质、电解质物质类别判断 几组常见同素异形体 | |
| 12 | 0.94 | 非电解质、电解质物质类别判断 物质水溶液的导电性 | |
| 13 | 0.65 | 离子反应的发生条件 离子方程式的书写 离子方程式的正误判断 溶度积 | |
| 14 | 0.65 | 胶体 胶体的性质和应用 | |
| 15 | 0.65 | 电离方程式 离子反应的发生条件 离子方程式的书写 离子方程式的正误判断 | |
| 16 | 0.65 | 电解质、非电解质概念 强电解质与弱电解质 | |
| 17 | 0.65 | 离子反应的发生及书写 | |
| 18 | 0.94 | 氧化还原反应基本概念 氧化还原反应定义、本质及特征 氧化还原反应的规律 | |
| 19 | 0.65 | 离子反应的发生条件 离子共存 离子反应在生活、生产中的应用 | |
| 20 | 0.65 | 离子反应的发生条件 离子反应在化合物组成的分析、鉴定的应用 常见阴离子的检验 物质检验和鉴别的实验方案设计 | |
| 21 | 0.65 | 物质的量浓度的计算 化学方程式中物质的量的运用 物质的量浓度与溶质成分有关的计算 | |
| 22 | 0.94 | 四种基本反应类型 氧化还原反应基本概念 氧化还原反应定义、本质及特征 四种基本反应类型与氧化还原反应的关系 | |
| 23 | 0.85 | 非电解质、电解质物质类别判断 物质水溶液的导电性 | |
| 24 | 0.85 | 摩尔质量 物质的量有关计算 | |
| 25 | 0.85 | 离子共存 离子反应的实际应用 铵根离子的检验 常见阳离子的检验 | |
| 二、填空题 | |||
| 26 | 0.65 | 非电解质、电解质物质类别判断 物质水溶液的导电性 | |
| 三、解答题 | |||
| 27 | 0.65 | 物质分离、提纯的常见物理方法 蒸发与结晶 萃取和分液 过滤 | 实验探究题 |
| 28 | 0.85 | 蒸馏与分馏 | 实验探究题 |
| 29 | 0.85 | 胶体的性质和应用 胶体的制备 物质性质实验方案的设计 | 实验探究题 |
| 30 | 0.65 | 配制一定物质的量浓度的溶液的步骤、操作 配制一定物质的量浓度的溶液实验的误差分析 配制一定物质的量浓度的溶液实验的仪器 配制一定物质的量浓度溶液的综合考查 | 实验探究题 |
| 四、计算题 | |||
| 31 | 0.65 | 物质的量有关计算 物质的量浓度的计算 电离方程式 | |



