安徽省肥东县高级中学2020-2021学年高一上学期第二次月考化学试题
安徽
高一
阶段练习
2020-10-25
334次
整体难度:
适中
考查范围:
认识化学科学、物质结构与性质、常见无机物及其应用、化学反应原理、化学实验基础
一、单选题 添加题型下试题
选项 | 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 |
A | NaOH | HNO3 | NaHCO3 | CaO | CO2 |
B | Fe(OH)3 | HCl | NaCl | K2O | CO |
C | Cu2(OH)2CO3 | HF | CaCO3 | CaO | SO2 |
D | NaOH | CH3COOH | CaF2 | K2O | CO |
| A.A | B.B | C.C | D.D |
【知识点】 酸、碱、盐、氧化物的概念及其相互联系解读
 ”表示氧原子,“
”表示氧原子,“ ”表示碳原子,“
”表示碳原子,“ ”表示氢原子,则该化学反应中不存在的物质种类是
”表示氢原子,则该化学反应中不存在的物质种类是
| A.单质 | B.氧化物 | C.盐 | D.有机物 |
【知识点】 无机物与有机物解读 物质结构与性质综合考查解读

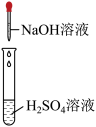
| A.水进入左瓶 | B.水进入右瓶 |
| C.水同时进入两瓶 | D.水不进入任何一瓶 |
【知识点】 阿伏加德罗定律 钠的化学性质 钠与氧气等非金属的反应解读
| A.钠着火后,可用泡沫灭火器来灭火 |
| B.氧化钠和过氧化钠都属于碱性氧化物 |
| C.氧化钠和过氧化钠的组成元素相同,都可以与CO2反应且产物相同 |
| D.用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧,说明CO2、H2O与Na2O2的反应是放热反应 |
| A.84消毒液的有效成分是HCl |
| B.氯气既是氧化产物又是还原产物,氯化钠是还原产物 |
| C.每生成1molCl2,氧化剂NaClO共失去电子数为1NA |
| D.若有0.1molHCl被氧化,生成的氯气在标准状况下的体积为2.24L |
A. |
B.2NaHCO3 Na2CO3+CO2↑+H2O Na2CO3+CO2↑+H2O |
C. |
| D.2Na2O2+2H2O=4NaOH+O2↑ |
【知识点】 四种基本反应类型解读 氧化还原反应定义、本质及特征解读
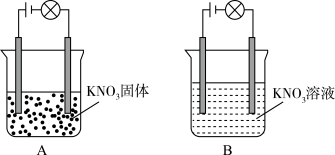
| A.硝酸钾固体不是电解质 |
| B.硝酸钾溶液是电解质 |
| C.硝酸钾在水溶液中电离出了可以自由移动的离子 |
| D.在硝酸钾溶液中,水电离出了大量的离子 |
A.NaHCO3===Na++H++ | B.(NH4)2SO4=== + + |
C.NH4Cl=== +Cl- +Cl- | D.Ba(OH)2===Ba2++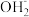 |
【知识点】 电离方程式解读 离子反应的发生及书写
二、未知 添加题型下试题
①将硫酸钡放入水中不能导电,所以硫酸钡是非电解质
②氨溶于水得到的溶液氨水能导电,所以氨水是电解质
③固态HCl不导电,熔融态的HCl可以导电
④NaHSO4电离时生成的阳离子有氢离子,所以是酸
⑤电解质溶于水中一定能导电,非电解质溶于水中一定不导电
| A.①④ | B.①④⑤ | C.①②③④ | D.①②③④⑤ |
三、单选题 添加题型下试题
| A.强电解质溶液的导电性一定比弱电解质溶液的导电性强 |
| B.稀盐酸溶液能导电,所以稀盐酸是电解质 |
| C.二氧化硫溶于水能导电,故二氧化硫属于电解质 |
| D.硫酸钡虽然难溶于水,但硫酸钡属于电解质 |
阳离子 |
|
阴离子 | OH-、 |
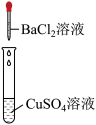
| A.甲中一定含有Na+ | B.乙中一定含有 |
| C.丙中一定含有Mg2+ | D.丙中一定含有 |
| A.向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体 |
| B.“血液透析”利用了胶体的性质 |
| C.明矾能生成Al(OH)3胶体,可用作净水剂 |
| D.用平行光照射NaCl溶液和Fe(OH)3胶体时,产生的现象相同 |
编号 | I | II | III |
实验装置 |
|
|
|
现象 | 没有明显变化,溶液仍为无色 | 有白色沉淀生成,溶液为蓝色 | 有无色气体放出 |
| A.I中无明显变化,说明两溶液不反应 |
| B.II 中的白色沉淀为CuCl2 |
| C.III中的离子方程式为2H++Zn=Zn2++H2↑ |
| D.I中发生的反应不是离子反应 |
A.K+、MnO 、Na+、Cl- 、Na+、Cl- | B.K+、Na+、NO 、CO 、CO |
C.Na+、H+、NO 、SO 、SO | D.Fe3+、Na+、Cl-、SO |
【知识点】 离子共存 限定条件下的离子共存解读
A.某溶液中加入硝酸银溶液生成白色沉淀,说明原溶液中一定有 离子 离子 |
B.某溶液中加入盐酸酸化的氯化钡溶液生成白色沉淀,说明原溶液中一定有SO 离子 离子 |
C.某溶液中加入氢氧化钠溶液生成蓝色沉淀,说明原溶液中一定有 离子 离子 |
D.某溶液中加入稀硫酸产生无色无味气体,说明原溶液中一定有CO 离子 离子 |
四、填空题 添加题型下试题
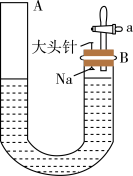
(1)钠与水反应的化学方程式为
(2)钠与水反应的现象有很多,不同的现象证明不同的性质。
①能证明钠的密度比水小的现象是
②能证明钠的熔点低的现象是
③能证明有氢氧化钠生成的现象是
④能证明有气体产生的现象是A端液面
(1)下列生产、生活中的事例中没有发生氧化还原反应的是
a. 海水提溴 b. 工业制氯碱 c. 海水晒盐 d. 海带提碘
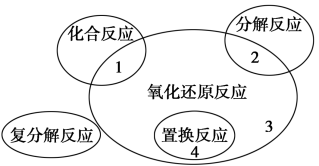
(2)水是人体的重要组成部分,是人体中含量最多的一种物质。“四种基本反应类型与氧化还原反应的关”可用下图表示。
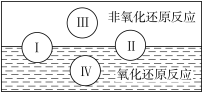
试写出有水参加且符合反应类型 IV 的一个化学方程式:
(3)工业上利用 NaIO3和 NaHSO3反应来制取单质 I2。
①配平下列化学方程式并标明电子转移的方向和数目:
②该反应还原剂是
(4)已知:HSO3-、I2、I-、SO42-和一些未知物组成的一个氧化还原反应,其中SO42-是氧化产物,该反应中还原性HSO3-
(1)写出制备Fe(OH)3胶体的化学方程式:
(2)氢氧化铁胶体中粒子直径大小的范围是
(3)你认为可以用什么方法判断胶体制备是否成功?
(4)在做制备氢氧化铁胶体的实验时,甲同学没有选用饱和氯化铁溶液,而是用稀氯化铁溶液滴入沸水中,结果没有观察到
(5)乙同学画出了在实验室中进行胶体的丁达尔效应实验的示意图,该实验室里的空气十分洁净。下图中的一处明显错误是

(6)丁同学取烧杯中的少量Fe(OH)3胶体置于试管中,向试管中滴加一定量的稀盐酸,边滴边振荡,可看到溶液中的红褐色逐渐变浅,最终又得到棕黄色的FeCl3溶液,发生此变化的化学方程式为
试卷分析
试卷题型(共 19题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 酸、碱、盐、氧化物的概念及其相互联系 | |
| 2 | 0.65 | 无机物与有机物 物质结构与性质综合考查 | |
| 3 | 0.65 | 钠的化学性质 钠与盐溶液的反应 | |
| 4 | 0.65 | 阿伏加德罗定律 钠的化学性质 钠与氧气等非金属的反应 | |
| 5 | 0.65 | 钠的化学性质 过氧化钠 | |
| 6 | 0.65 | 氧化还原反应的几组概念 氧化还原反应的应用 氧化还原反应有关计算 氧化还原反应在生活、生产中的应用 | |
| 7 | 0.65 | 四种基本反应类型 氧化还原反应定义、本质及特征 | |
| 8 | 0.65 | 电解质的电离 物质水溶液的导电性 | |
| 9 | 0.94 | 电离方程式 离子反应的发生及书写 | |
| 11 | 0.65 | 非电解质、电解质物质类别判断 物质水溶液的导电性 强电解质与弱电解质 | |
| 12 | 0.85 | 离子共存 离子反应的实际应用 离子反应在化合物组成的分析、鉴定的应用 | |
| 13 | 0.85 | 分散系概念 胶体的定义及分类 胶体的性质和应用 胶体的制备 | |
| 14 | 0.65 | 离子反应概念 离子方程式的书写 物质性质实验方案的设计 | |
| 15 | 0.65 | 离子共存 限定条件下的离子共存 | |
| 16 | 0.65 | 氯离子的检验 硫酸根离子的检验 离子的检验 | |
| 二、未知 | |||
| 10 | 0.85 | 酸、碱、盐、氧化物的概念及其相互联系 电解质与非电解质 非电解质、电解质物质类别判断 | 未知 |
| 三、填空题 | |||
| 17 | 0.94 | 钠与水反应原理 化学实验探究 物质性质的探究 | |
| 18 | 0.65 | 氧化还原反应方程式的配平 氧化还原反应在生活、生产中的应用 氧化还原反应的规律 亚硫酸及其盐 | |
| 19 | 0.65 | 胶体 胶体的性质和应用 胶体的制备 | |

 、
、