吉林省长春外国语学校2020-2021学年高一上学期第一次月考化学(理)试题
吉林
高一
阶段练习
2020-10-01
612次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、化学反应原理
一、单选题 添加题型下试题
| A.硫酸、纯碱、孔雀石 | B.硝酸、烧碱、纯碱 |
| C.冰醋酸、乙醇、醋酸钠 | D.盐酸、熟石灰、苛性钠 |
①由一种元素组成的物质一定是纯净物
②冰水混合物是纯净物
③
 是混合物
是混合物④酸性氧化物一定是非金属氧化物,非金属氧化物不一定是酸性氧化物
⑤碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物
| A.①和④ | B.②和⑤ | C.③和④ | D.全部 |
| A.用激光笔照射该液体,会出现丁达尔效应 |
| B.将液体静置片刻,会出现沉淀现象 |
| C.所得分散系中分散质的粒子直径大于100 nm |
| D.用滤纸可实现该分散系中分散剂与分散质的分离 |
①根据氧化物的性质将氧化物分成酸性氧化物、碱性氧化物和两性氧化物等
②根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应
③根据分散系是否有丁达尔效应将分散系分为溶液、胶体和浊液
④根据组成元素的种类将纯净物分为单质和化合物
⑤根据电解质的水溶液导电能力的强弱将电解质分为强电解质和弱电解质
| A.②④⑤ | B.②③④ | C.①③⑤ | D.①②④ |
| A.氨水能导电,所以氨气是电解质 |
| B.盐酸是强电解质,所以导电能力比醋酸溶液强 |
| C.氯化银难溶于水,所以氯化银是非电解质 |
| D.蔗糖溶液和熔融的蔗糖都不能导电,所以蔗糖是非电解质 |
| A.Zn→ZnSO4 | B.CaCO3→CO2 | C.MgO→MgCl2 | D.BaCl2→BaSO4 |
【知识点】 物质的转化 含硫化合物之间的转化解读
| A.固体NaCl不存在阴阳离子,不导电 |
| B.Na2O、Fe2O3、CO2均属于碱性氧化物 |
| C.硫酸钡溶液几乎不导电,但硫酸钡属于电解质 |
| D.金刚石和石墨是同素异形体,化学性质不同,物理性质相同 |
【知识点】 非电解质、电解质物质类别判断解读 物质水溶液的导电性解读
A.Na+、K+、SO 、Cl- 、Cl- | B.Cu2+、 K+、SO 、NO 、NO |
C.H+、K+、HCO 、Cl- 、Cl- | D.Mg2+、 Na+、Cl-、SO |
| A.Cu(OH)2和盐酸;Cu(OH)2和CH3COOH |
| B.BaCl2和Na2SO4;Ba(OH)2和CuSO4 |
| C.NaHCO3和H2SO4;Na2CO3 和NaHSO4 |
| D.石灰石与硝酸;碳酸钙与盐酸 |
2R(OH)3+ 3C1O-+ 4OH-= 2RO4n-+3Cl-+5H2O。则RO4n-中R的化合价是()
| A.+3 | B.+4 | C.+5 | D.+6 |
【知识点】 离子反应的发生及书写
| A.离子反应一定是离子与离子之间的反应 |
| B.电解质溶液之间发生的反应均为离子反应 |
| C.在溶液中有离子参加的化学反应是离子反应 |
| D.离子反应均能用离子方程式表示 |
A.H+、K+、Fe3+、SO | B.Ba2+、Ca2+、OH-、CO |
C.H+、Na+、NO 、Cu2+、 、Cu2+、 | D.Mg2+、Na+、Cl-、SO |
【知识点】 限定条件下的离子共存解读
A.碳酸钙与盐酸的反应:  +2H+=CO2↑+H2O +2H+=CO2↑+H2O |
| B.硫酸溶液与氢氧化钡溶液的反应: H++OH-=H2O |
C.硝酸银与氯化钠溶液的反应:AgNO3 +Cl-=AgCl↓+ |
| D.铝与硫酸铜溶液的反应:2Al+3Cu2+=2A13++3Cu |
【知识点】 离子方程式的正误判断解读
A.熔融状态下NaHSO4的电离:NaHSO4=Na++H++SO |
| B.水溶液中Ba(OH)2的电离:Ba(OH)2=Ba2++OH- |
C.水溶液中NaHCO3的电离:NaHCO3=Na++HCO |
D.水溶液中Al2(SO4)3的电离: Al2(SO4)3=3Al3++3SO |
| A.失去电子的反应是还原反应 | B.作氧化剂的物质不能是还原剂 |
| C.发生氧化反应的物质是氧化剂 | D.失去电子的物质是还原剂 |
【知识点】 氧化还原反应基本概念 氧化还原反应的几组概念解读
| A.2NaBr+Cl2= 2NaCl+Br2 |
| B.AlCl3+3NaAlO2+6H2O=4Al(OH)3↓+3NaCl |
| C.2H2S+SO2= 2H2O+3S↓ |
| D.C+H2O=CO+H2 |
【知识点】 氧化还原反应定义、本质及特征解读 氧化还原反应的规律解读
①2Na2O2+2H2O=4NaOH+O2↑②4Fe(OH)2+O2+2H2O=4Fe(OH)3③2F2+2H2O=4HF+O2④2Na+2H2O=2NaOH+H2↑
| A.①③ | B.①④ | C.③④ | D.②④ |
【知识点】 氧化还原反应的几组概念解读
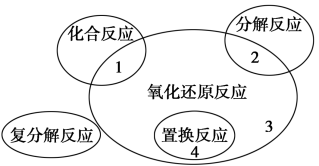
A. |
B.2NaHCO3 Na2CO3+CO2↑+H2O Na2CO3+CO2↑+H2O |
C. |
| D.2Na2O2+2H2O=4NaOH+O2↑ |
【知识点】 四种基本反应类型解读 氧化还原反应定义、本质及特征解读
A.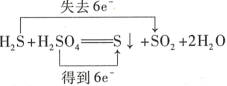 |
B. |
C.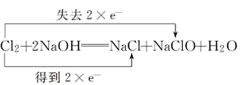 |
D. |
【知识点】 单线桥、双线桥分析氧化还原反应解读
| A.2:1 | B.1:4 | C.3:1 | D.1:3 |
【知识点】 氧化还原反应有关计算 与氧化剂、还原剂有关的计算解读
| A.Br2+2HI=I2+2HBr |
| B.2FeCl2+Cl2=2FeCl3 |
| C.2FeCl2+2HCl+I2=2FeCl3+2HI |
| D.Cl2通入NaBr和NaI的混合溶液中:I-先被氧化 |
【知识点】 氧化性、还原性强弱的比较解读
二、填空题 添加题型下试题
(1)可以导电的有
(2)属于电解质的有
(3)属于非电解质的有
(4)②在水中的电离方程式为
【知识点】 电解质的电离 电解质、非电解质概念解读 电离方程式解读
(1)已知
 中铬元素是+3价,则其中铁元素是
中铬元素是+3价,则其中铁元素是 是一种酸根离子,则
是一种酸根离子,则 属于
属于(2)明胶的水溶液和
 溶液共同具备的性质是
溶液共同具备的性质是a.都不稳定,密封放置沉淀
b.能产生丁达尔效应
c.分散质粒子可通过滤纸
(3)现有10mL明胶的水溶液与5mL
 溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明
溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明 能够透过半透膜:
能够透过半透膜:(1)请将上述化学方程式改写为离子方程式:
(2)浓盐酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)此反应中氧化产物是
(4)用单线桥法表示该反应电子转移的方向和数目:
三、解答题 添加题型下试题
 、CO
、CO 、OH-中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水但溶于盐酸并放出无色无味的气体E;③C的水溶液呈碱性,与稀硫酸反应生成A;④D可溶于水,与稀硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
、OH-中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水但溶于盐酸并放出无色无味的气体E;③C的水溶液呈碱性,与稀硫酸反应生成A;④D可溶于水,与稀硫酸作用时放出气体E,E可使澄清石灰水变浑浊。(1)推断A、C的化学式:A
(2)写出下列反应的离子方程式。
①D与氯化钙反应:
②B与盐酸反应:
③C与稀硫酸反应:
试卷分析
试卷题型(共 27题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 分类方法的应用 酸、碱、盐、氧化物的概念及其相互联系 | |
| 2 | 0.65 | 无机物质的分类 酸、碱、盐、氧化物 | |
| 3 | 0.65 | 分散系概念及其分类 胶体的性质和应用 | |
| 4 | 0.65 | 无机物质的分类 分散系概念 | |
| 5 | 0.85 | 电解质与非电解质 电解质、非电解质概念 非电解质、电解质物质类别判断 物质水溶液的导电性 | |
| 6 | 0.65 | 物质的转化 含硫化合物之间的转化 | |
| 7 | 0.65 | 非电解质、电解质物质类别判断 物质水溶液的导电性 | |
| 8 | 0.85 | 离子共存 限定条件下的离子共存 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 | |
| 9 | 0.85 | 离子方程式的书写 | |
| 10 | 0.85 | 离子反应的发生及书写 | |
| 11 | 0.85 | 离子反应概念 | |
| 12 | 0.85 | 物质水溶液的导电性 离子反应的发生条件 | |
| 13 | 0.65 | 限定条件下的离子共存 | |
| 14 | 0.85 | 离子方程式的正误判断 | |
| 15 | 0.85 | 电离的定义 电离方程式 | |
| 16 | 0.85 | 氧化还原反应基本概念 氧化还原反应的几组概念 | |
| 17 | 0.65 | 氧化还原反应的规律 含硫化合物之间的转化 | |
| 18 | 0.65 | 氧化还原反应定义、本质及特征 氧化还原反应的规律 | |
| 19 | 0.85 | 氧化还原反应的几组概念 | |
| 20 | 0.65 | 四种基本反应类型 氧化还原反应定义、本质及特征 | |
| 21 | 0.85 | 单线桥、双线桥分析氧化还原反应 | |
| 22 | 0.85 | 氧化还原反应有关计算 与氧化剂、还原剂有关的计算 | |
| 23 | 0.85 | 氧化性、还原性强弱的比较 | |
| 二、填空题 | |||
| 24 | 0.85 | 电解质的电离 电解质、非电解质概念 电离方程式 | |
| 25 | 0.85 | 酸、碱、盐、氧化物的概念及其相互联系 胶体的性质和应用 硫酸根离子的检验 | |
| 26 | 0.65 | 氧化还原反应的几组概念 单线桥、双线桥分析氧化还原反应 氧化性、还原性强弱的比较 | |
| 三、解答题 | |||
| 27 | 0.85 | 离子方程式的书写 离子反应在化合物组成的分析、鉴定的应用 | 无机推断题 |







