河北省辛集一中2018-2019学年高二下学期返校考试化学试题
河北
高二
阶段练习
2019-03-12
604次
整体难度:
适中
考查范围:
常见无机物及其应用、认识化学科学、化学实验基础、物质结构与性质、有机化学基础、化学与STSE、化学反应原理
一、单选题 添加题型下试题
| A.铝粉与氧化镁共热可制取金属镁 |
| B.足量铝分别与含1 mol HCl、1 mol NaOH的溶液反应,产生相同量的氢气 |
| C.工业上用电解熔融Al2O3的方法冶炼铝 |
| D.在浓硝酸中加入等体积的浓硫酸后,立即加入铝片,铝片表面发生钝化 |
 ,关于氢铝化合物的推测不正确的是( )
,关于氢铝化合物的推测不正确的是( )A.氢铝化合物中铝显 价,氢显 价,氢显 价 价 |
| B.氢铝化合物与水反应生成氢氧化铝和氢气 |
| C.铝与水蒸气高温下反应生成氢铝化合物 |
| D.氢铝化合物具有强还原性 |
| A.Al | B.Al(OH)3 | C.AlCl3 | D.Al2O3 |
| A.K+、Na+、HCO3-、NO3- | B.Na+、SO42-、Cl-、S2- |
| C.NH4+、Mg2+、SO42-、NO3- | D.H+、K+、Cl-、Na+ |
【知识点】 离子共存 限定条件下的离子共存解读

下列叙述正确的是
| A.按上述流程,试剂X可以是氢氧化钠溶液,也可以是盐酸 |
| B.反应①过滤后所得沉淀为氧化铁 |
| C.图中所有的转化反应都不是氧化还原反应 |
| D.反应②的离子方程式为2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| A.1 mol•L﹣1 | B.1.5 mol•L﹣1 | C.2 mol•L﹣1 | D.2.5 mol•L﹣1 |
【知识点】 物质的量浓度的计算 化学方程式计算中物质的量的运用解读 镁 铝
①SiO2 ②Al ③Al2O3 ④Al(OH)3 ⑤Na2CO3溶液⑥Ca(HCO3)2溶液 ⑦NH4HCO3溶液 ⑧KHSO4溶液
| A.②③④⑥⑦ | B.①②③④⑦ | C.④⑥⑦⑧ | D.②③④⑤⑧ |
二、未知 添加题型下试题
三、单选题 添加题型下试题
 氧化产物为
氧化产物为 、
、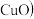 共
共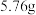 ,经如下处理,下列说法正确的是
,经如下处理,下列说法正确的是


A.滤液A中的阳离子为 、 、 、 、 |
B.样品中Fe元素的质量为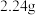 |
C.样品中CuO的质量为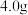 |
D. |
| A.6.4g | B.4.8g | C.2.4g | D.1.6g |
【知识点】 铁及铁的氧化物混合物反应的相关计算解读
①铁能被磁铁吸引,但纯铁易被腐蚀 ②在人体内的血红蛋白中含有铁元素 ③铁位于元素周期表中第四周期第ⅧB族 ④铁能在氧气中剧烈燃烧,但不能在水蒸气中燃烧 ⑤铁与强氧化剂硝酸反应的产物仅是Fe(NO3)3 ⑥不能通过化合反应制得FeCl2和Fe(OH)3
| A.①③ | B.②④ | C.②⑤ | D.④⑥ |
【知识点】 铁
| A.从HF、HCl、HBr、HI酸性递增的事实,可推出F、Cl、Br、I的非金属性递增的规律 |
| B.HF、HCl、HBr、HI的热稳定性依次减弱,还原性依次增强 |
| C.淀粉-碘化钾溶液在空气中变蓝,4I-+O2+2H2O===2I2+4OH- |
| D.碘在碘化钾溶液中的溶解度大于在纯水中的溶解度 |
| A.H2O | B.Zn | C.KI | D.KCl |
【知识点】 溴、碘的性质 其他含卤化合物 物质分离、提纯综合应用解读
| A.氯气除杂过程中通入浓硫酸中 |
| B.浓硫酸与木炭共热 |
| C.乙酸乙酯与稀硫酸共热 |
| D.浓硫酸滴到蔗糖中制“黑面包” |
【知识点】 氧族元素及其化合物
①Ca(OH)2 ②BaCl2 ③NaAlO2 ④Na2SiO3 ⑤Ba(NO3)2 ⑥苯酚钠 ⑦Na2CO3
| A.①②④⑦ | B.②③⑥⑦ | C.④⑤⑥⑦ | D.③④⑤⑥ |
【知识点】 二氧化硫的化学性质
| A.二氧化硫气体能用浓硫酸干燥,是因为二氧化硫无还原性 |
| B.医疗上可用硫酸钡作X射线透视肠胃的内服药,是因为硫酸钡不溶于酸 |
| C.向50 mL 18 mol·L-1的H2SO4溶液中加入足量的铜片加热充分反应后,被还原的H2SO4的物质的量等于0.45 mol |
| D.常温下,浓H2SO4可以用铝制容器贮存,说明铝与浓H2SO4不反应 |
| A.铜与浓硫酸共热 |
| B.用铜片为阳极,石墨为阴极,电解稀硫酸 |
| C.先灼烧废铜屑生成氧化铜,然后再用浓硫酸溶解 |
| D.适当温度下,使铜片在持续通入空气的稀硫酸中溶解 |
| A.NH4Cl和NH4HCO3受热都能分解,说明可以用加热NH4Cl或NH4HCO3固体的方法制氨气 |
| B.向溶液中滴加酸化的Ba(NO3)2溶液出现白色沉淀,说明该溶液中一定有SO42- |
| C.Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应 |
| D.分别将充满HCl、NH3的烧瓶倒置于水中,液面均迅速上升,说明二者均易溶于水 |
| A.在稀硫酸中加入铜粉,铜粉不溶解,再加入Cu(NO3)2固体,铜粉仍不溶解 |
| B.某气体能使湿润的红色石蕊试纸变蓝,该气体的水溶液一定显碱性 |
| C.铜与稀硝酸反应的离子方程式为3Cu+8H++2NO3-===3Cu2++2NO↑+ 4H2O |
| D.HNO3→NO→NO2,以上各步变化均能通过一步实现 |
| A.酒精能使蛋白质变性,可用于杀菌消毒 |
| B.CaO能与SO2反应,可作工业废气的脱硫剂 |
| C.明矾水解时产生具有吸附性的胶体粒子,可作漂白剂 |
| D.镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料 |
| A.化合反应均为氧化还原反应 |
| B.金属氧化物均为碱性氧化物 |
| C.催化剂能改变可逆反应达到平衡的时间 |
| D.石油是混合物,其分馏产品汽油为纯净物 |
【知识点】 物质的分类 氧化还原反应基本概念 化石能源
①硫酸铝 ②小苏打 ③氯化亚铁 ④氢氧化铜 ⑤氢氧化铁 ⑥磁性氧化铁
| A.3种 | B.4种 | C.5种 | D.6种 |
| A.闪电 | B.光化学烟雾 |
| C.酸雨 | D.臭氧层空洞 |
【知识点】 化学与环境保护
| A.②比①多 | B.①比②多 |
| C.一样多 | D.无法判断 |
【知识点】 化学方程式计算中物质的量的运用解读 氯气的实验室制法解读
| A.在标准状况下,2.24 L HF含有的电子数为NA |
| B.7.8 g Na2S和Na2O2的混合物中所含离子数为0.3NA |
| C.常温下,2.7 g铝片投入足量的浓硫酸中,铝失去的电子数为0.3NA |
| D.电解精炼铜时,阳极质量每减少32 g,电路中就转移NA个电子 |
| A.6.8 g熔融的KHSO4中含有0.05 NA个阴离子 |
| B.1.0 L 2 mol/L的NaOH水溶液中含有的氧原子数目为2NA |
| C.25℃时,p H=13的氢氧化钡溶液中含有0.1 NA个OH— |
| D.5.6g铁与一定量稀硝酸完全反应,电子转移数目一定为0.3 NA |
【知识点】 阿伏加德罗常数的求算解读
①250 mL容量瓶 ②托盘天平 ③烧瓶 ④胶头滴管 ⑤烧杯 ⑥玻璃棒 ⑦试管 ⑧药匙
| A.①④⑤⑥ | B.①②④⑤ |
| C.①②④⑤⑥⑧ | D.全部 |
| A.0.37 mol | B.0.63 mol | C.0.74 mol | D.1.5 mol |
【知识点】 根据n=m/M的相关计算解读
| A.向NaHCO3溶液中加入过量的Ba(OH)2溶液:2HCO3-+Ba2++2OH-===BaCO3↓+2H2O+CO32- |
B.用铁电极电解饱和食盐水:2Cl-+2H2O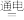 2OH-+H2↑+Cl2↑ 2OH-+H2↑+Cl2↑ |
| C.向NaNO2溶液中加入酸性KMnO4溶液:2MnO4-+5NO2-+6H+===2Mn2++5NO3-+3H2O |
| D.向Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-===2Fe2++I2 |
【知识点】 离子方程式的书写解读 氧化还原反应方程式的配平解读
| A.饱和碳酸钠溶液中通入足量的二氧化碳:2Na++CO32-+CO2+H2O=2NaHCO3↓ |
| B.FeI2溶液中滴入过量溴水:2Fe2++2I-+2Br2=2Fe3++I2+4Br- |
| C.NaHSO4溶液中滴入少量Ba(OH)2溶液:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
| D.饱和石灰水与醋酸溶液混合:Ca(OH)2+2CH3COOH=Ca2++2CH3COO-+2H2O |
【知识点】 离子反应的发生及书写
| A.液态 HBr 不导电,因此 HBr 是非电解质 |
| B.强电解质溶液的导电能力不一定比弱电解质溶液的导电能力强 |
| C.NH3的水溶液能导电,因此NH3是电解质 |
| D.BaSO4难溶于水,其水溶液的导电性极弱,因此BaSO4是弱电解质 |
| A.M | B.M2+ | C.M3+ | D.MO2+ |
【知识点】 氧化还原反应有关计算 基于氧化还原反应守恒规律的计算解读
| A.ClO2 | B.Cl2O | C.Cl2 | D.Cl2O3 |
【知识点】 氧化还原反应的规律解读 与氧化剂、还原剂有关的计算解读
2R(OH)3+ 3C1O-+ 4OH-= 2RO4n-+3Cl-+5H2O。则RO4n-中R的化合价是()
| A.+3 | B.+4 | C.+5 | D.+6 |
【知识点】 离子反应的发生及书写
四、填空题 添加题型下试题
①非金属元素构成的单质中一定存在共价键; ②非金属之间形成的化合物一定是共价化合物;③非金属的气态氢化物中一定存在极性共价键;④离子化合物中一定含有离子键;⑤金属元素和非金属元素形成的化合物一定是离子化合物;⑥在一种化合物中只能存在一种类型的化学键;⑦含共价键的化合物不一定是共价化合物;⑧含离子键的化合物一定是离子化合物;⑨氯化钠和HCl溶于水都发生电离,克服粒子间作用力的类型相同
(2)下列能说明氯元素原子得电子能力比硫元素原子得电子能力强的是
①HCl的溶解度比H2S的大 ②HCl的酸性比H2S的强 ③HCl的稳定性比H2S的强
④还原性:Cl-<S2- ⑤HClO4的酸性比H2SO4的强 ⑥Cl2能与H2S反应生成S
⑦Cl2与铁反应生成FeCl3,而S与铁反应生成FeS
【知识点】 同周期元素性质递变规律 同主族元素性质递变规律 离子键 共价键

(2)核内中子数为N的R2+,质量数为A,则它的n g氧化物中所含质子的物质的量是
(3)最外层电子数为2的元素有
最外层电子数与次外层电子数相等的元素有
(4)在“石蜡→液体石蜡→石蜡蒸气→裂化气”的变化过程中,被破坏的作用力依次是
【知识点】 元素周期律、元素周期表的推断 共价键 分子间作用力 氢键
五、解答题 添加题型下试题
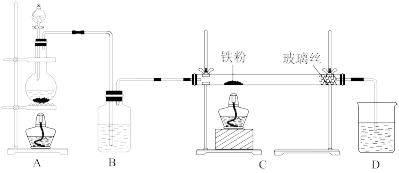
回答下列问题:
(1)制取无水氯化铁的实验中,A中反应的化学方程式为
(2)制取无水氯化亚铁的实验中,装置A用来制取
(3)若操作不当,制得的FeCl2会含有少量FeCl3,检验FeCl3常用的试剂是
六、填空题 添加题型下试题
| X | Y | ||||
| Z | W | Q | |||
(1)Q的原子结构示意图是
(2)Y、Z、W形成简单离子,其离子半径关系为
(3)用有关离子方程式表示Q、W元素的非金属性强弱
(4)Y的氢化物分子中含有18个电子,该分子中的共价键类型
(5)W的最高价氧化物对应的水化物的浓溶液与Cu反应的化学方程式为
七、解答题 添加题型下试题
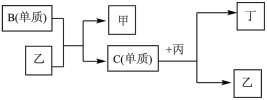
(1)写出B+乙→甲+C的化学反应方程式
(2)根据以上条件可以确定A、B、C、D四种元素中的三种,不能被确定的第四种元素是
①A②B③C④D
(3)依据下列条件可以进一步确定上述第四种元素:①甲与丙以及乙与丙均能够发生反应
②甲、丙都是无色、有刺激性气味的物质。
据此,请回答下列问题:写出上述第四种元素在周期表中第
【知识点】 无机综合推断 根据物质性质进行元素种类推断解读
(1)仪器A的名称为
(2)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫:装置A、B、C中所装药品分别为
(3)若要证明非金属性:C>Si,则A中加

试卷分析
试卷题型(共 41题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 铝与酸溶液反应 铝与强碱溶液反应 含氧化铝的混合物的提纯 | |
| 2 | 0.85 | 常见氧化剂与还原剂 氧化还原反应的规律 | |
| 3 | 0.65 | 铝 氧化铝与碱溶液反应 氢氧化铝与强碱反应 | |
| 4 | 0.65 | 离子共存 限定条件下的离子共存 | |
| 5 | 0.65 | 含氧化铝的混合物的提纯 铝土矿提取铝 铝土矿提取铝的综合考查 物质分离、提纯综合应用 | |
| 6 | 0.65 | 物质的量浓度的计算 化学方程式计算中物质的量的运用 镁 铝 | |
| 7 | 0.65 | 二氧化硅的化学性质 既能与酸反应又能与碱反应的无机物质 | |
| 9 | 0.65 | 离子反应在化合物组成的分析、鉴定的应用 铁及铁的氧化物混合物反应的相关计算 探究物质组成或测量物质的含量 | |
| 10 | 0.65 | 铁及铁的氧化物混合物反应的相关计算 | |
| 11 | 0.65 | 铁 | |
| 12 | 0.65 | 卤素离子 同主族元素性质递变规律 元素周期律的应用 元素非金属性强弱的比较方法 | |
| 13 | 0.65 | 溴、碘的性质 其他含卤化合物 物质分离、提纯综合应用 | |
| 14 | 0.64 | 氧族元素及其化合物 | |
| 15 | 0.4 | 二氧化硫的化学性质 | |
| 16 | 0.65 | 二氧化硫 硫酸盐 浓硫酸的强氧化性 | |
| 17 | 0.65 | 硫酸 硫酸铜 物质制备的探究 | |
| 18 | 0.65 | 氨气的制备 硝酸的强氧化性 硫酸根离子的检验 | |
| 19 | 0.65 | 氨的碱性 一氧化氮的化学性质 硝酸的强氧化性 | |
| 20 | 0.85 | 硫、氮氧化物对人体、环境的危害 酸雨 明矾的净水作用及原理 蛋白质的变性 | |
| 21 | 0.64 | 物质的分类 氧化还原反应基本概念 化石能源 | |
| 22 | 0.65 | 碳酸氢钠 铝 氢氧化铁 常见无机物的制备 | |
| 23 | 0.64 | 常见无机物及其应用 | |
| 24 | 0.85 | 化学与环境保护 | |
| 25 | 0.65 | 化学方程式计算中物质的量的运用 氯气的实验室制法 | |
| 26 | 0.65 | 结合气体物质与NA相关推算 结合氧化还原反应知识与NA相关推算 浓硫酸的强氧化性 铜的电解精炼 | |
| 27 | 0.65 | 阿伏加德罗常数的求算 | |
| 28 | 0.65 | 仪器使用与实验安全 配制一定物质的量浓度的溶液实验的仪器 | |
| 29 | 0.4 | 根据n=m/M的相关计算 | |
| 30 | 0.4 | 离子方程式的书写 氧化还原反应方程式的配平 | |
| 31 | 0.4 | 离子反应的发生及书写 | |
| 32 | 0.85 | 电解质、非电解质概念 物质水溶液的导电性 强电解质和弱电解质的判断 | |
| 33 | 0.65 | 氧化还原反应有关计算 基于氧化还原反应守恒规律的计算 | |
| 34 | 0.94 | 氧化还原反应的规律 与氧化剂、还原剂有关的计算 | |
| 35 | 0.85 | 离子反应的发生及书写 | |
| 二、未知 | |||
| 8 | 0.65 | 化学方程式计算中物质的量的运用 铵盐 氢氧化铝 其他含铝化合物 | 未知 |
| 三、填空题 | |||
| 36 | 0.4 | 同周期元素性质递变规律 同主族元素性质递变规律 离子键 共价键 | |
| 37 | 0.65 | 元素周期律、元素周期表的推断 共价键 分子间作用力 氢键 | |
| 39 | 0.65 | 元素周期表提供的元素信息 元素金属性与非金属性递变规律的理解及应用 共价键 | |
| 四、解答题 | |||
| 38 | 0.65 | 氯气的实验室制法 铁盐 | 实验探究题 |
| 40 | 0.65 | 无机综合推断 根据物质性质进行元素种类推断 | 无机推断题 |
| 41 | 0.65 | 元素金属性、非金属性强弱探究实验 综合实验设计与评价 | 实验探究题 |



