2016届北京一五六中学上学期高三期中考试化学试卷
北京
高三
期中
2017-07-27
397次
整体难度:
适中
考查范围:
认识化学科学、物质结构与性质、常见无机物及其应用、有机化学基础、化学实验基础、化学反应原理、化学与STSE
一、单选题 添加题型下试题
| A.乙酸的结构简式:C2H4O2 |
B.S2—的结构示意图: |
C.质子数为53、中子数为78的碘原子: |
D.CO2的电子式  |
【知识点】 化学用语
| A.Na2O、Na2O2为相同元素组成的金属氧化物,都属于碱性氧化物 |
| B.SiO2、CO2均为酸性氧化物,均能与NaOH溶液反应生成盐和水 |
| C.FeO、Fe2O3均为碱性氧化物,与氢碘酸反应均只发生复分解反应 |
| D.将Fe(OH)3胶体和泥水分别进行过滤,分散质均不能通过滤纸孔隙 |
【知识点】 物质的分类
| A.一定都是短周期元素 |
| B.原子序数:B > A > C > D |
| C.单质的还原性:B > A |
| D.气态氢化物的稳定性:D > C |
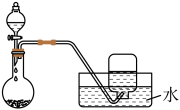
| A.饱和食盐水与碳化钙反应制取乙炔 |
| B.浓硝酸与铜反应制取二氧化氮 |
| C.浓氨水与生石灰反应制取氨气 |
| D.浓盐酸与二氧化锰反应制取氯气 |
| A.1 mol OH- 中含有10NA个电子 |
| B.46g的NO2气体中含有NA个NO2分子 |
| C.1 L 1 mol/L的AlCl3溶液中含有NA个Al3+ |
| D.常温常压下11.2 L的甲烷气体含有的分子数为0.5NA |
【知识点】 化学计量
①“84”消毒液的水溶液中:Fe2+、Cl-、Ca2+、Na+
②加入KSCN显红色的溶液:K+、NH4+、Cl-、S2-
③能够与金属Cu常温下反应放出气体的溶液:Fe3+、Al3+、SO42-、K+
④pH=2的溶液中:NH4+、Na+、Cl-、Cu2+
⑤无色溶液中:K+、CH3COO-、HCO3-、MnO4-
| A.③④ | B.①③ | C.①⑤ | D.②③ |
【知识点】 离子共存
| 元素代号 | X | Y | Z | R | W |
| 原子半径/pm | 160 | 143 | 89 | 70 | 66 |
| 主要化合价 | +2 | +3 | +2 | +5、-3 | -2 |
下列叙述正确的是
| A.X、Z元素的金属性:X < Z |
| B.一定条件下,R单质与常见的W单质能直接生成RW2 |
| C.气态氢化物的稳定性:R > W |
| D.Y的最高价氧化物既能溶于H2SO4又能溶于NaOH |
【知识点】 元素周期表 元素周期律

| 选项 | 甲 | 乙 | 丙 |
| A | AlCl3 | Al | Al(OH)3 |
| B | AlCl3 | Al(OH)3 | NaAlO2 |
| C | CO2 | NaHCO3 | Na2CO3 |
| D | CO2 | (NH4)2CO3 | NH3 |
| A.A | B.B | C.C | D.D |
【知识点】 物质的转化 碳酸钠与碳酸氢钠的相互转化解读 铝三角转化解读
二、未知 添加题型下试题
三、单选题 添加题型下试题

| A.异秦皮啶与秦皮素互为同系物 |
| B.异秦皮啶分子式为C11H12O5 |
| C.秦皮素一定条件下能发生加成反应、消去反应和取代反应 |
| D.1mol秦皮素最多可与2molBr2(浓溴水中的)、4molNaOH反应 |
| A.若无固体剩余,则溶液中一定有Fe3+ |
| B.若有固体存在,则溶液中一定有Fe2+ |
| C.若溶液中有Cu2+,则一定没有固体析出 |
| D.若溶液中有Fe2+,则一定有Cu析出 |
| A.将FeCl3饱和溶液滴入沸水中可制得Fe(OH)3胶体 |
| B.AlCl3溶液和Al2(SO4)3溶液加热蒸干、灼烧都得到Al2O3 |
| C.向FeBr2溶液中通入过量Cl2 ,加CCl4振荡静置,上层液体无色、下层为橙红色 |
| D.将Cl2通入Na2SO3溶液中,检验是否有SO42-生成,可向该溶液中滴加足量盐酸酸化的Ba(NO3)2溶液 |
【知识点】 盐类的水解
| A.1 mol·L-1的NaCl溶液中,Na+数目为NA |
| B.标准状况下,1 mol Cl2溶于水,转移电子的数目为NA |
| C.1 mol Na2O和1 mol Na2O2中,所含阴离子的数目均为NA |
| D.含2 mol H2SO4的浓硫酸与足量铜粉完全反应,生成气体分子的数目为NA |
【知识点】 化学计量

| A.集气瓶中产生的沉淀是BaSO4 |
| B.Z导管出来的气体中无CO2 |
| C.Z导管口没有红棕色气体出现 |
| D.集气瓶中产生的沉淀是BaCO3 |

| A.实验室在坩埚中灼烧干海带,使有机碘转化为无机碘(I-)并富集 |
| B.含I-的滤液中加入稀硫酸和双氧水后,碘元素发生氧化反应 |
| C.在碘水中加入几滴淀粉溶液,溶液变蓝色 |
| D.碘水中加入CCl4得到I2的CCl4溶液,该操作为“分液” |
| A.H2O | B.Zn | C.KI | D.KCl |
【知识点】 溴、碘的性质 其他含卤化合物 物质分离、提纯综合应用解读
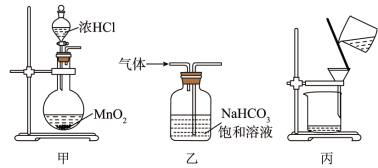
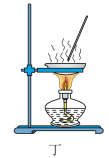
| A.用装置甲制取氯气 |
| B.用装置乙除去氯气中的少量氯化氢 |
| C.用装置丙分离二氧化锰和氯化锰溶液 |
| D.用装置丁蒸干氯化锰溶液制MnCl2·4H2O |
【知识点】 氯气的实验室制法解读 物质分离、提纯的常见物理方法
| 实验事实 | 结论 | |
| ① | HCl的水溶液中存在H+和Cl- | HCl是离子化合物 |
| ② | NO2通入水中,发生反应,产物中有HNO3 | NO2是酸性氧化物 |
| ③ | 向FeCl3溶液中加入铜片,溶液逐渐变为蓝色 | 氧化性:Fe3+ > Cu2+ |
| ④ | 等物质的量的Na和Al都完全反应,Al失电子多 | 金属性:Al > Na |
| ⑤ | 某无色溶液中加入氢氧化钠浓溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝 | 该溶液中一定有NH4+ |
| A.①② | B.①②④ | C.③⑤ | D.③④⑤ |
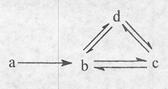
| a | b | c | d | |
| ① | Si | SiO2 | H2SiO3 | Na2SiO3 |
| ② | Al | AlCl3 | NaAlO2 | Al(OH)3 |
| ③ | Cu | CuO | Cu(OH)2 | CuSO4 |
| ④ | Na | NaOH | Na2CO3 | NaHCO3 |
| A.①② | B.②③ | C.③④ | D.②④ |
| A.反应中共消耗1.85 mol H2SO4 | B.气体甲中SO2与H2的体积比为1∶4 |
| C.反应中共消耗65 g Zn | D.反应中共转移3.6 mol电子 |
【知识点】 氧族元素及其化合物
四、解答题 添加题型下试题

请回答:
(1)Z的电子式是
(2)实验室制取Z的的化学方程式:
(3)某化学小组同学模拟工业生产制取HNO3,设计下图所示装置,其中a为一个可持续鼓入空气的橡皮球。

① A中发生反应的化学方程式是
② B中浓H2SO4的作用是
(4)写出D装置中反应的化学方程式
(1)SiO2是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是
A.普通玻璃坩埚 B.石英玻璃坩埚 C.氧化铝坩埚 D.铁坩埚
(2)高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:
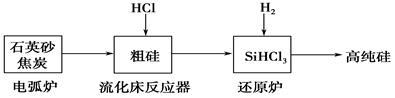
①用石英砂和焦炭在电弧炉中制粗硅,该反应的化学方程式为
②在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,有关物质的沸点数据如下表,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和
| 物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
| 沸点/℃ | 2 355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
③SiHCl3极易水解,其完全水解的化学方程式为
(3)某同学为了验证碳和硅两种元素非金属性的相对强弱,用下图所示装置进行实验(夹持仪器已略去,气密性已检验),实验操作步骤:
Ⅰ.打开弹簧夹1,关闭弹簧夹2,并打开活塞a,滴加盐酸。
Ⅱ.A中看到白色沉淀时,关闭弹簧夹1,打开弹簧夹2,,关闭活塞a。

① B中反应的离子方程式是
②通过步骤Ⅰ得知盐酸具有的性质是
A.挥发性 B. 还原性 C. 氧化性 D. 酸性
③ C装置中的试剂X是
④碳、硅的非金属性逐渐减弱的原因:碳和硅
【知识点】 二氧化硅 硅的制备解读 同主族元素性质递变规律 化学实验探究
五、填空题 添加题型下试题
| 成分 | Cl- | Na+ | SO42- | Mg2+ | Ca2+ | HCO3- | Br- |
| 含量/(mg·L-1) | 18980 | 10560 | 2560 | 1272 | 400 | 142 | 64 |
(1)以食盐为原料进行生产并综合利用的某些过程如下图所示。

①除去粗盐中的Ca2+、Mg2+和SO
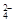 离子,加入沉淀剂a.Na2CO3 b.NaOH c.BaCl2,
离子,加入沉淀剂a.Na2CO3 b.NaOH c.BaCl2,合理的一种顺序是(填序号)
②电解饱和食盐水的化学方程式是
③侯德榜向饱和食盐水中通入NH3、CO2气体制NaHCO3晶体的化学方程式为
其依据是
④工业上可用纯碱代替烧碱生产某些化工产品。如用饱和纯碱溶液与Cl2制取有效成分为NaClO的消毒液,反应的化学方程式是
(2)利用海水可以提取溴和镁,提取过程如下:

① 从MgCl2溶液中得到MgCl2·6H2O晶体的主要实验操作是
②用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为
③依据上述流程,若将5 m3海水中的溴元素转化为工业溴,至少需要标准状况下Cl2的体积为
六、解答题 添加题型下试题
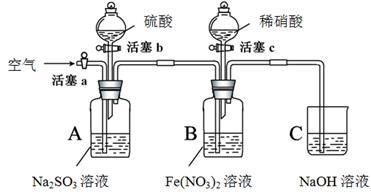
实验记录如下:
| 实验操作 | 实验现象 | |
| I | 打开活塞c,将过量稀HNO3加入装置B中,关闭活塞c | B中浅绿色溶液立即变为深棕色;一段时间后,溶液最终变为黄色。 |
| II | 用注射器取出少量B装置中的溶液,加入KSCN溶液 | 溶液变为红色。 |
| III | 打开活塞b,向A装置中加入足量硫酸,关闭活塞b | A中产生气体;B中有气泡,液面上有少量红棕色气体生成。 |
| IV | 一段时间后,用注射器取出少量B装置中的溶液,…… | …… |
| V | 打开活塞a,通入一段时间空气 | ———— |
请回答下列问题:
(1)保存Fe(NO3)2溶液时,常加入铁粉,目的是(用化学方程式表示)________。
(2)实验I中,发生反应的离子方程式是________。
(3)资料表明,Fe2+能与NO结合形成深棕色物质[Fe(NO)]2+: Fe2++ NO
 [Fe(NO)]2+
[Fe(NO)]2+用平衡移动原理解释实验I中溶液由深棕色变为黄色的原因是________________________。
(4)分析实验现象,同学们得出了结论。则:
① 实验IV的后续操作是________________,观察到的现象是________________。
② 由实验得出的结论是_______________________。
(5)实验反思
① 实验操作V的目的是_______________________________________。
② 实验操作III,开始时B中溶液的颜色并无明显变化,此时溶液中发生反应的离子方程式是________。
③ 有同学认为装置中的空气会干扰实验结论的得出,应在实验前通一段时间的氮气。你是否同意该看法,理由是________________________________________。
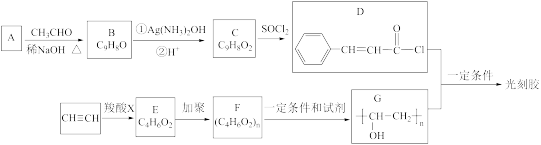
已知:
Ⅰ.
 (R,R’为烃基或氢)
(R,R’为烃基或氢)Ⅱ.
 (R,R’为烃基)
(R,R’为烃基)(1)A分子中含氧官能团名称为
(2)C物质可发生的反应类型为
a.加聚反应 b. 酯化反应 c. 还原反应 d.缩聚反应
(3)B与Ag(NH3)2OH反应的化学方程式为
(4)乙炔和羧酸X加成生成E,E的核磁共振氢谱为三组峰,且峰面积比为3:2:1,E能发生水解反应,则E的结构简式为
(5)与C具有相同官能团且含有苯环的同分异构体有
(6)D和G反应生成光刻胶的化学方程式为
试卷分析
试卷题型(共 25题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 化学用语 | |
| 2 | 0.64 | 物质的分类 | |
| 3 | 0.65 | 元素周期律的应用 原子序数与元素在周期表中的位置的关系分析及利用 | |
| 4 | 0.65 | 氯气的实验室制法 氨气的实验室制法 乙炔的制备 常见气体的制备与收集 | |
| 5 | 0.64 | 化学计量 | |
| 6 | 0.4 | 离子共存 | |
| 7 | 0.64 | 元素周期表 元素周期律 | |
| 8 | 0.65 | 物质的转化 碳酸钠与碳酸氢钠的相互转化 铝三角转化 | |
| 10 | 0.65 | 有机反应类型 有机物分子式的确定 含酯基有机物水解消耗NaOH的量的计算 | |
| 11 | 0.65 | 铁与铁离子反应 Fe、Cu及相关离子的反应 Fe、Cu与Fe3+反应几种情况分析及判断 | |
| 12 | 0.4 | 盐类的水解 | |
| 13 | 0.64 | 化学计量 | |
| 14 | 0.4 | 氮族元素及其化合物 氧族元素及其化合物 | |
| 15 | 0.65 | 物质分离、提纯综合应用 海水资源综合利用 海带中碘的提取及检验 | |
| 16 | 0.65 | 溴、碘的性质 其他含卤化合物 物质分离、提纯综合应用 | |
| 17 | 0.65 | 氯气的实验室制法 物质分离、提纯的常见物理方法 | |
| 18 | 0.65 | 硝酸的强氧化性 铵根离子的检验 Fe3+与其他物质氧化性强弱关系 | |
| 19 | 0.65 | 二氧化硅的化学性质 碳酸钠与碳酸氢钠的相互转化 铝三角转化 铜的其他化合物 | |
| 20 | 0.4 | 氧族元素及其化合物 | |
| 二、未知 | |||
| 9 | 0.85 | 离子反应的实际应用 离子反应在化合物组成的分析、鉴定的应用 过氧化钠的强氧化性 | 未知 |
| 三、解答题 | |||
| 21 | 0.65 | 无机综合推断 氨的还原性 二氧化氮 常见物质的制备 | 实验探究题 |
| 22 | 0.4 | 二氧化硅 硅的制备 同主族元素性质递变规律 化学实验探究 | 实验探究题 |
| 24 | 0.15 | 氧化性、还原性强弱的比较 物质性质的探究 物质性质实验方案的设计 | 实验探究题 |
| 25 | 0.65 | 醛类的银镜反应 多官能团有机物的结构与性质 有机推断综合考查 | 有机推断题 |
| 四、填空题 | |||
| 23 | 0.4 | 海水中盐的开发及利用 海水提取溴 海水提取镁 | |



