苏教版(2020)高一必修第一册专题3 总结检测
全国
高一
课后作业
2020-09-02
384次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、化学实验基础、化学反应原理
一、单选题 添加题型下试题
| 选项 | 古诗或谚语 | 含有的化学反应类型 |
| A | 熬胆矾之铁釜,久之亦化为铜 | 复分解反应 |
| B | 千锤万凿出深山,烈火焚烧若等闲 | 分解反应 |
| C | 春蚕到死丝方尽,蜡炬成灰泪始干 | 化合反应 |
| D | 爆竹声中除旧岁,春风送暖入屠苏 | 非氧化还原反应 |
| A.A | B.B | C.C | D.D |
【知识点】 四种基本反应类型解读 氧化还原反应基本概念
| A.金属在氯气中燃烧都有棕黄色的烟产生 |
| B.氯气为黄绿色有毒气体,与铁反应生成氯化亚铁 |
| C.氯气不能使干燥的有色布条褪色 |
D.可通过下图装置除去Cl2中的HCl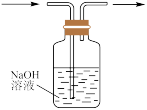 |
| A.新制的氯水中,溶质既有分子又有离子 |
| B.新制的氯水是无色透明的液体,有酸性和漂白性 |
| C.光照氯水有气泡逸出,该气体是O2 |
| D.氯水放置数天后酸性将增强 |
| A.Na和O2 | B.NaOH和CO2 | C.Na2O2和CO2 | D.Na2CO3和HCl |
【知识点】 钠与氧气等非金属的反应解读 过氧化钠和二氧化碳反应解读 碳酸钠
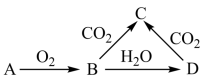
| A.易溶于水 |
| B.与澄清石灰水反应产生白色沉淀 |
| C.与足量盐酸反应放出气体 |
| D.属于碱 |
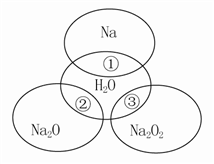
| A.Na2O2中阴阳离子数目之比为1∶1 |
| B.反应①的离子方程式为Na+2H2O===Na++2OH-+H2↑ |
| C.①、②、③充分反应后所得溶液中溶质的质量分数:①>②>③ |
| D.反应③转移电子的物质的量为0.1mol |
 =2X2++5Z2+8H2O
=2X2++5Z2+8H2O②2A2++B2=2A3++2B-
③2B-+Z2=B2+2Z-
由此推断下列说法错误的是( )
| A.反应Z2+2A2+=2A3++2Z-可以进行 |
| B.Z元素在反应③中被还原,在反应①中被氧化 |
C.氧化性由强到弱的顺序是XO 、Z2、B2、A3+ 、Z2、B2、A3+ |
| D.还原性由强到弱的顺序是Z-、B-、A2+、X2+ |
| A.取一定量固体,溶解,向溶液中通入足量的CO2,观察到有晶体析出,说明原固体中一定含有Na2CO3 |
| B.取一定量固体,溶解,向溶液中加入适量CaO粉末,充分反应后观察到有白色沉淀生成,说明原固体中一定含有Na2CO3 |
| C.取一定量固体,溶解,向溶液中滴加适量AgNO3溶液,观察到有白色沉淀生成,说明原固体中一定含有NaCl |
| D.称取3.80g固体,加热至恒重,质量减少了0.620g。用足量稀盐酸溶解残留固体,充分反应后,收集到0.880g气体,说明原固体中仅含有Na2CO3和NaHCO3 |
| 100mL 盐酸 | 100mL 盐酸 | 100mL 盐酸 | |
| m(混合物) | 14.2g | 25g | 27.6g |
| V(CO2) | 3.36L | 4.48L | 4.48L |
| A.盐酸的物质的量浓度为3.0mol·L-1 |
| B.加入混合物14.2g时盐酸不足 |
| C.加入25g混合物时盐酸过量 |
| D.根据表中数据计算出混合物中NaHCO3与KHCO3的物质的量之比是1:2 |
| A.NaClO2在酸性条件下歧化生成ClO2和NaCl,则n(氧化剂):n(还原剂)=1:4 |
| B.ClO2在强碱性环境中使用失效,可能的原因是:2ClO2+2OH- =ClO3- + ClO2-+H2O |
| C.可用饱和食盐水除去ClO2中的NH3 |
| D.等物质的量的ClO2杀菌效果比Cl2强 |
【知识点】 氧化还原反应基本概念 氧化还原反应有关计算
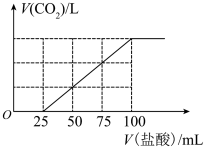
| A.通入CO2后,所得溶液的溶质成分的物质的量之比为n(NaHCO3):n(Na2CO3)=1:1 |
| B.通入CO2在标准状况下的体积为448mL |
| C.通入CO2后,所得溶液的溶质成分的物质的量之比为n(NaOH):n(Na2CO3)=1:3 |
| D.原NaOH溶液的浓度为0.2mol/L |
二、填空题 添加题型下试题
 的
的 、
、 (含淀粉)、
(含淀粉)、 (含酚酞)、
(含酚酞)、 (含
(含 )溶液各1滴,在表面皿中心处放置2小粒
)溶液各1滴,在表面皿中心处放置2小粒 晶体,并滴加一滴浓盐酸,立即将表面皿盖好。可见
晶体,并滴加一滴浓盐酸,立即将表面皿盖好。可见 晶体很快溶解,并产生气体。
晶体很快溶解,并产生气体。
已知
 能与
能与 反应生成红色络合物
反应生成红色络合物 。
。(1)①写出化学实验室中用
 制取
制取 的化学方程式:
的化学方程式:②完成本实验中制取
 的化学方程式:
的化学方程式:




 ,则转移电子数目为
,则转移电子数目为(2)b处的实验现象为
(3)d处反应的离子方程式为
(4)通过该实验能比较
 、
、 、
、 三种物质氧化性的强弱,其氧化性由强到弱的顺序是
三种物质氧化性的强弱,其氧化性由强到弱的顺序是三、解答题 添加题型下试题
已知:CO+2Ag(NH3)2OH=2Ag↓+ (NH4)2CO3+2NH3
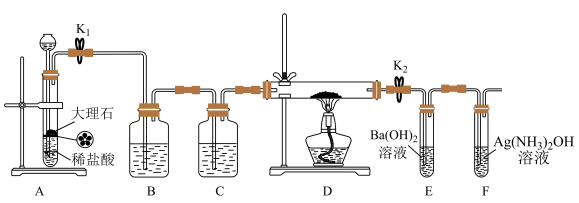
回答下列问题:
(1)B中的溶液为
(2)先称量硬质玻璃管的质量为mlg,将样品装入硬质玻璃管中,称得样品和硬质玻璃管的总质量是m2g。再进行下列实验操作,其正确顺序是
a.点燃酒精灯,加热b.熄灭酒精灯c.称量硬质玻璃管
d.打开K1和K2,通入CO2至E中出现浑浊e.关闭K1和K2f.冷却到室温
(3)加热硬质玻璃管一段时间,观察到以下现象:
①钠块表面变暗,熔融成金属小球;
②继续加热,钠迅速燃烧,产生黄色火焰。反应完全后,管中有大量黑色物质;
③F中试管内壁有银白物质产生。
产生上述②现象的原因是
(4)探究固体产物中钠元素的存在形式
假设一:只有Na2CO3;假设二:只有Na2O;假设三:Na2O和Na2CO3均有;
完成下列实验设计,验证上述假设:
| 步骤 | 操作和现象 | 结论 |
| 1 | 将硬质玻璃管中的固体产物溶于水后过滤; | 假设一成立 |
| 2 | 往步骤1所得滤液中 现象: |
| m1 | m2 | m3 |
| 66.7g | 69.0g | 72.1g |
四、单选题 添加题型下试题
| A.2NaBr+Cl2=2NaCl+Br2 | B.Br2+2NaI=2NaBr+I2 |
C.3Br2+6NaOH 5NaBr+NaBrO3+3H2O 5NaBr+NaBrO3+3H2O | D.HBr+NaOH=NaBr+H2O |
【知识点】 氧化还原反应的几组概念解读
A. NaHCO3的电离方程式为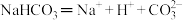 |
| B.HClO是弱酸,但NaClO是强电解质 |
| C.KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质 |
| D.BaSO4的水溶液不易导电,故BaSO4是弱电解质 |
【知识点】 电解质与非电解质 电离方程式解读 强电解质和弱电解质的判断
A. | B.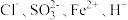 |
C.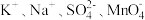 | D.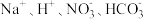 |
【知识点】 离子共存 无附加条件的离子共存解读
A.无色溶液中可能大量存在 、 、 、 、 、 、 |
B.澄清溶液中可能大量存在 、 、 、 、 、 、 |
C.弱碱性溶液中可能大量存在 、 、 、 、 、 、 |
D.中性溶液中可能大量存在 、 、 、 、 、 、 |
【知识点】 离子反应的发生条件解读 限定条件下的离子共存解读
2R(OH)3+ 3C1O-+ 4OH-= 2RO4n-+3Cl-+5H2O。则RO4n-中R的化合价是()
| A.+3 | B.+4 | C.+5 | D.+6 |
【知识点】 离子反应的发生及书写
五、多选题 添加题型下试题
A.大理石与醋酸反应: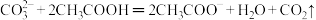 |
B.澄清石灰水中通入过量的二氧化碳: |
C.向氢氧化钡溶液中加入稀硫酸: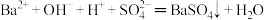 |
D.氢氧化钠溶液与过量的碳酸氢钙溶液反应: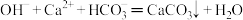 |
【知识点】 离子方程式的书写解读 离子方程式的正误判断解读
 中的氨作用相同的是
中的氨作用相同的是A. | B. |
C. | D. |
【知识点】 氧化还原反应的几组概念解读 氧化还原反应的规律解读
六、单选题 添加题型下试题
| A.氧气是氧化产物 |
| B.O2F2既是氧化剂又是还原剂 |
| C.若生成4.48 L HF,则转移0.8 mol电子 |
| D.还原剂与氧化剂的物质的量之比为1:4 |

| A.在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA |
| B.用如图装置(夹持、加热装置已略)进行实验,由②中澄清石灰水变浑浊,可证明①中NaHCO3固体受热分解 |
C. ,是水作还原剂的氧化还原反应 ,是水作还原剂的氧化还原反应 |
| D.过氧化钠会因为空气中的氧气而易变质 |
| A.用加热分解的方法区分碳酸钠和碳酸氢钠两种固体 |
B.由矿盐(主要成分是 ,还含有 ,还含有 等其他可溶性杂质的离子)生成食盐,除去 等其他可溶性杂质的离子)生成食盐,除去 最合适的试剂是 最合适的试剂是 |
| C.用酚酞试液可鉴别饱和食盐水和饱和纯碱溶液 |
D.用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液可能是钠盐溶液,也可能是 溶液 溶液 |
| A.氯水的颜色呈浅黄绿色,说明氯水中含有Cl2 |
| B.向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl- |
| C.向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+ |
| D.向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO |
试卷分析
试卷题型(共 25题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 四种基本反应类型 氧化还原反应基本概念 | |
| 2 | 0.65 | 氯气的化学性质 氯气与碱溶液反应 | |
| 3 | 0.65 | 氯水的成分及检验 氯水性质实验探究 | |
| 4 | 0.85 | 钠与氧气等非金属的反应 过氧化钠和二氧化碳反应 碳酸钠 | |
| 5 | 0.85 | 无机综合推断 钠 过氧化钠 碳酸钠 | |
| 6 | 0.65 | 钠 氧化钠 过氧化钠 电子转移计算 | |
| 7 | 0.65 | 氧化还原反应的规律 | |
| 8 | 0.65 | 离子的检验 常见阳离子的检验 | |
| 9 | 0.15 | 碳酸氢钠与酸反应 | |
| 10 | 0.4 | 氧化还原反应基本概念 氧化还原反应有关计算 | |
| 11 | 0.4 | 氢氧化钠、碳酸钠混合溶液与盐酸反应相关考查 碳酸钠、碳酸氢钠混合物的有关求算 | |
| 14 | 0.65 | 氧化还原反应的几组概念 | |
| 15 | 0.94 | 电解质与非电解质 电离方程式 强电解质和弱电解质的判断 | |
| 16 | 0.85 | 离子共存 无附加条件的离子共存 | |
| 17 | 0.94 | 离子反应的发生条件 离子共存 常见氧化剂与还原剂 | |
| 18 | 0.85 | 离子反应的发生条件 限定条件下的离子共存 | |
| 19 | 0.85 | 离子反应的发生及书写 | |
| 22 | 0.65 | 氧化还原反应的应用 氧化还原反应的规律 | |
| 23 | 0.85 | 氧化还原反应基本概念 过氧化钠 过氧化钠与水的反应 碳酸氢钠的不稳定性 | |
| 24 | 0.85 | 硫酸根离子的检验 焰色试验 碳酸钠 碳酸钠与碳酸氢钠鉴别的实验 | |
| 25 | 0.65 | 氯水的成分及检验 氯水性质实验探究 | |
| 二、填空题 | |||
| 12 | 0.65 | 氧化性、还原性强弱的比较 氧化还原反应方程式的配平 氯气的化学性质 氯气的实验室制法 | |
| 三、解答题 | |||
| 13 | 0.65 | 钠与氧气等非金属的反应 探究物质组成或测量物质的含量 化学实验探究 | 实验探究题 |
| 四、多选题 | |||
| 20 | 0.85 | 离子方程式的书写 离子方程式的正误判断 | |
| 21 | 0.94 | 氧化还原反应的几组概念 氧化还原反应的规律 | |

 、
、 、
、 、
、 、
、


