广东省汕头市潮南区田心中学2020-2021学年高一上学期第一次月考化学试题
广东
高一
阶段练习
2021-10-18
313次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用
一、单选题 添加题型下试题
| A.硫酸、纯碱、孔雀石 | B.硝酸、烧碱、纯碱 |
| C.冰醋酸、乙醇、醋酸钠 | D.盐酸、熟石灰、苛性钠 |
| A.用激光笔照射该液体,会出现丁达尔效应 |
| B.将液体静置片刻,会出现沉淀现象 |
| C.所得分散系中分散质的粒子直径大于100 nm |
| D.用滤纸可实现该分散系中分散剂与分散质的分离 |
| A.固体NaCl不存在阴阳离子,不导电 |
| B.Na2O、Fe2O3、CO2均属于碱性氧化物 |
| C.硫酸钡溶液几乎不导电,但硫酸钡属于电解质 |
| D.金刚石和石墨是同素异形体,化学性质不同,物理性质相同 |
【知识点】 非电解质、电解质物质类别判断解读 物质水溶液的导电性解读
| A.Na+ | B.H+ | C.CO | D.SO |
【知识点】 离子共存
| A.Cu(OH)2+2HNO3=Cu(NO3)2+2H2O | B.Ba(OH)2 +2 HCl = BaCl2+2H2O |
| C.2NaOH + H2SO4 = Na2SO4+2H2O | D.HCl+KOH=KCl+ H2O |
| A.雾霾天,汽车车灯照出光亮“通路”的现象属于丁达尔效应 |
| B.雾和霾都是混合物 |
| C.防雾霾口罩的原理与过滤、渗析类似,防雾霾效果好的口罩往往呼吸阻力较大 |
D. 是指直径小于或等于2.5 μm的污染物颗粒,该颗粒直径完全在胶体粒子的直径范围内 是指直径小于或等于2.5 μm的污染物颗粒,该颗粒直径完全在胶体粒子的直径范围内 |
A.熔融状态下NaHSO4的电离:NaHSO4=Na++H++SO |
| B.水溶液中Ba(OH)2的电离:Ba(OH)2=Ba2++OH- |
C.水溶液中NaHCO3的电离:NaHCO3=Na++HCO |
D.水溶液中Al2(SO4)3的电离: Al2(SO4)3=3Al3++3SO |
A.H+、K+、Fe3+、SO | B.Ba2+、Ca2+、OH-、CO |
C.H+、Na+、NO 、Cu2+、 、Cu2+、 | D.Mg2+、Na+、Cl-、SO |
【知识点】 限定条件下的离子共存解读
| A.CuO与稀硫酸反应:CuO+2H+=Cu2++H2O |
| B.铜与稀硫酸反应:Cu+2H+=Cu2++H2↑ |
| C.稀HNO3与Ba(OH)2溶液反应:H++OH-=H2O |
| D.铜片插入硝酸银溶液中:Cu+2Ag+=Cu2++2Ag |
【知识点】 离子反应的发生及书写 离子方程式的正误判断解读
A. 溶液 溶液 溶液, 溶液, 溶液 溶液 溶液 溶液 |
B. 溶液 溶液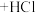 溶液, 溶液, 溶液+ 溶液+ 溶液 溶液 |
C. 溶液 溶液 溶液, 溶液, 溶液 溶液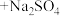 溶液 溶液 |
D. 溶液, 溶液, 溶液 溶液 溶液 溶液 |
【知识点】 离子反应的发生及书写 离子方程式的书写解读
| A.失去电子的反应是还原反应 | B.作氧化剂的物质不能是还原剂 |
| C.发生氧化反应的物质是氧化剂 | D.失去电子的物质是还原剂 |
【知识点】 氧化还原反应基本概念 氧化还原反应的几组概念解读
| A.H2O2+SO2 = H2SO4 | B.2NaHCO3 Na2CO3+H2O+CO2↑ Na2CO3+H2O+CO2↑ |
| C.Cl2+SO2+2H2O = H2SO4+2HCl | D.2Na+2H2O = 2NaOH + H2↑ |
【知识点】 氧化还原反应基本概念 氧化还原反应的定义及实质
2R(OH)3+ 3C1O-+ 4OH-= 2RO4n-+3Cl-+5H2O。则RO4n-中R的化合价是()
| A.+3 | B.+4 | C.+5 | D.+6 |
【知识点】 离子反应的发生及书写
A.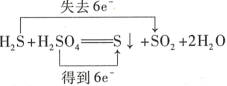 |
B. |
C.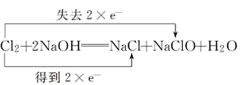 |
D. |
【知识点】 单线桥、双线桥分析氧化还原反应解读
二、填空题 添加题型下试题
(1)可以导电的有
(2)属于电解质的有
(3)属于非电解质的有
(4)②在水中的电离方程式为
【知识点】 电解质的电离 电解质、非电解质概念解读 电离方程式解读
(1)写出下列物质的电离方程式:
Fe2(SO4)3
Na2CO3
Cu(NO3)2
(2)写出下列反应的离子方程式:
稀盐酸与碳酸钙反应
氢氧化钡溶液与稀硫酸反应
①

②

③

④

⑤

⑥

⑦

⑧

⑨

⑩

(1)其中属于化合反应的有
(2)在化学反应前后元素的化合价没有发生变化的是
(3)上述反应中,既是分解反应又是氧化还原反应的是
(4)上述反应中,既是溶液中的离子反应,又是氧化还原反应的是
(5)根据你的理解,氧化还原反应的实质是
A.分子中原子的重新组合
B.氧元素的得失
C.电子的得失或共用电子对的偏移
D.元素化合价的改变
【知识点】 物质的转化 离子反应概念解读 氧化还原反应基本概念
(1)已知
 中铬元素是+3价,则其中铁元素是
中铬元素是+3价,则其中铁元素是 是一种酸根离子,则
是一种酸根离子,则 属于
属于(2)明胶的水溶液和
 溶液共同具备的性质是
溶液共同具备的性质是a.都不稳定,密封放置沉淀
b.能产生丁达尔效应
c.分散质粒子可通过滤纸
(3)现有10mL明胶的水溶液与5mL
 溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明
溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明 能够透过半透膜:
能够透过半透膜:(1)上述所举抗酸药中有
(2)CaCO3作抗酸药时发生反应的离子方程式为
(3)
(4)如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],反应的离子方程式为
【知识点】 非电解质、电解质物质类别判断解读 离子反应的发生及书写
三、解答题 添加题型下试题
 、CO
、CO 、OH-中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水但溶于盐酸并放出无色无味的气体E;③C的水溶液呈碱性,与稀硫酸反应生成A;④D可溶于水,与稀硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
、OH-中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水但溶于盐酸并放出无色无味的气体E;③C的水溶液呈碱性,与稀硫酸反应生成A;④D可溶于水,与稀硫酸作用时放出气体E,E可使澄清石灰水变浑浊。(1)推断A、C的化学式:A
(2)写出下列反应的离子方程式。
①D与氯化钙反应:
②B与盐酸反应:
③C与稀硫酸反应:
试卷分析
试卷题型(共 20题)
试卷难度
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 分类方法的应用 酸、碱、盐、氧化物的概念及其相互联系 | |
| 2 | 0.65 | 分散系概念及其分类 胶体的性质和应用 | |
| 3 | 0.65 | 非电解质、电解质物质类别判断 物质水溶液的导电性 | |
| 4 | 0.94 | 离子共存 | |
| 5 | 0.94 | 离子反应概念 离子方程式的书写 | |
| 6 | 0.85 | 分散系概念 胶体 | |
| 7 | 0.85 | 电离的定义 电离方程式 | |
| 8 | 0.65 | 限定条件下的离子共存 | |
| 9 | 0.85 | 离子反应的发生及书写 离子方程式的正误判断 | |
| 10 | 0.85 | 离子反应的发生及书写 离子方程式的书写 | |
| 11 | 0.85 | 氧化还原反应基本概念 氧化还原反应的几组概念 | |
| 12 | 0.85 | 氧化还原反应基本概念 氧化还原反应的定义及实质 | |
| 13 | 0.85 | 离子反应的发生及书写 | |
| 14 | 0.85 | 单线桥、双线桥分析氧化还原反应 | |
| 二、填空题 | |||
| 15 | 0.85 | 电解质的电离 电解质、非电解质概念 电离方程式 | |
| 16 | 0.85 | 电离方程式 离子方程式的书写 | |
| 17 | 0.65 | 物质的转化 离子反应概念 氧化还原反应基本概念 | |
| 18 | 0.85 | 酸、碱、盐、氧化物的概念及其相互联系 胶体的性质和应用 硫酸根离子的检验 | |
| 19 | 0.65 | 非电解质、电解质物质类别判断 离子反应的发生及书写 | |
| 三、解答题 | |||
| 20 | 0.85 | 离子方程式的书写 离子反应在化合物组成的分析、鉴定的应用 | 无机推断题 |



