“皮鞋很忙”的恶搞段子曾经风靡网络,揭露了某些行业用烂皮鞋制造酸奶或毒胶囊的不法行为。央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知 中铬元素是+3价,则其中铁元素是
中铬元素是+3价,则其中铁元素是______ 价。 是一种酸根离子,则
是一种酸根离子,则 属于
属于______ (填“酸”“碱”“盐”或“氧化物”)。
(2)明胶的水溶液和 溶液共同具备的性质是
溶液共同具备的性质是____ (填序号)。
a.都不稳定,密封放置沉淀
b.能产生丁达尔效应
c.分散质粒子可通过滤纸
(3)现有10mL明胶的水溶液与5mL 溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明
溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明 能够透过半透膜:
能够透过半透膜:_____ 。
(1)已知
 中铬元素是+3价,则其中铁元素是
中铬元素是+3价,则其中铁元素是 是一种酸根离子,则
是一种酸根离子,则 属于
属于(2)明胶的水溶液和
 溶液共同具备的性质是
溶液共同具备的性质是a.都不稳定,密封放置沉淀
b.能产生丁达尔效应
c.分散质粒子可通过滤纸
(3)现有10mL明胶的水溶液与5mL
 溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明
溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明 能够透过半透膜:
能够透过半透膜:
19-20高一·全国·单元测试 查看更多[9]
广东省汕头市潮南区田心中学2020-2021学年高一上学期第一次月考化学试题安徽省灵璧县第一中学2020-2021学年高一上学期12月月考试题陕西省汉中市汉中中学2020-2021学年高一上学期期中考试化学试题四川省南充市阆中中学2020-2021学年高一上学期期中考试化学试题(仁智班)云南省玉溪第一中学2020-2021学年高一上学期第一次月考化学试题安徽省宣城市郎溪县郎溪中学2020-2021学年高一第一次月考化学试题高一必修第一册(苏教2019版)专题1 B 素养拓展区吉林省长春外国语学校2020-2021学年高一上学期第一次月考化学(理)试题鲁科版(2019)高一必修第一册第二章B 素养拓展区 过综合 章末素养综合检测
更新时间:2020-09-14 08:32:39
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】现有①氧气;②空气;③碱式碳酸铜;④氯酸钾;⑤硫;⑥水;⑦氧化镁;⑧氯化钠等物质,其中属于单质的有(填序号)________ ;属于化合物的有________ ,其中________ 属于含氧化合物,________ 属于氧化物;属于混合物的有________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】从不同的角度对物质进行分类有利于研究物质的组成与性质。现有以下物质:①Cu②NaC1③盐酸④KHSO4晶体⑤干冰⑥熔融NaOH⑦SiO2⑧Fe(OH)3胶体⑨蔗糖固体。回答下列问题:
(1)以上物质属于氧化物的有___________ (填序号)。
(2)以上物质能导电的有___________ (填序号)。
(3)以上物质属于电解质的有___________ (填序号)。
(4)以上物质属于非电解质的有___________ (填序号)。
(5)实验室制备⑧的化学反应方程式为___________ 。
(1)以上物质属于氧化物的有
(2)以上物质能导电的有
(3)以上物质属于电解质的有
(4)以上物质属于非电解质的有
(5)实验室制备⑧的化学反应方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】 、
、 的资源化利用既能解决环保问题,又能提供化工原料,解决能源紧张,具有重要的现实意义和广阔的应用前景。
的资源化利用既能解决环保问题,又能提供化工原料,解决能源紧张,具有重要的现实意义和广阔的应用前景。
(1)利用 可合成多种化工产品。
可合成多种化工产品。
① 与
与 能在催化剂表面反应生成优质气体燃料
能在催化剂表面反应生成优质气体燃料 和
和 ,该反应的化学方程式为
,该反应的化学方程式为__ 。
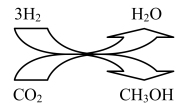
②2021年9月24日我国科学家首次报告了 到淀粉的人工合成路线,其中第一步转化如图所示,该反应的化学方程式为
到淀粉的人工合成路线,其中第一步转化如图所示,该反应的化学方程式为___________ 。
(2) 是一种酸性氧化物,可用氨水吸收烟气中的
是一种酸性氧化物,可用氨水吸收烟气中的 。
。
① 属于
属于___________ (填“电解质”或“非电解质”),标准状况下,1体积水约能溶解 体积
体积 ,所得氨水密度为
,所得氨水密度为 ,则该氨水的物质的量浓度为
,则该氨水的物质的量浓度为___________ 。
②氨水吸收少量 ,可生成
,可生成 ,反应的离子方程式为
,反应的离子方程式为___________ 。所得溶液再用 氧化,可制得化肥
氧化,可制得化肥 ,反应的化学方程式为
,反应的化学方程式为___________ 。
 、
、 的资源化利用既能解决环保问题,又能提供化工原料,解决能源紧张,具有重要的现实意义和广阔的应用前景。
的资源化利用既能解决环保问题,又能提供化工原料,解决能源紧张,具有重要的现实意义和广阔的应用前景。(1)利用
 可合成多种化工产品。
可合成多种化工产品。
①
 与
与 能在催化剂表面反应生成优质气体燃料
能在催化剂表面反应生成优质气体燃料 和
和 ,该反应的化学方程式为
,该反应的化学方程式为②2021年9月24日我国科学家首次报告了
 到淀粉的人工合成路线,其中第一步转化如图所示,该反应的化学方程式为
到淀粉的人工合成路线,其中第一步转化如图所示,该反应的化学方程式为(2)
 是一种酸性氧化物,可用氨水吸收烟气中的
是一种酸性氧化物,可用氨水吸收烟气中的 。
。①
 属于
属于 体积
体积 ,所得氨水密度为
,所得氨水密度为 ,则该氨水的物质的量浓度为
,则该氨水的物质的量浓度为②氨水吸收少量
 ,可生成
,可生成 ,反应的离子方程式为
,反应的离子方程式为 氧化,可制得化肥
氧化,可制得化肥 ,反应的化学方程式为
,反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】I.下列每组中都有一种物质与其他物质在分类上不同,试分析每组中物质的组成规律,将这种不同于其他物质的物质找出来写在横线上:
(1)NaCl、KCl、NaClO、MgCl2_______
(2)H3PO4 、H2SO3 、HCl、HNO3_______
(3)CO2、CaO、 SO3、SO2_______
(4)空气、盐酸、氨水、胆矾_______
(5)Mg、Al、Zn、S_______
II.某课外活动小组进行Fe(OH)3胶体的制备实验并检验其相关性质。
(1)若将饱和FeCl3溶液分别滴入下列液体中,不能形成Fe(OH)3胶体的是_______ 。
A.冷水 B.沸水 C.NaOH稀溶液 D.NaCl浓溶液
(2)区分Fe(OH)3胶体与FeCl3溶液的方法是_______ ,分离提纯Fe(OH)3胶体的方法是_______ 。
(3)氢氧化铁胶体能稳定存在的原因是_______ (选填序号)。
A.胶体微粒直径在1 nm -100nm之间 B.胶体微粒能透过滤纸
C.胶体微粒做布朗运动 D.胶体微粒带电荷
(1)NaCl、KCl、NaClO、MgCl2
(2)H3PO4 、H2SO3 、HCl、HNO3
(3)CO2、CaO、 SO3、SO2
(4)空气、盐酸、氨水、胆矾
(5)Mg、Al、Zn、S
II.某课外活动小组进行Fe(OH)3胶体的制备实验并检验其相关性质。
(1)若将饱和FeCl3溶液分别滴入下列液体中,不能形成Fe(OH)3胶体的是
A.冷水 B.沸水 C.NaOH稀溶液 D.NaCl浓溶液
(2)区分Fe(OH)3胶体与FeCl3溶液的方法是
(3)氢氧化铁胶体能稳定存在的原因是
A.胶体微粒直径在1 nm -100nm之间 B.胶体微粒能透过滤纸
C.胶体微粒做布朗运动 D.胶体微粒带电荷
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】某校学生在学习完胶体的知识后,利用化学兴趣社团活动时间,在实验室中用饱和FeCl3溶液制备Fe(OH)3胶体。具体操作是:取一支烧杯,加入适量的蒸馏水,加热至沸腾。将少量饱和FeCl3溶液分多次缓慢滴入,继续加热至刚好变成红褐色,停止加热。
(1)该反应的化学方程式为___________ 。证明有氢氧化铁胶体生成的实验操作和现象是___________ 。
(2)乙同学认为Fe(OH)3胶体中可能含有FeCl3溶液,为了提纯Fe(OH)3胶体,他可以采用的提纯方法是___________ 。
(3)丙同学将制备好的Fe(OH)3胶体装入U型玻璃管中,插入电极,连通直流电,进行电泳
实验。一段时间后,观察到阴极附近液体颜色加深,原因是:___________ 。
(4)丁同学取适量Fe(OH)3胶体于试管,然后用胶头滴管逐滴向试管中加入稀硫酸,看到的现象是先产生红褐色沉淀,原因是:___________ ,随着稀硫酸的不断滴加,沉淀又溶解,发生的离子反应为:___________ 。
(1)该反应的化学方程式为
(2)乙同学认为Fe(OH)3胶体中可能含有FeCl3溶液,为了提纯Fe(OH)3胶体,他可以采用的提纯方法是
(3)丙同学将制备好的Fe(OH)3胶体装入U型玻璃管中,插入电极,连通直流电,进行电泳
实验。一段时间后,观察到阴极附近液体颜色加深,原因是:
(4)丁同学取适量Fe(OH)3胶体于试管,然后用胶头滴管逐滴向试管中加入稀硫酸,看到的现象是先产生红褐色沉淀,原因是:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】由工业明胶制成的胶囊往往含有超标的重金属铬,从而对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知 中铬元素是+3价,则其中铁元素是
中铬元素是+3价,则其中铁元素是___________ 价。 是一种酸根离子,则
是一种酸根离子,则 属于
属于___________ (填“酸”“碱”“盐”或“氧化物”)。
(2)区分明胶的水溶液和 溶液的方法是
溶液的方法是___________ 。胶体与溶液的本质区别是___________ 。
(3)若将饱和 溶液分别滴入下列液体中,能形成胶体的是___________。
溶液分别滴入下列液体中,能形成胶体的是___________。
(4)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。现有10mL明胶的水溶液与5mL 溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计一个实验证明
溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计一个实验证明 能够透过半透膜:
能够透过半透膜:___________ 。
(1)已知
 中铬元素是+3价,则其中铁元素是
中铬元素是+3价,则其中铁元素是 是一种酸根离子,则
是一种酸根离子,则 属于
属于(2)区分明胶的水溶液和
 溶液的方法是
溶液的方法是(3)若将饱和
 溶液分别滴入下列液体中,能形成胶体的是___________。
溶液分别滴入下列液体中,能形成胶体的是___________。| A.冷水 | B.沸水 | C.NaOH浓溶液 | D.NaCl浓溶液 |
 溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计一个实验证明
溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计一个实验证明 能够透过半透膜:
能够透过半透膜:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】有五种等浓度溶液①Na2SO3、②BaCl2、③AgNO3、④NaOH、⑤X五种溶液(X为某未知溶液),将部分溶液两两混合,现象如下表所示:
查阅资料:Na2SO3类似Na2CO3,具有某些相似的化学性质
(1)将表格补充完整。a._________________ ;b.____________________ ;
(2)预测②与④不能发生反应,依据是_________________________________________________ 。
(3)猜测⑤是H2SO4,因此在实验iii的基础上增加实验iv,证明了猜测。实验iv的操作及现象是:(所需试剂任选)。__________________________________________________________________________________
查阅资料:Na2SO3类似Na2CO3,具有某些相似的化学性质
| 序号 | 操作 | 现象 | 离子方程式 |
| i | ①+② | 白色沉淀 | a |
| ii | ②+③ | b | c |
| iii | ①+⑤ | 无色气体 | d |
(1)将表格补充完整。a.
(2)预测②与④不能发生反应,依据是
(3)猜测⑤是H2SO4,因此在实验iii的基础上增加实验iv,证明了猜测。实验iv的操作及现象是:(所需试剂任选)。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】某化学兴趣小组在课外活动中,对某溶液进行了多次检测,其中两次检测结果如下表所示,请回答下列问题:
(1)在上述的两次检测中,如果检测结果正确的那一次涉及的五种离子(顺序见上表)个数之比为4∶5∶1∶x∶3,则x=___________ 。
(2)为了进一步确认检验溶液中存在的 、
、 和Cl-,按照下列步骤依次进行:
和Cl-,按照下列步骤依次进行:
第一步:向溶液中滴加过量的___________ 溶液(填化学式),其目的是确认 并将其除去;发生反应的
并将其除去;发生反应的离子方程式 为___________ ;
第二步:加入过量的___________ 溶液(填化学式),其目的是确认 并将其除去;发生反应的
并将其除去;发生反应的离子方程式 为___________ ;
第三步:过滤,再向滤液中加入___________ 溶液(填化学式),其目的是确认Cl-离子。
| 检测次数 | 溶液中检测出的离子 |
| 第①次 | K+、Na+、 、 、 、Cl- 、Cl- |
| 第②次 | K+、Na+、Ba2+、Cl-、 |
(2)为了进一步确认检验溶液中存在的
 、
、 和Cl-,按照下列步骤依次进行:
和Cl-,按照下列步骤依次进行:第一步:向溶液中滴加过量的
 并将其除去;发生反应的
并将其除去;发生反应的第二步:加入过量的
 并将其除去;发生反应的
并将其除去;发生反应的第三步:过滤,再向滤液中加入
您最近一年使用:0次
【推荐3】为除去粗盐中的Ca2+、Mg2+、SO 及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
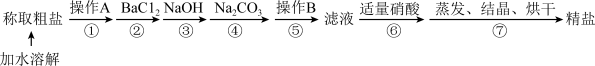
(1)第①步中,操作A是_______ ,第⑤步中,操作B是_______ 。
(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为氯化钙)_______ 。
(3)第②步和第③步操作是否可以调换?_______ 理由是_______ 。
(4)第②步与第④步操作是否可以调换?_______ 原因是_______ 。
(5)若先用盐酸调溶液至中性,再过滤,将对实验结果产生影响,其原因:_______ 。
(6)如何判断SO 已经除尽?
已经除尽?_______ 。
 及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
(1)第①步中,操作A是
(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为氯化钙)
(3)第②步和第③步操作是否可以调换?
(4)第②步与第④步操作是否可以调换?
(5)若先用盐酸调溶液至中性,再过滤,将对实验结果产生影响,其原因:
(6)如何判断SO
 已经除尽?
已经除尽?
您最近一年使用:0次



