天津市和平区耀华中学2019-2020学年高一上学期第一次月考化学试题
天津
高一
阶段练习
2020-08-26
464次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、化学实验基础、化学反应原理
一、单选题 添加题型下试题
| A.金属氧化物一定是碱性氧化物,非金属氧化物一定是酸性氧化物 |
| B.碱性氧化物一定是金属氧化物,酸性氧化物不一定是非金属氧化物 |
| C.碱性氧化物都能与水化合生成碱 |
| D.酸性氧化物都能与水化合生成酸 |
【知识点】 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系解读
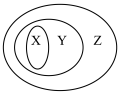
| X | Y | Z | |
| A | 氧化物 | 化合物 | 纯净物 |
| B | 电解质 | 盐 | 化合物 |
| C | 胶体 | 分散系 | 混合物 |
| D | 碱性氧化物 | 金属氧化物 | 氧化物 |
| A.A | B.B | C.C | D.D |
| A.加入碘水变蓝色 | B.加入碘水溶液不变蓝色 |
| C.加入AgNO3溶液产生黄色沉淀 | D.加入溴水变蓝色 |
【知识点】 胶体的性质和应用解读 溴、碘的性质 化学实验方案的设计与评价
| A.利用丁达尔现象可以鉴别胶体和溶液 |
| B.在豆浆里加入盐卤做豆腐与胶体的聚沉有关 |
| C.胶体与溶液的分离可用渗析的方法 |
| D.KCl溶液、淀粉溶液和纯水都属于分散系 |
| A.石墨、醋酸溶液、食盐晶体 |
| B.熔融的KOH、熔融的NaCl、熔融的 KCl |
| C.稀 H2SO4、NaOH 溶液、稀 HNO3 |
| D.食盐水、石灰水、水银 |
| A.盐酸中逐滴加入食盐溶液 | B.硫酸中逐滴加入氢氧化钠溶液 |
| C.硫酸中逐滴加入氢氧化钡溶液 | D.醋酸中逐滴加入氨水 |
| A.含最高价元素的化合物,一定具有强氧化性 |
| B.氧化剂在同一反应中既可以是反应物,也可以是生成物 |
| C.失电子多的还原剂,还原性就强 |
| D.化学反应中,某元素由化合态变为游离态,此元素可能被氧化,也可能被还原 |
| A.含金属元素的离子一定都是阳离子 |
| B.在氧化还原反应中,非金属单质一定是氧化剂 |
| C.金属元素从化合态变为游离态,该元素一定被还原 |
| D.金属阳离子被还原一定得到金属单质 |
【知识点】 氧化还原反应基本概念 金属通性
A.Mg2+、Na+、NO 、SO 、SO | B.Na+、K+、NO 、HCO 、HCO |
C.K+、Ba2+、Cl-、NO | D.Na+、Cl-、K+、MnO |
【知识点】 限定条件下的离子共存解读
| A.氢氧化钠与盐酸;氢氧化钾与碳酸 |
| B.BaCl2 溶液与Na2SO4 溶液;Ba(OH)2 溶液与H2SO4 溶液 |
| C.NaHCO3 溶液与 KHSO4 溶液;Ca(HCO3)2 溶液与过量HCl溶液 |
| D.氧化钠与稀盐酸混合;氧化铜与稀盐酸 |
【知识点】 离子反应的发生及书写 离子方程式的正误判断解读
| A.金属钠和氧气反应,条件不同,产物不同 |
| B.钠钾合金通常状况下呈液态,可作原子反应堆的导热剂 |
| C.钠的化学活泼性很强,少量的钠可保存在有机溶剂 CCl4 中 |
| D.钠比较活泼,但是它不能从溶液中置换出金属活动顺序表中钠后面的金属 |
| A.Na2CO3 比NaHCO3 稳定 |
| B.Na2CO3 比NaHCO3 易溶于水 |
| C.相同质量的Na2CO3 和NaHCO3 分别与足量盐酸反应,Na2CO3 放出 CO2 少 |
| D.Na2CO3 和NaHCO3 溶液分别与同浓度的盐酸反应,Na2CO3 反应的速率比NaHCO3 快 |
【知识点】 碳酸氢钠与酸反应解读 碳酸钠与碳酸氢钠性质的比较解读
| A.不同 | B.相同 | C.②是还原剂作用 | D.③是氧化剂的作用 |
| A.5:3 | B.5:4 | C.1:1 | D.3:5 |
【知识点】 氧化还原反应基本概念 氧化还原反应有关计算
①2Fe2++Br2=2Fe3++2Br- ②2Fe3++2I-=2Fe2++I2
③2MnO
 +16H++10Br-=2Mn2++5Br2 +8H2O ④I2 +SO2+2H2O=4H++SO
+16H++10Br-=2Mn2++5Br2 +8H2O ④I2 +SO2+2H2O=4H++SO +2I-
+2I-据此,判断出氧化性由强到弱的正确顺序是
A.MnO >Fe3+>Br2 >I2 >SO2 >Fe3+>Br2 >I2 >SO2 | B.MnO >Br2>Fe3+>I2>SO2 >Br2>Fe3+>I2>SO2 |
C.MnO >Br2>Fe3+>SO2>I2 >Br2>Fe3+>SO2>I2 | D.Br2>MnO >Fe3+>I2>SO2 >Fe3+>I2>SO2 |
 =2X2++5Z2+8H2O
=2X2++5Z2+8H2O②2A2++B2=2A3++2B-
③2B-+Z2=B2+2Z-
由此推断下列说法错误的是( )
| A.反应Z2+2A2+=2A3++2Z-可以进行 |
| B.Z元素在反应③中被还原,在反应①中被氧化 |
C.氧化性由强到弱的顺序是XO 、Z2、B2、A3+ 、Z2、B2、A3+ |
| D.还原性由强到弱的顺序是Z-、B-、A2+、X2+ |
| A.澄清石灰水通入少量二氧化碳:Ca(OH)2+CO2=CaCO3↓+H2O |
| B.铜与 FeCl3 溶液反应 :Cu+Fe3+=Cu2++Fe2+ |
C.碳酸氢钙溶液与过量烧碱溶液反应:Ca2++2HCO +2OH-=CaCO3 ↓+CO +2OH-=CaCO3 ↓+CO +2H2O +2H2O |
D.亚硫酸钡与足量盐酸反应:SO +2H+=H2O+SO2↑ +2H+=H2O+SO2↑ |
【知识点】 离子反应的发生及书写 离子方程式的正误判断解读
| A.上述三个反应都有单质生成,所以都是置换反应 |
| B.氧化性由强到弱顺序为 KBrO3>KClO3>Cl2>Br2 |
| C.反应②中氧化剂与还原剂的物质的量之比为1:6 |
| D.③中 1 mol 还原剂反应,则氧化剂得到电子的物质的量为 2 mol |

| A.H2、Fe2O3 | B.CO、Na2CO3 |
| C.CO、Na2O2 | D.H2、NaHCO3 |
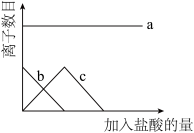
A.Na+、 、 、 | B.Cl一、Na+、 |
C.Na+、 、 、 | D.Na+、 、H+ 、H+ |
| A.2.3g | B.3.1g | C.4.6g | D.5.3g |
二、填空题 添加题型下试题
(1)能导电的是
(2)属于电解质的是
(3)属于非电解质的是
【知识点】 电解质与非电解质
(1)碳酸钙与醋酸反应
(2)等体积、等物质量浓度的 NaHCO3 溶液和 Ba(OH)2混合
(3)向 NaHSO4 溶液中逐滴加入Ba(OH)2 至 SO
 完全沉淀
完全沉淀(4)Na 投入到 CuSO4 溶液中
(5)铜与稀硝酸反应生成硝酸铜、一氧化氮和水
【知识点】 离子反应的发生及书写 离子方程式的书写解读
①反应中
②用单线桥标出电子转移方向和数目
③反应产物中,所得氧化产物与还原产物物质的量之比为
 →NO
→NO(1)该反应的氧化剂是.
(2)该反应中,发生氧化反应的过程是
(3)写出该反应的化学方程式,并标出电子转移的方向和数目:
 ,那么X元素的最终价态为
,那么X元素的最终价态为【知识点】 氧化还原反应有关计算 基于氧化还原反应守恒规律的计算解读
①_ KMnO4+__ K2SO3+___ H2O=____ MnO2+____ K2SO4+__ KOH
②_ K2Cr2O7+_ KI+_ H2SO4=_ K2SO4+_ Cr2(SO4)3+_ I2+_ H2O
③ Cu2S+_ HNO3= _ S+_ NO↑+ _ Cu(NO3)2+ _ H2O
【知识点】 氧化还原反应方程式的配平解读
(1)所得溶液的质量分数;
(2)向该溶液中通入一定量CO2,然后小心蒸干,所得固体冷却干燥,称重为 28.5g,通过计算推出该固体物体的组成和质量。
试卷分析
试卷题型(共 32题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系 | |
| 2 | 0.85 | 分类方法的应用 无机物质的分类 酸、碱、盐、氧化物 分散系概念 | |
| 3 | 0.85 | 胶体的性质和应用 溴、碘的性质 化学实验方案的设计与评价 | |
| 4 | 0.85 | 胶体的定义及分类 胶体的性质和应用 渗析 | |
| 5 | 0.65 | 电解质、非电解质概念 物质水溶液的导电性 强电解质和弱电解质的判断 | |
| 6 | 0.85 | 电解质的电离 物质水溶液的导电性 离子反应的实际应用 | |
| 7 | 0.85 | 氧化还原反应基本概念 氧化还原反应的几组概念 氧化性、还原性强弱的比较 | |
| 8 | 0.65 | 氧化还原反应基本概念 金属通性 | |
| 9 | 0.85 | 限定条件下的离子共存 | |
| 10 | 0.65 | 钠与水反应原理 | |
| 11 | 0.65 | 焰色试验 | |
| 12 | 0.65 | 离子反应的发生及书写 离子方程式的正误判断 | |
| 13 | 0.85 | 钠与氧气等非金属的反应 钠与水反应原理 钠与盐溶液的反应 | |
| 14 | 0.85 | 物质的量浓度的计算 钠与水反应原理 | |
| 15 | 0.65 | 碳酸氢钠与酸反应 碳酸钠与碳酸氢钠性质的比较 | |
| 16 | 0.85 | 氧化还原反应基本概念 氧化还原反应的几组概念 常见氧化剂与还原剂 氧化还原反应的应用 | |
| 17 | 0.85 | 氧化还原反应基本概念 氧化还原反应有关计算 | |
| 18 | 0.85 | 氧化性、还原性强弱的比较 氧化还原反应的应用 氧化还原反应的规律 | |
| 19 | 0.65 | 氧化还原反应的规律 | |
| 20 | 0.65 | 离子反应的发生及书写 离子方程式的正误判断 | |
| 21 | 0.65 | 四种基本反应类型 氧化性、还原性强弱的比较 氧化还原反应的规律 与氧化剂、还原剂有关的计算 | |
| 22 | 0.94 | 氧化还原反应的规律 | |
| 23 | 0.65 | 过氧化钠 碳酸钠 碳酸氢钠的不稳定性 铁的氧化物 | |
| 24 | 0.85 | 离子共存 离子反应的实际应用 碳酸钠 氢氧化钠、碳酸钠混合溶液与盐酸反应相关考查 | |
| 25 | 0.65 | 钠与水反应原理 氧化钠 | |
| 二、填空题 | |||
| 26 | 0.94 | 电解质与非电解质 | |
| 27 | 0.65 | 离子反应的发生及书写 离子方程式的书写 | |
| 28 | 0.65 | 氧化还原反应的几组概念 单线桥、双线桥分析氧化还原反应 氧化还原反应有关计算 | |
| 29 | 0.65 | 单线桥、双线桥分析氧化还原反应 氧化还原反应方程式的配平 氧化还原反应在生活、生产中的应用 | |
| 30 | 0.85 | 氧化还原反应有关计算 基于氧化还原反应守恒规律的计算 | |
| 31 | 0.85 | 氧化还原反应方程式的配平 | |
| 32 | 0.65 | 过氧化钠的相关计算 碳酸钠、碳酸氢钠混合物的有关求算 | |

 在酸性溶液中与MnO
在酸性溶液中与MnO 反应,反应产物为RO2、Mn2+、H2O。已知反应中氧化剂与还原剂的物质的量之比为2∶5,则x的值为
反应,反应产物为RO2、Mn2+、H2O。已知反应中氧化剂与还原剂的物质的量之比为2∶5,则x的值为

