陕西省汉中中学2019届高三上学期第一次月考化学试题
陕西
高三
阶段练习
2018-11-04
442次
整体难度:
适中
考查范围:
有机化学基础、化学与STSE、常见无机物及其应用、认识化学科学、化学实验基础、化学反应原理
一、单选题 添加题型下试题
| A.氢氧化钾 | B.碳酸钠 | C.氧化钙 | D.次氯酸钠 |
【知识点】 油脂的性质 化学科学对人类文明发展的意义解读
| A.A12O3作耐火材料是因为氧化铝熔点高 |
| B.医疗上,碳酸氢钠是治疗胃穿孔的一种药剂 |
| C.明矾可用于自来水的杀菌消毒 |
| D.水玻璃是纯净物。 |
| A.Na2O和H2O | B.Na和H2O |
| C.电解水 | D.Na2O2和H2O |
| A.Na与水反应:Na+H2O=Na++OH-+H2↑ |
| B.明矾净水原理:Al3++3H2O= Al(OH)3↓+3H+ |
| C.实验室盛装NaOH溶液的试剂瓶不能用玻璃塞的原因:SiO2+2OH-=SiO32-+H2O |
| D.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+= Fe 3++3H2O |
【知识点】 离子方程式的正误判断解读
①金属钠投入到FeCl3溶液中 ②过量NaOH溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中 ④Na2O2投入FeCl2溶液中.
| A.只有①④ | B.只有③ | C.只有②③ | D.只有①③④ |
| A.NaOH | B.蔗糖 | C.H2SO4 | D.NaCl |
【知识点】 非电解质、电解质物质类别判断解读
| A.Na+ Ca2+ SO42- CO32- | B.Na+ Cu2+ SO42- OH- |
| C.Na+ H+ Cl- SO42- | D.Na+ H+ Cl- CO32- |
| A.H2CO3+ 2NaOH = Na2CO3+2H2O |
| B.HCl + NH3·H2O = NH4Cl + H2O |
| C.Fe(OH)3+ 3HCl = FeCl3+ 3H2O |
| D.H2SO4+ 2KOH = K2SO4+ 2H2O |
【知识点】 离子反应的发生及书写
| A.加NaOH溶液 | B.加盐酸 | C.通入CO2 | D.加热 |
【知识点】 碳酸钠与碳酸氢钠的相互转化解读
| A.CaCl2溶液 | B.澄清石灰水 |
| C.饱和Na2CO3溶液 | D.稀H2SO4 |
【知识点】 碳酸钠与碳酸氢钠的相互转化解读
 + 3 S2- + 14H+= 2M 3++ 3S↓+ 7H2O,则M2O
+ 3 S2- + 14H+= 2M 3++ 3S↓+ 7H2O,则M2O 中的M的化合价为
中的M的化合价为| A.+2 | B.+3 | C.+4 | D.+6 |
| A.5:3 | B.5:4 | C.1:1 | D.3:5 |
【知识点】 氧化还原反应基本概念 氧化还原反应有关计算
| A.向FeI2溶液中通入少量Cl2:2Fe2++ Cl2=2Fe3++ 2Cl- |
| B.氧化钠与盐酸反应:O2-+2H+ =H2O |
| C.CaCO3悬浊液中通CO2:CO32—+CO2+H2O =2HCO3— |
| D.小苏打溶液与少量Ca(OH)2溶液混合:2HCO3—+2OH-+Ca2+=CaCO3↓+2 H2O+CO32- |
【知识点】 离子方程式的正误判断解读
| A.Ca(HCO3)2 | B.Na2S | C.FeI2 | D.AlCl3 |
【知识点】 过氧化钠
| A.2 4 3 2 2 6 | B.0 2 1 0 1 2 |
| C.2 0 1 2 0 2 | D.2 2 2 2 1 4 |
【知识点】 离子反应的发生及书写 氧化性、还原性强弱的比较解读
 、
、 、
、 、
、 ,向该溶液中加入少量溴水,溶液呈无色,则下列关于溶液组成的判断正确的是
,向该溶液中加入少量溴水,溶液呈无色,则下列关于溶液组成的判断正确的是①肯定不含
 ②肯定不含
②肯定不含 ③肯定含有
③肯定含有 ④可能含有
④可能含有 .
.| A.①③ | B.①②③ | C.③④ | D.②③④ |
【知识点】 离子反应在化合物组成的分析、鉴定的应用解读
 完全转化为N2,该反应可表示为2NH
完全转化为N2,该反应可表示为2NH +3ClO-=N2↑+3Cl-+2H++3H2O。下列说法中不正确的是( )
+3ClO-=N2↑+3Cl-+2H++3H2O。下列说法中不正确的是( )| A.反应中氮元素被氧化,氯元素被还原 |
B.还原性:NH >Cl- >Cl- |
| C.反应中每生成1个N2分子,转移6个电子 |
| D.经此法处理过的废水不用再处理就可以直接排放 |
二、填空题 添加题型下试题
(1)84消毒液的主要成分是次氯酸钠,次氯酸钠与空气中CO2反应生成次氯酸,写出次氯酸钠的电子式:
(2)洁厕灵的主要成分是HCl。洁厕液与84消毒液混合后会发生氧化还原反应,生成有毒的氯气。写出该反应的离子方程式:
(3)下列氧化还原反应中,与上述反应类型不同的是________。
| A.Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O | B.2FeCl3+Fe=3FeCl2 |
C.S+2H2SO4(浓) 3SO2↑+2H2O 3SO2↑+2H2O | D.KClO3+5KCl+3H2SO4=3K2SO4+3Cl2↑+3H2O |
II.已知高锰酸钾(硫酸酸化)溶液和草酸(H2C2O4)溶液可以发生氧化还原反应。请回答下列问题:
(4)该反应中的还原剂是
(5)写出该反应的离子方程式:
(6)若生成1molCO2则转移电子
【知识点】 有关粒子结构的化学用语 氧化还原反应的应用 漂白粉和漂粉精
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液.在FeCl2溶液中需加入少量铁屑,其目的是
(2)甲组同学取2mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和l滴KSCN溶液,溶液变红,煤油的作用是
(4)丙组同学取10 mL0.1mol/LKI溶液,加入6mL0.1mol/LFeCl3溶液混合。分别取2mL此溶液于3 支试管中进行如下实验:
①第一支试管中加入1mLCCl4充分振荡、静置,CCl4层呈紫色;
②第二支试管中加入1滴K3[Fe(CN)6] 溶液,生成蓝色沉淀:
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是
(5)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为
三、解答题 添加题型下试题
(1)选择仪器。完成本实验所必需的仪器有:托盘天平(精确到0.1 g)、药匙、烧杯、量筒、玻璃棒、
(2)计算,应选择下列
A.需要CuSO4固体8 g B.需要CuSO4固体7.7 g
C.需要CuSO4·5H2O晶体12.5 g D.需要CuSO4·5H2O晶体12.0 g
(3)称量。所用砝码生锈则所配溶液的浓度会
(4)溶解、冷却,该步实验中需要使用玻璃棒,目的是
(5)转移、洗涤。在转移时应使用
(6)定容,摇匀。
(7)将配好的溶液静置一段时间后,倒入指定的试剂瓶,贴好标签,注明配制的时间、溶液名称及浓度。
(8)在配制过程中,某学生观察定容时液面情况如图所示,所配溶液的浓度会
四、填空题 添加题型下试题
(1)用Fe2(SO4)3吸收H2S。在配制硫酸铁溶液时需要向溶液中加入一定量的硫酸,其目的是:
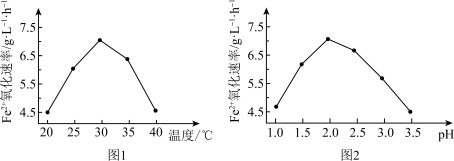
图1、图2为再生时Fe2+的转化速率与反应条件的关系。再生的最佳条件为
(2)在一定条件下,用H2O2氧化H2S。
随着参加反应的n(H2O2)/n(H2S)变化,氧化产物不同。当n(H2O2)/n(H2S)=4时,氧化产物的化学式为
(3)H2S与CO2在高温下反应可生成氧硫化碳(COS),其结构式为
(4)加热条件下用O2氧化H2S,使硫元素转化为硫单质并回收,写出氧气氧化硫化氢的反应方程式:
【知识点】 氧化还原反应方程式的配平解读 硫化氢解读 盐类水解的应用
试卷分析
试卷题型(共 24题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 油脂的性质 化学科学对人类文明发展的意义 | |
| 2 | 0.85 | 硅酸钠的俗名和用途 碳酸氢钠 明矾 氧化铝的物理性质与用途 | |
| 3 | 0.85 | 分散系概念及其分类 胶体的制备 石油分馏 煤的综合利用 | |
| 4 | 0.85 | 氧化还原反应的几组概念 钠与水反应原理 氧化钠的化学性质 过氧化钠与水的反应 | |
| 5 | 0.85 | 硅的制备 电解法制取铝 海水中盐的开发及利用 海水提取镁 | |
| 6 | 0.65 | 离子方程式的正误判断 | |
| 7 | 0.65 | 钠与盐溶液的反应 过氧化钠与水的反应 碳酸氢钠与碱反应 铝盐与强碱溶液反应 | |
| 8 | 0.94 | 非电解质、电解质物质类别判断 | |
| 9 | 0.65 | 物质共存 | |
| 10 | 0.85 | 离子反应的发生及书写 | |
| 11 | 0.85 | 碳酸钠与碳酸氢钠的相互转化 | |
| 12 | 0.85 | 铵盐与碱反应 | |
| 13 | 0.94 | 碳酸钠与碳酸氢钠的相互转化 | |
| 14 | 0.85 | 氧化还原反应有关计算 氧化还原反应方程式的书写与配平 基于氧化还原反应守恒规律的计算 | |
| 15 | 0.85 | 氧化还原反应基本概念 氧化还原反应有关计算 | |
| 16 | 0.65 | 离子方程式的正误判断 | |
| 17 | 0.65 | 过氧化钠 | |
| 18 | 0.65 | 离子反应的发生及书写 氧化性、还原性强弱的比较 | |
| 19 | 0.65 | 离子反应在化合物组成的分析、鉴定的应用 | |
| 20 | 0.65 | 氧化还原反应的几组概念 氧化性、还原性强弱的比较 电子转移计算 | |
| 二、填空题 | |||
| 21 | 0.65 | 有关粒子结构的化学用语 氧化还原反应的应用 漂白粉和漂粉精 | |
| 22 | 0.65 | 离子方程式的书写 Fe2+的鉴别及其应用 Fe2+的还原性 亚铁盐溶液的配制与保存 | |
| 24 | 0.4 | 氧化还原反应方程式的配平 硫化氢 盐类水解的应用 | |
| 三、解答题 | |||
| 23 | 0.85 | 配制一定物质的量浓度的溶液的步骤、操作 配制一定物质的量浓度的溶液实验的误差分析 配制一定物质的量浓度的溶液实验的仪器 配制一定物质的量浓度溶液的综合考查 | 实验探究题 |



